名校
1 . 在一定条件下,体积不变的密闭容器中,发生可逆反应2SO2(g)+O2(g)  2SO3(g) ΔH<0,达到平衡后,当单独改变下列条件后,有关叙述正确的是
2SO3(g) ΔH<0,达到平衡后,当单独改变下列条件后,有关叙述正确的是
 2SO3(g) ΔH<0,达到平衡后,当单独改变下列条件后,有关叙述正确的是
2SO3(g) ΔH<0,达到平衡后,当单独改变下列条件后,有关叙述正确的是| A.增大压强,平衡正向移动,此反应的ΔH仍保持不变 |
| B.增大O2浓度,SO2的平衡转化率减小 |
| C.降低温度,化学平衡常数减小 |
| D.升高温度,SO2的转化率一定增大 |
您最近一年使用:0次
2018-11-03更新
|
229次组卷
|
3卷引用:河北省唐山市第一中学2018-2019学年高二上学期10月月考化学试题
名校
2 . 对于平衡体系mA(g)+nB(g)⇌pC(g)+qD(g) △H=b kJ·mol-1,下列结论中错误的是
| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q |
| B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C.保持其它条件不变,升高温度,D的体积分数增大说明该反应的△H<0。 |
| D.若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol |
您最近一年使用:0次
2018-07-25更新
|
284次组卷
|
7卷引用:【全国校级联考】辽宁省抚顺市六校2017-2018学年高一下学期期末考试化学试题
名校
3 . 反应N2O4(g) 2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

 2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深,c浅 |
| C.b、c两点的转化率:b>c |
| D.由b点到a点,可以用加热的方法 |
您最近一年使用:0次
2018-07-25更新
|
3283次组卷
|
11卷引用:【全国校级联考】辽宁省抚顺市六校2017-2018学年高一下学期期末考试化学试题
【全国校级联考】辽宁省抚顺市六校2017-2018学年高一下学期期末考试化学试题安徽省宣城市郎溪县郎溪中学2018-2019学年高二上学期直升部返校考化学试题四川省成都市外国语学校2019届高三上学期开学考试化学试题吉林省长春汽车经济开发区第六中学2018-2019学年高二上学期第一次月考化学试题安徽省阜阳市第三中学2018-2019学年高一下学期第二次调研考试化学试题福建省莆田市私立一中2019-2020学年高二上学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——选修四化学反应原理——化学反应速率及其影响因素专练(已下线)2.3.3 温度对化学平衡的影响(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)黑龙江省大庆市东风中学2021-2022学年高二上学期期中考试化学试题福建省福州第三中学2022-2023学年高二上学期半期考试化学试题福建省漳州市正兴学校2023-2024学年高二上学期10月月考化学试卷
名校
4 . 氮及其化合物在工业生产中有广泛用。
(1)稀硝酸与二价活泼金属M反应制备硝酸盐,当反应物之比n(HNO3)∶n(M)=5∶2时,还原产物为___ (填化学式)。
(2)连二次硝酸(HO-N=N-OH)是一种二元弱酸,向0.1 mol·L-1连二次硝酸钠(Na2N2O2)溶液中滴加酚酞,溶液变红色 ,用离子方程式表示其主要原因:__________________ 。
(3)已知以下热化学方程式: 2N2O5(g) 4NO2(g)+O2(g) ΔH1
4NO2(g)+O2(g) ΔH1
2NO(g)+O2(g)=2NO2(g) ΔH2
3NO2(g) N2O5(g)+NO(g) ΔH3
N2O5(g)+NO(g) ΔH3
①ΔH3=______________________ (用ΔH1、ΔH2表示)。
②一定温度下,在恒容密闭容器中进行反应:3NO2(g) N2O5(g)+NO(g),下列表明反应已达到平衡状态的是
N2O5(g)+NO(g),下列表明反应已达到平衡状态的是________ 。
A.容器内总压强保持不变 B.容器内气体密度保持不变
C.v正(NO2)∶v逆(N2O5)=3∶1 D. 保持不变
保持不变
(4)在密闭容器中充入NO,发生反应2NO(g) N2(g)+O2(g) ΔH,达到平衡之后,升高温度,平衡常数K减小。
N2(g)+O2(g) ΔH,达到平衡之后,升高温度,平衡常数K减小。
①ΔH________ 0。(填“>”“<”或“=”)
②上述反应达到平衡之后,仅缩小容器体积,下列推断正确的是_________ 。
A.NO的浓度不再变化
B.NO的转化率不再变化
C.正、逆反应速率不再变化
D.容器内气体压强不再变化
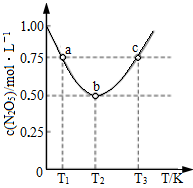
(5)在2 L恒容密闭容器中投入一定量的N2O5(g),发生反应:2N2O5(g) 4NO2(g)+O2(g),测得c(N2O5)与温度关系如图所示。T2 K时,该反应的平衡常数K为
4NO2(g)+O2(g),测得c(N2O5)与温度关系如图所示。T2 K时,该反应的平衡常数K为_________ 。若平衡时温度不变,再向容器中充入少量的N2O5气体,达到新平衡时N2O5的转化率会_________ (填“增大”“减小”或“不变”)。
(1)稀硝酸与二价活泼金属M反应制备硝酸盐,当反应物之比n(HNO3)∶n(M)=5∶2时,还原产物为
(2)连二次硝酸(HO-N=N-OH)是一种二元弱酸,向0.1 mol·L-1连二次硝酸钠(Na2N2O2)溶液中滴加酚酞,溶液变红色 ,用离子方程式表示其主要原因:
(3)已知以下热化学方程式: 2N2O5(g)
 4NO2(g)+O2(g) ΔH1
4NO2(g)+O2(g) ΔH12NO(g)+O2(g)=2NO2(g) ΔH2
3NO2(g)
 N2O5(g)+NO(g) ΔH3
N2O5(g)+NO(g) ΔH3①ΔH3=
②一定温度下,在恒容密闭容器中进行反应:3NO2(g)
 N2O5(g)+NO(g),下列表明反应已达到平衡状态的是
N2O5(g)+NO(g),下列表明反应已达到平衡状态的是A.容器内总压强保持不变 B.容器内气体密度保持不变
C.v正(NO2)∶v逆(N2O5)=3∶1 D.
 保持不变
保持不变(4)在密闭容器中充入NO,发生反应2NO(g)
 N2(g)+O2(g) ΔH,达到平衡之后,升高温度,平衡常数K减小。
N2(g)+O2(g) ΔH,达到平衡之后,升高温度,平衡常数K减小。①ΔH
②上述反应达到平衡之后,仅缩小容器体积,下列推断正确的是
A.NO的浓度不再变化
B.NO的转化率不再变化
C.正、逆反应速率不再变化
D.容器内气体压强不再变化
(5)在2 L恒容密闭容器中投入一定量的N2O5(g),发生反应:2N2O5(g)
 4NO2(g)+O2(g),测得c(N2O5)与温度关系如图所示。T2 K时,该反应的平衡常数K为
4NO2(g)+O2(g),测得c(N2O5)与温度关系如图所示。T2 K时,该反应的平衡常数K为
您最近一年使用:0次
5 . 向两个体积可变的密闭容器中均充入1mol 的A2 和2mol的B2发生反应:A2(g)+2B2(g) 2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2 的体积分数随温度的变化如图所示。
2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2 的体积分数随温度的变化如图所示。
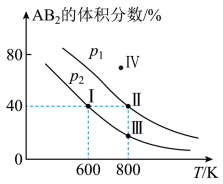
已知: 图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上;IV点不在曲线上
下列叙述正确的是
 2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2 的体积分数随温度的变化如图所示。
2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2 的体积分数随温度的变化如图所示。
已知: 图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上;IV点不在曲线上
下列叙述正确的是
| A.Ⅰ点和Ⅱ点反应速率相等 | B.IV点时反应未到达平衡v(正)<v(逆) |
| C.I点时,A的平衡转化率为40% | D.将点II所对应容器冷却到600K,可变成点I |
您最近一年使用:0次
2018-03-24更新
|
797次组卷
|
3卷引用:浙江省十校联盟(学考)选考2018年3月适应性考试化学试题
浙江省十校联盟(学考)选考2018年3月适应性考试化学试题河南省鹤壁市淇县第一中学2018-2019学年高二上学期第一次月考化学试题(已下线)专题17 化学平衡图表分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
解题方法
6 . 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s) + CO2(g) 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
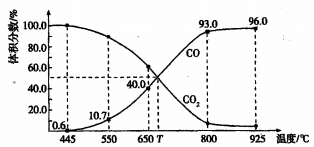
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
| A.550℃时,若充入惰性气体,V正、V逆均减小,平衡不移动 |
| B.650℃时,反应达平衡后CO2的转化率为40.0% |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= 23. 04p总 |
您最近一年使用:0次
2018-02-06更新
|
1277次组卷
|
5卷引用:新疆乌鲁木齐地区2018届高三第一次诊断测试化学试题
名校
7 . 在温度相同、容积均为2L的三个恒容密闭容器中,按不同方式投入反应物,发生反应:N2(g)+3H2(g)  2NH3(g)△H= -92.4kJ/mol;保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
2NH3(g)△H= -92.4kJ/mol;保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
 2NH3(g)△H= -92.4kJ/mol;保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
2NH3(g)△H= -92.4kJ/mol;保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molN2、6molH2 | 2molNH3 |
| NH3 的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
| 体系压强 | p1 | p2 | p3 |
| 反应物转化率 |  |  |  |
| A.2p1=2p3<p2 | B.达到平衡时丙容器中NH3的体积分数最大 |
C.Q3+92.4 =92.4 =92.4 | D.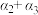 <1 <1 |
您最近一年使用:0次
名校
8 . 常温下,将一定量的氨基甲酸铵置于密闭真空容器中(固体体积忽略不计)发生反应:H2NCOONH4(s) 2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是
2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是
 2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是
2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是| A.混合气体的平均相对分子质量不再变化时表明达到平衡状态 |
| B.达到新平衡时,△H为原来的2倍 |
| C.上述反应达到新平衡状态时x=2a |
| D.上述反应体系中,压缩容器体积过程中n(H2NCOONH4)不变 |
您最近一年使用:0次
2018-01-20更新
|
2869次组卷
|
14卷引用:河北省邯郸市2018届高三1月教学质量检测化学试题
河北省邯郸市2018届高三1月教学质量检测化学试题河北省定州中学2018届高三高中毕业班下学期开学考试化学试题【全国百强校】河南省林州市第一中学2017-2018学年高二5月月考化学试题河北省辛集市第一中学2017-2018学年高一下学期期末考试化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校2020届高三上学期期末考试化学试题重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题河北省石家庄市第二中学2019-2020高一下学期期末考试模拟化学试题(一)河北省石家庄市第二中学2019-2020高一下期末考试化学模拟试题(三)河北省石家庄市第二中学2019-2020高一下学期期末考试模拟(四)化学试题安徽省马鞍山市含山县含山中学2020-2021学年高二上学期第一次月考化学试题黑龙江省大庆实验中学2020-2021学年高二上学期期末考试化学试题江西省南昌市新建区第二中学2019-2020学年高一下学期“新星计划”体验营7月期终考试化学试题陕西省西安市西航一中2021-2022学年高二上学期期中考试化学试题山西省山西大学附属中学2022-2023学年高二上学期10月考化学试题
名校
9 . 对于平衡体系:a A(g)+b B(g) c C(g)+d D(s) △H<0,下列判断中正确的是
c C(g)+d D(s) △H<0,下列判断中正确的是
 c C(g)+d D(s) △H<0,下列判断中正确的是
c C(g)+d D(s) △H<0,下列判断中正确的是| A.若(a+b) < (c+d),则反应一定能自发向右进行 |
| B.若起始时只充入A、B,且物质的量之比为a:b,则平衡时A、B的转化率之比为a:b |
| C.若a+b = c+d,往含m mol气体的平衡体系中充入n mol B,则达到平衡时气体总物质的量等于(m+n)mol。 |
| D.若a+b = c,对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强增大 |
您最近一年使用:0次
10 . 以下是关于“外界因素对化学平衡移动影响的实验研究”的课题,回答问题:
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是________ ,所以影响化学平衡的因素可以从分析影响的因素入手.
a. v(正)≠v(逆) .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 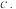 v(正)和v(逆)都减小
v(正)和v(逆)都减小
(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
 .
.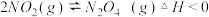
 .
.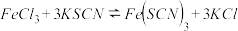
其中, 适合于研究
适合于研究_______ 对平衡的影响, 适合于研究
适合于研究_______ 对平衡的影响.
 .浓度
.浓度  .温度
.温度  .压强
.压强  .催化剂
.催化剂
②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
 .浓度:将
.浓度:将 与
与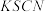 反应后所得的混合液分为
反应后所得的混合液分为 等份,分别加入浓
等份,分别加入浓 溶液、浓
溶液、浓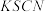 溶液和
溶液和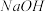 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓 溶液后的混合溶液红色
溶液后的混合溶液红色________ ,加入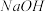 固体后,混合溶液红棕色
固体后,混合溶液红棕色________ .
 .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有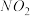 的两个玻璃球,一个放入热水中,另一个放入冷水中.
的两个玻璃球,一个放入热水中,另一个放入冷水中.
现象:放入热水中的球内红棕色________ ;放入冷水中的球内红棕色________ .
(4)综合(3)能得出的影响化学平衡移动的原因是________ .
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是
a. v(正)≠v(逆)
 .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 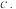 v(正)和v(逆)都减小
v(正)和v(逆)都减小(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
 .
.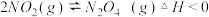
 .
.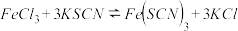
其中,
 适合于研究
适合于研究 适合于研究
适合于研究 .浓度
.浓度  .温度
.温度  .压强
.压强  .催化剂
.催化剂②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
 .浓度:将
.浓度:将 与
与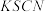 反应后所得的混合液分为
反应后所得的混合液分为 等份,分别加入浓
等份,分别加入浓 溶液、浓
溶液、浓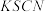 溶液和
溶液和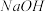 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓 溶液后的混合溶液红色
溶液后的混合溶液红色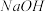 固体后,混合溶液红棕色
固体后,混合溶液红棕色 .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有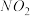 的两个玻璃球,一个放入热水中,另一个放入冷水中.
的两个玻璃球,一个放入热水中,另一个放入冷水中.现象:放入热水中的球内红棕色
(4)综合(3)能得出的影响化学平衡移动的原因是
您最近一年使用:0次



