名校
解题方法
1 . 工业上利用一氧化碳和水蒸气在一定条件下发生的反应来制取氢气:CO(g) + H2O(g)  CO2(g) + H2(g) ΔH = - 41 kJ·mol-1,某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积相等的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应,获得如下数据:
CO2(g) + H2(g) ΔH = - 41 kJ·mol-1,某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积相等的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应,获得如下数据:
(1)容器①中反应达到平衡时,生成H2的物质的量为____ mol。
(2)若容器①体积变为原来的一半,则CO的转化率为_____ (填“增大”“减小”或“不变”)。
(3)计算容器①中反应的平衡常数K =______ 。
(4)容器②中反应的平均速率大于容器①,原因是___________ 。
(5)容器②中反应达到平衡状态后,放出的热量Q____ 65.6kJ(填“>”“=”或“<”)。
 CO2(g) + H2(g) ΔH = - 41 kJ·mol-1,某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积相等的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应,获得如下数据:
CO2(g) + H2(g) ΔH = - 41 kJ·mol-1,某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积相等的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应,获得如下数据:| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡的时间/min | 达到平衡时体系能量的变化 | |||
| CO | H₂O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
(2)若容器①体积变为原来的一半,则CO的转化率为
(3)计算容器①中反应的平衡常数K =
(4)容器②中反应的平均速率大于容器①,原因是
(5)容器②中反应达到平衡状态后,放出的热量Q
您最近一年使用:0次
名校
解题方法
2 . 氢能是一种清洁能源,按照生产过程中的碳排放情况分为灰氢、蓝氢和绿氢。
(1)煤的气化制得灰氢 :C(s) + H2O(g)  CO(g) + H2(g)。该反应的平衡常数表达式K=
CO(g) + H2(g)。该反应的平衡常数表达式K=_____ 。在恒容容器中发生上述反应,下列说法正确的是_______ 。
a. 升高温度,可提高活化分子百分数
b. 将煤粉碎可提高反应速率
c. 断裂2mol H-O的同时断裂1molH-H,反应达到化学平衡状态
d. 容器内混合气体平均摩尔质量不变时,反应达到化学平衡状态
(2)甲烷水蒸气催化重整制得蓝氢 ,步骤如下。
I.H2的制取:CH4(g) + H2O(g) CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0
①为提高CH4的平衡转化率,可采取的措施有___________ (写出两条即可)。
Ⅱ.H2的富集:CO(g) + H2O(g) CO2(g) + H2(g) ΔH<0
CO2(g) + H2(g) ΔH<0
②已知830 ℃时,该反应的平衡常数K=1.在容积不变的的密闭容器中,将2 mol CO与8 mol H2O混合加热到830 ℃。利用三段式 计算反应达平衡时CO的转化率(书写过程) _______ 。
Ⅲ.用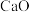 吸收
吸收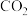 实现低碳排放。
实现低碳排放。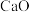 消耗率随时间变化关系如图所示。
消耗率随时间变化关系如图所示。
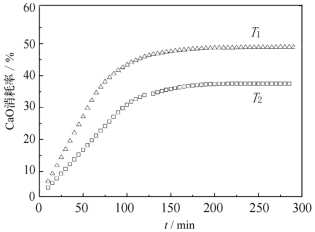
③比较温度高低:T1_____ T2(填“>”或“<”)。
(3)热化学硫碘循环分解水制得绿氢 ,全程零碳排放。反应如下:
反应i:SO2(g) + I2(g) + 2H2O(g) = H2SO4(l) + 2HI(g) ∆H1=-82 kJ·mol−1。
反应ii:2H2SO4(l) = 2SO2(g) + O2(g) + 2H2O(g) ∆H2=+544 kJ·mol−1。
反应iii:∙∙∙∙∙∙
反应ⅰ~iii循环实现分解水:2H2O(g) = 2H2(g) + O2(g) ∆H=+484 kJ·mol−1。
写出反应iii的热化学方程式___________ 。
(1)煤的气化制得
 CO(g) + H2(g)。该反应的平衡常数表达式K=
CO(g) + H2(g)。该反应的平衡常数表达式K=a. 升高温度,可提高活化分子百分数
b. 将煤粉碎可提高反应速率
c. 断裂2mol H-O的同时断裂1molH-H,反应达到化学平衡状态
d. 容器内混合气体平均摩尔质量不变时,反应达到化学平衡状态
(2)甲烷水蒸气催化重整制得
I.H2的制取:CH4(g) + H2O(g)
 CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0①为提高CH4的平衡转化率,可采取的措施有
Ⅱ.H2的富集:CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH<0
CO2(g) + H2(g) ΔH<0②已知830 ℃时,该反应的平衡常数K=1.在容积不变的的密闭容器中,将2 mol CO与8 mol H2O混合加热到830 ℃。利用
Ⅲ.用
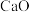 吸收
吸收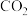 实现低碳排放。
实现低碳排放。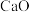 消耗率随时间变化关系如图所示。
消耗率随时间变化关系如图所示。
③比较温度高低:T1
(3)热化学硫碘循环分解水制得
反应i:SO2(g) + I2(g) + 2H2O(g) = H2SO4(l) + 2HI(g) ∆H1=-82 kJ·mol−1。
反应ii:2H2SO4(l) = 2SO2(g) + O2(g) + 2H2O(g) ∆H2=+544 kJ·mol−1。
反应iii:∙∙∙∙∙∙
反应ⅰ~iii循环实现分解水:2H2O(g) = 2H2(g) + O2(g) ∆H=+484 kJ·mol−1。
写出反应iii的热化学方程式
您最近一年使用:0次
解题方法
3 . 丙烯是应用广泛的化工原料,工业上两种利用丙烷制备丙烯的反应如下:
I.丙烷直接脱氢: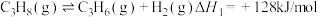
II.氧化丙烷脱氢: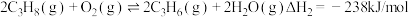
回答下列问题:
(1)反应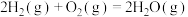 ∆H=
∆H=___________ kJ∙mol-1。
(2)一定条件下,向1L实验容器中充入1mol气态C3H8发生反应Ⅰ。其中主要副反应为:III.丙烷裂解: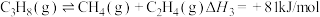 。下图为测得不同温度下C3H6的平衡产率:
。下图为测得不同温度下C3H6的平衡产率:
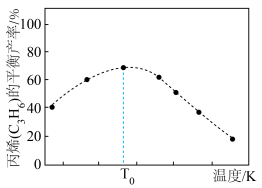
温度高于T0,C3H6的平衡产率随温度升高而减小的原因是___________ 。
(3)运用丙烷直接脱氢法,在相同温度和催化剂条件下,体积均为0.5L的恒容密闭容器中只发生反应I,测得反应的有关数据如下:
①容器a达到平衡时C3H8(g)的平衡浓度为c(C3H8)=___________ ,平衡常数为___________ 。
②容器b经过5分钟达到平衡,则用C3H8(g)表示化学反应速率v(C3H8)=___________ ,反应吸收热量Q为___________ kJ。
③容器c达到平衡时,反应对外___________ (填吸收或放出)热量。
I.丙烷直接脱氢:
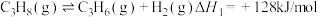
II.氧化丙烷脱氢:
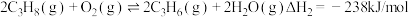
回答下列问题:
(1)反应
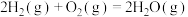 ∆H=
∆H=(2)一定条件下,向1L实验容器中充入1mol气态C3H8发生反应Ⅰ。其中主要副反应为:III.丙烷裂解:
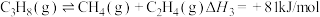 。下图为测得不同温度下C3H6的平衡产率:
。下图为测得不同温度下C3H6的平衡产率:
温度高于T0,C3H6的平衡产率随温度升高而减小的原因是
(3)运用丙烷直接脱氢法,在相同温度和催化剂条件下,体积均为0.5L的恒容密闭容器中只发生反应I,测得反应的有关数据如下:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系的能量变化 | ||
| C3H8(g) | C3H6(g) | H2(g) | ||
| a | 0 | 1 | 1 | 放热32kJ |
| b | 1 | 0 | 0 | 吸热QkJ |
| c | 0.2 | 0.8 | 0.8 | ∆Hc |
②容器b经过5分钟达到平衡,则用C3H8(g)表示化学反应速率v(C3H8)=
③容器c达到平衡时,反应对外
您最近一年使用:0次
4 . 某温度时,H2(g)+CO2(g) H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:
H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:
5 min时达到平衡。平衡时,下列推断不正确的是
 H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:
H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:| 起始浓度 | 甲 | 乙 | 丙 | 丁 |
| c(H2)/(mol/L) | 0.10 | 0.10 | 0.20 | 0.20 |
| c(CO2)/(mol/L) | 0.10 | 0.20 | 0.10 | 0.20 |
| A.5min时,甲中v(CO2)=0.01 mol/(L·mn) | B.乙中CO2转化率等于丙中H2转化率 |
| C.丁中各物质的物质的量相等 | D.甲、乙、丁中c(H2)关系为甲<乙<丁 |
您最近一年使用:0次
5 . NH3经一系列反应可以得到HNO3,如下图所示。
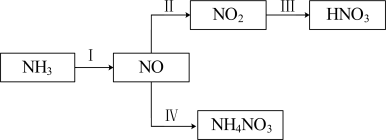
(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是________ 。
(2)Ⅱ中,2NO(g)+O2 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
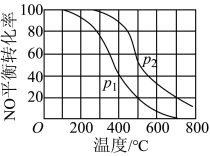
①比较P1、P2的大小关系:______ 。
②随温度升高,该反应平衡常数变化的趋势是______ 。(填“增大”、“减小”或“不变”)
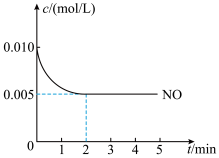
③2NO(g)+O2 2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
a.2min内,v(O2)=________ mol/(L·min)。
b.800℃时,该反应的化学平衡常数为_______ 。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2 (g) N2O4(g) △H1;2NO2 (g)
N2O4(g) △H1;2NO2 (g) N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母)
N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母) ____ 。
A. B.
B.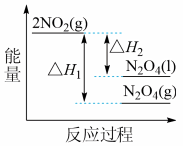 C.
C.
②N2O4与O2、H2O化合的化学方程式是____ 。
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示:
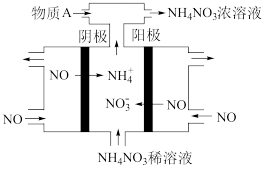
①阳极反应方程式为:___________
②为使电解产物全部转化为NH4NO3,需补充物质A,A是____ 。

(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是
(2)Ⅱ中,2NO(g)+O2
 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
①比较P1、P2的大小关系:
②随温度升高,该反应平衡常数变化的趋势是
③2NO(g)+O2
 2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。a.2min内,v(O2)=
b.800℃时,该反应的化学平衡常数为

(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2 (g)
 N2O4(g) △H1;2NO2 (g)
N2O4(g) △H1;2NO2 (g) N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母)
N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母) A.
 B.
B. C.
C.
②N2O4与O2、H2O化合的化学方程式是
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示:

①阳极反应方程式为:
②为使电解产物全部转化为NH4NO3,需补充物质A,A是
您最近一年使用:0次
6 . 某温度下,反应 的平衡常数为400。此温度下,在容积一定的密闭容器中加入
的平衡常数为400。此温度下,在容积一定的密闭容器中加入 ,反应到某时刻测得各组分的浓度如下:
,反应到某时刻测得各组分的浓度如下:
下列说法正确的是
 的平衡常数为400。此温度下,在容积一定的密闭容器中加入
的平衡常数为400。此温度下,在容积一定的密闭容器中加入 ,反应到某时刻测得各组分的浓度如下:
,反应到某时刻测得各组分的浓度如下:| 物质 |  |  |  |
浓度/( ) ) | 0.44 | 0.6 | 0.6 |
| A.此时逆反应速率大于正反应速率 |
B.平衡时 的转化率小于80% 的转化率小于80% |
C.平衡时 的浓度为0.04mol/L 的浓度为0.04mol/L |
D.该温度下增大 的起始浓度,平衡常数增大 的起始浓度,平衡常数增大 |
您最近一年使用:0次
7 . 一定条件下,向体积为1 L密闭导热容器内加入1 mol  ,发生反应:
,发生反应:
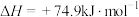 ,达到平衡时吸收q kJ热量。下列说法
,达到平衡时吸收q kJ热量。下列说法不正确 的是
 ,发生反应:
,发生反应:
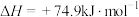 ,达到平衡时吸收q kJ热量。下列说法
,达到平衡时吸收q kJ热量。下列说法| A.当容器内压强不再改变时,说明反应达到平衡状态 |
B.平衡时 的转化率为 的转化率为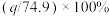 |
C.该反应平衡常数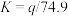 |
D.其它条件不变,初始投料改为2 mol  ,达到平衡时吸热 ,达到平衡时吸热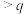 |
您最近一年使用:0次
名校
解题方法
8 . 氨是化学实验室及化工生产中的重要物质,工业上合成氨的部分工艺流程如下:
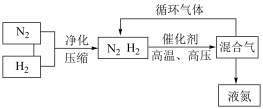
(1)请写出工业合成氨的化学方程式_____ 。
(2)请用平衡移动原理解释在流程中及时分离出氨气和循环使用气体的原因_____ 。
(3)在合成氨工业中原料气( 、
、 、及少量CO、
、及少量CO、 的混合气体)在进入合成塔之前需要经过铜氨液处理,目的是去除其中的CO,其反应为:
的混合气体)在进入合成塔之前需要经过铜氨液处理,目的是去除其中的CO,其反应为:

①铜氨液吸收CO适宜的生产条件是_____ 。
②吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用,铜氨液。再生适宜的生产条件是_____ 。
(4)模拟工业合成氨( ),在恒温恒容密闭容器中进行,起始投料时各物质浓度如下表:
),在恒温恒容密闭容器中进行,起始投料时各物质浓度如下表:
①按投料Ⅰ递行反应,测得达到化学平衡状态时 的转化率为60%,则该温度下合成氨反应的平衡常数
的转化率为60%,则该温度下合成氨反应的平衡常数
_____ (最简分数即可)。
②按投料Ⅱ进行反应,起始时反应进行的方向为_____ (填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数_____ (填“变大”、“变小”或“不变”)。

(1)请写出工业合成氨的化学方程式
(2)请用平衡移动原理解释在流程中及时分离出氨气和循环使用气体的原因
(3)在合成氨工业中原料气(
 、
、 、及少量CO、
、及少量CO、 的混合气体)在进入合成塔之前需要经过铜氨液处理,目的是去除其中的CO,其反应为:
的混合气体)在进入合成塔之前需要经过铜氨液处理,目的是去除其中的CO,其反应为:

①铜氨液吸收CO适宜的生产条件是
②吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用,铜氨液。再生适宜的生产条件是
(4)模拟工业合成氨(
 ),在恒温恒容密闭容器中进行,起始投料时各物质浓度如下表:
),在恒温恒容密闭容器中进行,起始投料时各物质浓度如下表: |  |  | |
| 投料Ⅰ | 1.0mol/L | 3.0mol/L | 0 |
| 投料Ⅱ | 0.5mol/L | 1.5mol/L | 1.0mol/L |
 的转化率为60%,则该温度下合成氨反应的平衡常数
的转化率为60%,则该温度下合成氨反应的平衡常数
②按投料Ⅱ进行反应,起始时反应进行的方向为
③若升高温度,则合成氨反应的化学平衡常数
您最近一年使用:0次
名校
9 . 某研究性学习小组研究可逆反应:在容积为1.00 L恒容密闭容器中,通入一定量的 ,发生反应
,发生反应 ,请回答下列问题:
,请回答下列问题:
(1)反应一段时间,能说明该反应达到化学平衡状态的是_______(填字母)。
(2)达到化学平衡状态后,升高温度,混合气体的颜色变深,则该反应的
_______ (填“大于”或“小于”)0。
(3) ℃时,体系中各物质浓度随时间变化如下图所示。在0~60s时段,反应速率
℃时,体系中各物质浓度随时间变化如下图所示。在0~60s时段,反应速率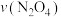 为
为_______ mol⋅L ⋅s
⋅s ,反应的平衡常数
,反应的平衡常数 为
为_______ 。

(4) ℃达到平衡后,改变反应温度为
℃达到平衡后,改变反应温度为 ,
, 以0.0020 mol⋅L
以0.0020 mol⋅L ⋅s
⋅s 的平均速率降低,经10s又达到平衡。
的平均速率降低,经10s又达到平衡。
①
_______ (填“大于”或“小于”) ,判断理由是
,判断理由是_______ 。
②计算温度 时反应的平衡常数
时反应的平衡常数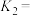
_______ 。
(5)将 球分别浸泡在甲、乙两个烧杯中,向甲中加入
球分别浸泡在甲、乙两个烧杯中,向甲中加入 晶体,此烧杯中
晶体,此烧杯中 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡 向
向_______ (填“正反应”或“逆反应”)方向移动,所以 晶体溶于水是
晶体溶于水是_______ (填“放热”或“吸热”)过程。

(6)将一定量的 充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。

①b点的操作是_______ 注射器(填“压缩”或“拉伸”)。
②c点与a点相比,
_______ ,
_______ (填“增大”或“减小”)。
③若不忽略体系温度变化,且没有能量损失,则温度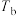
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 ,发生反应
,发生反应 ,请回答下列问题:
,请回答下列问题:(1)反应一段时间,能说明该反应达到化学平衡状态的是_______(填字母)。
A.单位时间内消耗n mol  ,同时生成2n mol ,同时生成2n mol  |
| B.容器内气体颜色保持不变 |
| C.容器内气体质量不随时间变化 |
| D.容器内气体的压强不随时间变化 |
(2)达到化学平衡状态后,升高温度,混合气体的颜色变深,则该反应的

(3)
 ℃时,体系中各物质浓度随时间变化如下图所示。在0~60s时段,反应速率
℃时,体系中各物质浓度随时间变化如下图所示。在0~60s时段,反应速率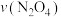 为
为 ⋅s
⋅s ,反应的平衡常数
,反应的平衡常数 为
为
(4)
 ℃达到平衡后,改变反应温度为
℃达到平衡后,改变反应温度为 ,
, 以0.0020 mol⋅L
以0.0020 mol⋅L ⋅s
⋅s 的平均速率降低,经10s又达到平衡。
的平均速率降低,经10s又达到平衡。①

 ,判断理由是
,判断理由是②计算温度
 时反应的平衡常数
时反应的平衡常数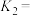
(5)将
 球分别浸泡在甲、乙两个烧杯中,向甲中加入
球分别浸泡在甲、乙两个烧杯中,向甲中加入 晶体,此烧杯中
晶体,此烧杯中 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡 向
向 晶体溶于水是
晶体溶于水是
(6)将一定量的
 充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
①b点的操作是
②c点与a点相比,


③若不忽略体系温度变化,且没有能量损失,则温度
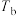
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
名校
10 . 碳单质在工业上有多种用途。
(1)焦炭可用于制取水煤气。测得 碳与水蒸气完全反应生成水煤气(主要成分为
碳与水蒸气完全反应生成水煤气(主要成分为 和
和 )时,吸收了
)时,吸收了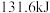 热量。该反应的热化学方程式是
热量。该反应的热化学方程式是___________ 。
(2)活性炭可处理大气污染物 。在
。在 密闭容器中加入
密闭容器中加入 和活性炭(无杂质),生成气体E和F。当温度分别在
和活性炭(无杂质),生成气体E和F。当温度分别在 和
和 时,测得各物质平衡时物质的量如下表:
时,测得各物质平衡时物质的量如下表:

①请结合上表数据,写出 与活性炭反应的化学方程式
与活性炭反应的化学方程式___________ 。
②上述反应 时的平衡常数为
时的平衡常数为 时的平衡常数为
时的平衡常数为 。
。
Ⅰ.计算
___________ 。
Ⅱ.根据上述信息判断,温度 和
和 的关系是(填序号)
的关系是(填序号)___________ 。
a. b.
b. c.无法比较
c.无法比较
③在T温度下反应达到平衡后,下列措施不能改变 的转化率的是
的转化率的是___________ 。
a.增大 b.增大压强 c.升高温度 d.移去部分F
b.增大压强 c.升高温度 d.移去部分F
(3)工业上可用焦炭冶炼金属。若 碳完全与赤铁矿(Fe2O3)反应,得到
碳完全与赤铁矿(Fe2O3)反应,得到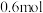 铁,同时生成2种常见气体,则该反应的化学方程式是
铁,同时生成2种常见气体,则该反应的化学方程式是___________ 。
(1)焦炭可用于制取水煤气。测得
 碳与水蒸气完全反应生成水煤气(主要成分为
碳与水蒸气完全反应生成水煤气(主要成分为 和
和 )时,吸收了
)时,吸收了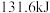 热量。该反应的热化学方程式是
热量。该反应的热化学方程式是(2)活性炭可处理大气污染物
 。在
。在 密闭容器中加入
密闭容器中加入 和活性炭(无杂质),生成气体E和F。当温度分别在
和活性炭(无杂质),生成气体E和F。当温度分别在 和
和 时,测得各物质平衡时物质的量如下表:
时,测得各物质平衡时物质的量如下表:
①请结合上表数据,写出
 与活性炭反应的化学方程式
与活性炭反应的化学方程式②上述反应
 时的平衡常数为
时的平衡常数为 时的平衡常数为
时的平衡常数为 。
。Ⅰ.计算

Ⅱ.根据上述信息判断,温度
 和
和 的关系是(填序号)
的关系是(填序号)a.
 b.
b. c.无法比较
c.无法比较③在T温度下反应达到平衡后,下列措施不能改变
 的转化率的是
的转化率的是a.增大
 b.增大压强 c.升高温度 d.移去部分F
b.增大压强 c.升高温度 d.移去部分F(3)工业上可用焦炭冶炼金属。若
 碳完全与赤铁矿(Fe2O3)反应,得到
碳完全与赤铁矿(Fe2O3)反应,得到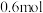 铁,同时生成2种常见气体,则该反应的化学方程式是
铁,同时生成2种常见气体,则该反应的化学方程式是
您最近一年使用:0次



