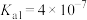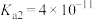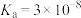1 . 生物质铁炭纳米材料可以活化过一硫酸盐,降解废水中有机污染物.
(1)生物质铁炭纳米材料活化过—硫酸钾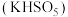 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中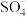 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基. (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: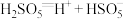 、
、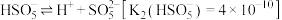 .写出
.写出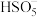 的结构式:
的结构式:_______ 。
②生物质铁炭纳米材料降解有机污染物的机理可描述为______ 。
③若有机污染物为苯酚,写出酸性条件下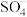 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:______ 。
(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:______ 。
(3)铁炭纳米材料在不同 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是:______ 。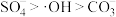 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是:______ 。
(1)生物质铁炭纳米材料活化过—硫酸钾
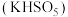 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中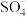 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基.
 (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: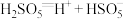 、
、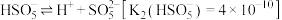 .写出
.写出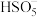 的结构式:
的结构式:②生物质铁炭纳米材料降解有机污染物的机理可描述为
③若有机污染物为苯酚,写出酸性条件下
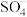 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:
(3)铁炭纳米材料在不同
 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是: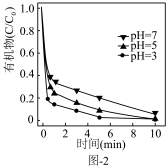
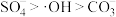 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是: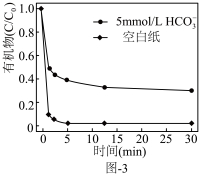
您最近一年使用:0次
2 . 现有常温下甲、乙、丙三种溶液,甲为0.1mol•L-1的NaOH溶液,乙为0.1mol•L-1的HCl溶液,丙为0.1mol•L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的c(H+)=______ ,pH=______ 。
(2)丙溶液中存在的两个电离平衡为______ (用电离平衡方程式表示)。
(3)常温下,用水稀释0.1mol•L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是______ (填序号)。
①n(H+) ②c(H+) ③ ④c(OH-)
④c(OH-)
(4)乙、丙两种溶液中水电离程度大小顺序为______ 。
(5)将等体积的甲、丙溶液混合,充分反应后,得到的溶液中离子浓度由大到小为______ ;溶液中电荷守恒______ (用粒子浓度形式表示)。
(1)甲溶液的c(H+)=
(2)丙溶液中存在的两个电离平衡为
(3)常温下,用水稀释0.1mol•L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是
①n(H+) ②c(H+) ③
 ④c(OH-)
④c(OH-)(4)乙、丙两种溶液中水电离程度大小顺序为
(5)将等体积的甲、丙溶液混合,充分反应后,得到的溶液中离子浓度由大到小为
您最近一年使用:0次
3 . 回答下列问题:
(1)某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,则AgCl的溶解度______ (填增大,减小或不变,下同),Ksp______ ,c(Ag+)______ 。
(2)现有25℃0.1mol/L的氨水。请回答以下问题:
①若向氨水中加入氯化铵固体,此时溶液中NH3•H2O电离程度_______ (填“增大”、“减小”或“不变”);此时溶液中水的离子积约等于_______ 。
②若向氨水中加入稀硫酸,使其恰好中和,写出离子方程式:______ 所得溶液的pH______ 7(填“>”“=”或“<”),用离子方程式表示其原因:______ 。
(1)某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,则AgCl的溶解度
(2)现有25℃0.1mol/L的氨水。请回答以下问题:
①若向氨水中加入氯化铵固体,此时溶液中NH3•H2O电离程度
②若向氨水中加入稀硫酸,使其恰好中和,写出离子方程式:
您最近一年使用:0次
名校
4 . 已知常温下部分弱电解质的电离平衡常数如下表所示:
(1)25℃时,pH=10的NaClO溶液中各离子浓度的大小关系为_______ (离子浓度如Na+的浓度以c(Na+)表示,下同)。向NaClO溶液中通入少量CO2,反应的离子方程式为_______ 。
(2)NH4Cl溶液中的电荷守恒关系式为_______ 。
(3)NH4F溶液显_______ (填酸性、碱性或中性)。
(4)物质的量浓度相同的NaNO2、NaClO两种溶液,pH较大的是_______ 。
(5)泡沫灭火器利用了硫酸铝溶液和碳酸氢钠溶液的反应,用离子方程式表示原理_______ 。
(6)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中 和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。_______ (填“A”或“B”)。
②当加入盐酸体积为50mL时,溶液中c( )∶c(NH3·H2O)=
)∶c(NH3·H2O)=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O | HNO2 |
| 电离常数 | 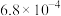 | 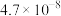 |  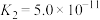 |  |  |
(1)25℃时,pH=10的NaClO溶液中各离子浓度的大小关系为
(2)NH4Cl溶液中的电荷守恒关系式为
(3)NH4F溶液显
(4)物质的量浓度相同的NaNO2、NaClO两种溶液,pH较大的是
(5)泡沫灭火器利用了硫酸铝溶液和碳酸氢钠溶液的反应,用离子方程式表示原理
(6)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中
 和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。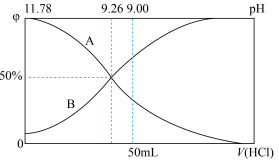
②当加入盐酸体积为50mL时,溶液中c(
 )∶c(NH3·H2O)=
)∶c(NH3·H2O)=
您最近一年使用:0次
5 . 25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)HCOOH、H2CO3、HCN的酸性由强到弱的顺序为___________ 。
(2)向Na2CO3溶液中加入足量HCN,反应的离子方程式为___________ 。
(3)写出HCOONa溶液中的电荷守恒式___________ 。
(4)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.00mol/L的NaOH标准溶液滴定:
①用NaOH固体配置100mL,1.00mol/L的NaOH溶液,需要用到的仪器除托盘天平,药匙,烧杯,玻璃棒,胶头滴管,还必须要___________ 。
②实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;NaOH溶液应装___________ 入(填“酸式滴定管”或“碱式滴定管”);滴定过程中,眼睛应注视___________ 。
③连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为___________ mL。
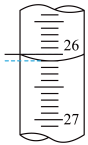
④某学生根据3次实验分别记录有关数据如下表:
依据上表数据计算该HCOOH溶液的物质的量浓度为___________ mol/L(计算结果保留到小数点后两位)。
⑤下列操作中可能使所测HCOOH溶液的浓度数值偏低的是___________ (填字母)。
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
| 化学式 | HCOOH | H2CO3 | HCN |
| 电离平衡常数 | 1.5×10-4 | Ka1=4.2×10-7 Ka2=4.9×10-11 | 3.0×10-8 |
(1)HCOOH、H2CO3、HCN的酸性由强到弱的顺序为
(2)向Na2CO3溶液中加入足量HCN,反应的离子方程式为
(3)写出HCOONa溶液中的电荷守恒式
(4)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.00mol/L的NaOH标准溶液滴定:
①用NaOH固体配置100mL,1.00mol/L的NaOH溶液,需要用到的仪器除托盘天平,药匙,烧杯,玻璃棒,胶头滴管,还必须要
②实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;NaOH溶液应装
③连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为

④某学生根据3次实验分别记录有关数据如下表:
| 实验序号 | 待测HCOOH溶液体积/mL | 1.00mol/LNaOH的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液的体积 | ||
| 1 | 25.00 | 0.00 | 12.49 | V1 |
| 2 | 25.00 | 0.56 | 14.56 | V2 |
| 3 | 25.00 | 0.22 | 12.73 | V3 |
⑤下列操作中可能使所测HCOOH溶液的浓度数值偏低的是
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
您最近一年使用:0次
6 . 回答下列问题
(1)现有a. b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
①相同物质的量浓度的两种酸溶液中,水的电离程度的大小关系为a_________ b。
②pH相同、体积相同的两种酸溶液中分别加入足量锌,相同状况下产生气体体积大小关系为a_________ b。
将体积相同、pH=2的醋酸和pH=2的盐酸分别与pH=12的氢氧化钠溶液等体积混合,反应后溶液的pH的大小关系为a_________ b。
(2)常温下,根据表中的几种物质的电离平衡常数回答下列问题:
①下列反应不能发生的是_________ (填序号)。
a.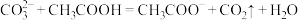
b.
c.
d.
②反应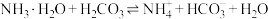 的平衡常数K=
的平衡常数K=_________ 。
(3)常温下,浓度均为0.1 的下列五种钠盐溶液的pH如下表:
的下列五种钠盐溶液的pH如下表:
①上述盐溶液中的阴离子,结合 能力最强的是
能力最强的是 _________ 。
②根据表中数据,浓度均为0.01 的下列四种酸的溶液分别稀释100倍,pH变化最大的是
的下列四种酸的溶液分别稀释100倍,pH变化最大的是_________ (填编号)。
A.HCN B.HClO C. D.
D.
(4)①已知t℃时,0.01 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中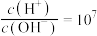 。该温度下,0.1
。该温度下,0.1 HA溶液中水电离出的
HA溶液中水电离出的
_________ 。
②25℃时,将体积 、pH=a的某一元强碱与体积为
、pH=a的某一元强碱与体积为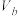 、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则
、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则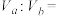
_________ 。
③25℃时,pH=5的醋酸和pH=5的 溶液中由水电离出的
溶液中由水电离出的 浓度之比为
浓度之比为_________ 。
(1)现有a.
 b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。①相同物质的量浓度的两种酸溶液中,水的电离程度的大小关系为a
②pH相同、体积相同的两种酸溶液中分别加入足量锌,相同状况下产生气体体积大小关系为a
将体积相同、pH=2的醋酸和pH=2的盐酸分别与pH=12的氢氧化钠溶液等体积混合,反应后溶液的pH的大小关系为a
(2)常温下,根据表中的几种物质的电离平衡常数回答下列问题:
弱酸 |
|
|
| HClO |
电离平衡常数 |
|
|
|
|
a.
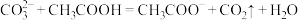
b.

c.

d.

②反应
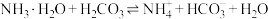 的平衡常数K=
的平衡常数K=(3)常温下,浓度均为0.1
 的下列五种钠盐溶液的pH如下表:
的下列五种钠盐溶液的pH如下表:溶质 |
|
|
| NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
 能力最强的是
能力最强的是 ②根据表中数据,浓度均为0.01
 的下列四种酸的溶液分别稀释100倍,pH变化最大的是
的下列四种酸的溶液分别稀释100倍,pH变化最大的是A.HCN B.HClO C.
 D.
D.
(4)①已知t℃时,0.01
 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中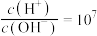 。该温度下,0.1
。该温度下,0.1 HA溶液中水电离出的
HA溶液中水电离出的
②25℃时,将体积
 、pH=a的某一元强碱与体积为
、pH=a的某一元强碱与体积为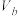 、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则
、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则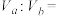
③25℃时,pH=5的醋酸和pH=5的
 溶液中由水电离出的
溶液中由水电离出的 浓度之比为
浓度之比为
您最近一年使用:0次
7 . 完成下列问题
(1)依据事实,写出下列反应的热化学方程式。
①1molCu(s)与适量 (g)反应生成CuO(s),放出157.3kJ的热量
(g)反应生成CuO(s),放出157.3kJ的热量___________ 。
②在载人航天器中,可以利用 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:
①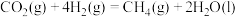
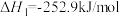
②

请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式___________ 。
(2)下列溶液,c(H+)由小到大的排列顺序是___________ ;pH由小到大的排列顺序是___________ 。
①0.1mol/LHCl溶液;②0.1mol/LH2SO4溶液;③0.1mol/LNaOH溶液;④0.1mol/LCH3COOH溶液
(1)依据事实,写出下列反应的热化学方程式。
①1molCu(s)与适量
 (g)反应生成CuO(s),放出157.3kJ的热量
(g)反应生成CuO(s),放出157.3kJ的热量②在载人航天器中,可以利用
 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:①
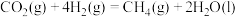
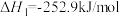
②


请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
(2)下列溶液,c(H+)由小到大的排列顺序是
①0.1mol/LHCl溶液;②0.1mol/LH2SO4溶液;③0.1mol/LNaOH溶液;④0.1mol/LCH3COOH溶液
您最近一年使用:0次
8 . 下表是几种常见弱酸的电离平衡常数(25℃),回答下列各题:
(1)可以证明醋酸是弱酸的事实是_____ (填字母序号)
A.醋酸和水能以任意比例混溶
B.在醋酸水溶液中还含有未电离的醋酸分子
C.醋酸与 溶液反应放出
溶液反应放出 气体
气体
D. 的醋酸水溶液能使紫色石蕊溶液变红色
的醋酸水溶液能使紫色石蕊溶液变红色
E.等体积等pH的醋酸和盐酸分别与足量氢氧化钠溶液充分反应,醋酸消耗的氢氧化钠更多
(2)结合表中给出的电离常数回答下列问题:
①上述四种酸中,最强的酸是_____ (用化学式表示)。
②下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的操作是
的电离程度增大,而电离平衡常数不变的操作是_____ 。
A.升高温度 B.加水稀释 C.加少量的 固体 D.加少量冰醋酸 E.加氢氧化钠固体
固体 D.加少量冰醋酸 E.加氢氧化钠固体
③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式_____ 。
(3)已知水溶液中 和
和 的关系如图所示:
的关系如图所示:
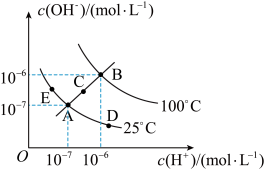
①图中A、B、C、D四点对应的水的离子积常数由大到小的顺序是_____ 。
②若A点到E点,可采用的措施是_____ (填序号,下同);促进水的电离平衡正向移动的措施是_____ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH
③室温下,在由水电离产生的 浓度为
浓度为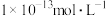 的溶液中,一定能大量共存的离子组是
的溶液中,一定能大量共存的离子组是_____ 。
a. 、
、 、
、 、
、 b.
b. 、
、 、
、 、
、
c. 、
、 、
、 、
、 d.
d. 、
、 、
、 、
、
e. 、
、 、
、 、
、
| 酸 |  |  | HCN | HClO |
电离平衡常数( ) ) |  |  | 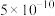 |  |
(1)可以证明醋酸是弱酸的事实是
A.醋酸和水能以任意比例混溶
B.在醋酸水溶液中还含有未电离的醋酸分子
C.醋酸与
 溶液反应放出
溶液反应放出 气体
气体D.
 的醋酸水溶液能使紫色石蕊溶液变红色
的醋酸水溶液能使紫色石蕊溶液变红色E.等体积等pH的醋酸和盐酸分别与足量氢氧化钠溶液充分反应,醋酸消耗的氢氧化钠更多
(2)结合表中给出的电离常数回答下列问题:
①上述四种酸中,最强的酸是
②下列能使醋酸溶液中
 的电离程度增大,而电离平衡常数不变的操作是
的电离程度增大,而电离平衡常数不变的操作是A.升高温度 B.加水稀释 C.加少量的
 固体 D.加少量冰醋酸 E.加氢氧化钠固体
固体 D.加少量冰醋酸 E.加氢氧化钠固体③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式
(3)已知水溶液中
 和
和 的关系如图所示:
的关系如图所示:
①图中A、B、C、D四点对应的水的离子积常数由大到小的顺序是
②若A点到E点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH
③室温下,在由水电离产生的
 浓度为
浓度为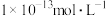 的溶液中,一定能大量共存的离子组是
的溶液中,一定能大量共存的离子组是a.
 、
、 、
、 、
、 b.
b. 、
、 、
、 、
、
c.
 、
、 、
、 、
、 d.
d. 、
、 、
、 、
、
e.
 、
、 、
、 、
、
您最近一年使用:0次
名校
解题方法
9 . 已知如下四种物质① ②
② ③NaOH④
③NaOH④
1.写出①的电离方程式_____ 。
2.向②的溶液中滴加几滴浓盐酸,平衡_____ 移动(填“正向”、“逆向”或“不移动”),平衡时溶液中
_____ (填“增大”、“减小”或者“不变”),
_____ (填“增大”、“减小”或者“不变”)。
3.将 的①溶液和
的①溶液和 的③溶液等体积混合后得到的溶液中主要溶质是
的③溶液等体积混合后得到的溶液中主要溶质是_____ (填化学式),该溶液显酸性,原因是_____ (请用文字结合该溶液中两个相关平衡方程式加以说明)。
4.将标准状况下2.24L④缓慢通入 的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为
的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为_____ ,该溶液中各离子浓度大小关系_____ 。
5.将足量④缓慢通入 的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度_____ 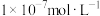 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH_____ (填“增大”、“减小”、或“不变”)。
 ②
② ③NaOH④
③NaOH④
1.写出①的电离方程式
2.向②的溶液中滴加几滴浓盐酸,平衡


3.将
 的①溶液和
的①溶液和 的③溶液等体积混合后得到的溶液中主要溶质是
的③溶液等体积混合后得到的溶液中主要溶质是4.将标准状况下2.24L④缓慢通入
 的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为
的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为5.将足量④缓慢通入
 的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度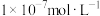 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH
您最近一年使用:0次
名校
10 . 25℃时部分弱酸的电离平衡常数如下表:
1.室温下① ②
② ③
③ ④
④ ,溶液的pH由大到小的关系为(填序号)
,溶液的pH由大到小的关系为(填序号)_____ 。
2.下列离子方程式书写正确的是
| 弱酸 |  |  |  |  |
| 电离平衡常数 |  |  |   |   |
 ②
② ③
③ ④
④ ,溶液的pH由大到小的关系为(填序号)
,溶液的pH由大到小的关系为(填序号)2.下列离子方程式书写正确的是
A.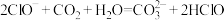 |
B. |
C. |
D. |
您最近一年使用:0次