1 . 乙二酸(HOOC-COOH)俗名为草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。回答下列问题:
(1)在恒温恒容密闭容器中发生反应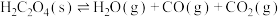 。下列描述能说明反应已达到平衡状态的是
。下列描述能说明反应已达到平衡状态的是___________ (填字母)。
A.压强不再变化
B. (g)的体积分数保持不变
(g)的体积分数保持不变
C.混合气体密度不再变化
(2)草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示。 的
的 溶液的pH=1.3,此时草酸的电离方程式为
溶液的pH=1.3,此时草酸的电离方程式为___________ 。
②向10mL 0.1
 溶液中逐滴加入0.1
溶液中逐滴加入0.1 的NaOH溶液,当溶液中
的NaOH溶液,当溶液中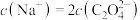
 时,加入的V(NaOH)
时,加入的V(NaOH)___________ (填“>”、“=”或“<”)10mL。若加入NaOH溶液的体积为20mL,此时溶液中阴离子浓度由大到小的顺序为___________ ;当pH=2.7时,溶液中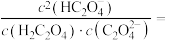
___________ 。
(1)在恒温恒容密闭容器中发生反应
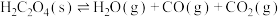 。下列描述能说明反应已达到平衡状态的是
。下列描述能说明反应已达到平衡状态的是A.压强不再变化
B.
 (g)的体积分数保持不变
(g)的体积分数保持不变C.混合气体密度不再变化
(2)草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示。
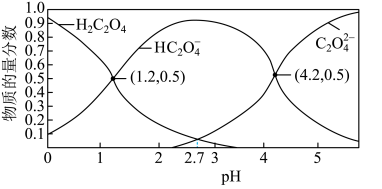
 的
的 溶液的pH=1.3,此时草酸的电离方程式为
溶液的pH=1.3,此时草酸的电离方程式为②向10mL 0.1

 溶液中逐滴加入0.1
溶液中逐滴加入0.1 的NaOH溶液,当溶液中
的NaOH溶液,当溶液中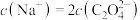
 时,加入的V(NaOH)
时,加入的V(NaOH)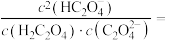
您最近一年使用:0次
解题方法
2 . 草酸 是一种白色粉末,
是一种白色粉末,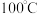 左右开始少量升华,熔点为
左右开始少量升华,熔点为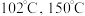 左右分解产生
左右分解产生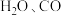 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为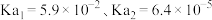 。
。
1.草酸可用于实验室制备少量 气体,应选择的发生装置为
气体,应选择的发生装置为___________ 。
常温下,向某浓度的草酸溶液中加入一定量等浓度的 溶液。
溶液。
3.当 时,溶液呈___________。
时,溶液呈___________。
A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中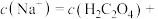
___________ 。
4.当 时,计算该溶液的
时,计算该溶液的
___________ 。(结果保留两位小数)计算过程。
 是一种白色粉末,
是一种白色粉末,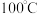 左右开始少量升华,熔点为
左右开始少量升华,熔点为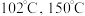 左右分解产生
左右分解产生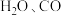 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为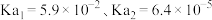 。
。1.草酸可用于实验室制备少量
 气体,应选择的发生装置为
气体,应选择的发生装置为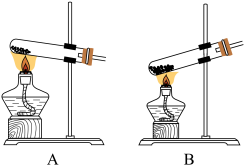
A.用足量的 溶液充分吸收后,可收集得到纯净的 溶液充分吸收后,可收集得到纯净的 |
| B.通过灼热的氧化铜,若出现黑色变红色现象,则产生的气体中一定有CO |
C.通入足量的澄清石灰水中,若能产生白色沉淀,则产生的气体中一定有 |
D.通入酸性 溶液中,若能使溶液褪色,说明草酸具有还原性 溶液中,若能使溶液褪色,说明草酸具有还原性 |
常温下,向某浓度的草酸溶液中加入一定量等浓度的
 溶液。
溶液。3.当
 时,溶液呈___________。
时,溶液呈___________。A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中
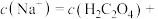
4.当
 时,计算该溶液的
时,计算该溶液的
您最近一年使用:0次
解题方法
3 . 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从①组情况分析,HA是___________ (填“强酸”或“弱酸”)。
(2)②组情况表明,c___________ (填“大于”、“小于”或“等于”)0.2mol/L。混合液中离子浓度c(A-)与c(Na+)的大小关系是:c(A-)___________ c(Na+) (“大于”、“小于”或“等于”)。
(3)从③组实验结果分析,说明HA的电离程度___________ (填“大于”、“小于”或“等于”)NaA的水解程度。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=___________ mol∙L-1。
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的 pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是
(2)②组情况表明,c
(3)从③组实验结果分析,说明HA的电离程度
(4)①组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
4 . 水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:
①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ ,不发生移动的是___________ 。(用序号填空)
(2)溶液呈酸性的是___________ ,溶液呈碱性的是___________ 。(用序号填空)
(3)能促进水的电离,且溶液pH>7的是___________ 。(用序号填空)
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=___________ ,温度升高,Ka将___________ (填“变大”、“不变”或“变小”)。
(5)向 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是___________ ,若微热溶液,观察到的现象是___________ ,由此证明碳酸钠的水解是___________ (填“吸热”或“放热”)反应。 溶液中
溶液中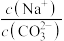
___________ 2(填“大于”或“小于”),能使其比值接近2的措施是___________ (填序号)。
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
 H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=
(5)向
 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是 溶液中
溶液中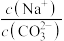
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
您最近一年使用:0次
名校
5 . 磷能形成次磷酸 、亚磷酸
、亚磷酸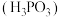 、磷酸
、磷酸 等多种含氧酸,完成下列问题。
等多种含氧酸,完成下列问题。
(1)①已知 是一元弱酸,书写
是一元弱酸,书写 的电离方程式:
的电离方程式:_______ 。
②以下可以证明 是弱酸的是
是弱酸的是_______ 。
A. 溶液与碳酸钙反应,缓慢放出二氧化碳
溶液与碳酸钙反应,缓慢放出二氧化碳
B. 溶液导电能力很弱
溶液导电能力很弱
C.常温时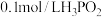 溶液的
溶液的 大于1
大于1
D. 溶液可以使石蕊变红
溶液可以使石蕊变红
(2)亚磷酸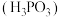 是二元弱酸,
是二元弱酸, 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(3)磷酸 是三元弱酸,
是三元弱酸, 溶液中含磷酸根浓度由大到小排第二位的微粒符号是
溶液中含磷酸根浓度由大到小排第二位的微粒符号是_______ 。
 、亚磷酸
、亚磷酸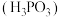 、磷酸
、磷酸 等多种含氧酸,完成下列问题。
等多种含氧酸,完成下列问题。(1)①已知
 是一元弱酸,书写
是一元弱酸,书写 的电离方程式:
的电离方程式:②以下可以证明
 是弱酸的是
是弱酸的是A.
 溶液与碳酸钙反应,缓慢放出二氧化碳
溶液与碳酸钙反应,缓慢放出二氧化碳 B.
 溶液导电能力很弱
溶液导电能力很弱C.常温时
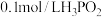 溶液的
溶液的 大于1
大于1 D.
 溶液可以使石蕊变红
溶液可以使石蕊变红(2)亚磷酸
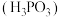 是二元弱酸,
是二元弱酸, 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(3)磷酸
 是三元弱酸,
是三元弱酸, 溶液中含磷酸根浓度由大到小排第二位的微粒符号是
溶液中含磷酸根浓度由大到小排第二位的微粒符号是
您最近一年使用:0次
名校
6 . 向0.1mol∙L-1FeSO4溶液中持续通入H2S至饱和,有微量黑色的FeS沉淀生成,该溶液中[H2S]=0.1mol∙L-1。(忽略FeSO4浓度的变化和溶液体积的变化)。已知常温下,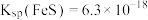 ,H2S的电离常数分别为:
,H2S的电离常数分别为: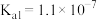 、
、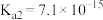 。
。
(1)写出生成黑色沉淀的离子方程式___________ 。
(2)溶液中[S2-]=___________ mol∙L-1;溶液中[H+]=___________ mol∙L-1。
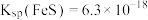 ,H2S的电离常数分别为:
,H2S的电离常数分别为: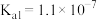 、
、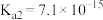 。
。(1)写出生成黑色沉淀的离子方程式
(2)溶液中[S2-]=
您最近一年使用:0次
名校
7 . 已知 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
1.物质的量浓度均为 的下列四种溶液:
的下列四种溶液: 最大是___________。
最大是___________。
2.标准状况下将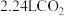 ,通入
,通入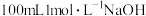 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
___________ 。
 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 |  |  |  |
| 电离平衡常数 |  | 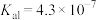  |  |
 的下列四种溶液:
的下列四种溶液: 最大是___________。
最大是___________。A. | B. | C. | D. |
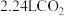 ,通入
,通入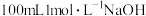 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
您最近一年使用:0次
名校
8 . 电解质的水溶液跟日常生活、工农业生产和环境保护息息相关.
(1)电解质在水中会发生电离,酸、碱在溶液中能发生中和反应.
①常温下, 的氢氧化钠溶液中由水电离出的
的氢氧化钠溶液中由水电离出的 的浓度为
的浓度为___________  .
.
②常温下, 的醋酸溶液与
的醋酸溶液与 的氢氧化钠溶液反应的离子方程式为:
的氢氧化钠溶液反应的离子方程式为:___________
③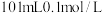 的盐酸和
的盐酸和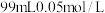 的
的 溶液混合后,
溶液混合后,
___________ .
(2)有浓度为 的盐酸、硫酸、醋酸三种溶液,试回答:
的盐酸、硫酸、醋酸三种溶液,试回答:
①中和一定量 溶液生成正盐时,需上述三种酸的体积依次是
溶液生成正盐时,需上述三种酸的体积依次是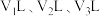 ,则
,则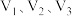 的关系为
的关系为
___________ =___________ .
②与锌反应时产生氢气的速率分别为 ,其由大到小关系为
,其由大到小关系为___________ .
(3) 时,有
时,有 的醋酸溶液,试回答:
的醋酸溶液,试回答:
达平衡时,溶液中氢离子浓度为___________  (
( 时,醋酸的电离平衡常数为
时,醋酸的电离平衡常数为 ).
).
(1)电解质在水中会发生电离,酸、碱在溶液中能发生中和反应.
①常温下,
 的氢氧化钠溶液中由水电离出的
的氢氧化钠溶液中由水电离出的 的浓度为
的浓度为 .
.②常温下,
 的醋酸溶液与
的醋酸溶液与 的氢氧化钠溶液反应的离子方程式为:
的氢氧化钠溶液反应的离子方程式为:③
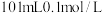 的盐酸和
的盐酸和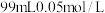 的
的 溶液混合后,
溶液混合后,
(2)有浓度为
 的盐酸、硫酸、醋酸三种溶液,试回答:
的盐酸、硫酸、醋酸三种溶液,试回答:①中和一定量
 溶液生成正盐时,需上述三种酸的体积依次是
溶液生成正盐时,需上述三种酸的体积依次是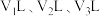 ,则
,则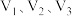 的关系为
的关系为
②与锌反应时产生氢气的速率分别为
 ,其由大到小关系为
,其由大到小关系为(3)
 时,有
时,有 的醋酸溶液,试回答:
的醋酸溶液,试回答:达平衡时,溶液中氢离子浓度为
 (
( 时,醋酸的电离平衡常数为
时,醋酸的电离平衡常数为 ).
).
您最近一年使用:0次
2024高三下·全国·专题练习
9 . 已知Ka(Kb)、Kw、Kh、Ksp分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据:Kw=1.0×10-14,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13,Ka(HF)=4.0×10-4,Ksp[Mg(OH)2]=1.8×10-11。
(1)为探究Mg(OH)2在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH)2(s)+2CH3COOH(aq) Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=___________ ,并据此推断Mg(OH)2___________ (填“能”或“不能”)溶解于醋酸(已知1.83≈5.8)。
(1)为探究Mg(OH)2在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH)2(s)+2CH3COOH(aq)
 Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
您最近一年使用:0次
2024高三下·全国·专题练习
10 . 硫及其化合物在日常生活、工业生产中都非常普遍。
(1)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++ ,
,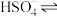 H++
H++ 。
。
①25℃时,Na2SO4溶液的pH___________ (填“>”“<”或“=”)7。
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数___________ (写出计算过程,结果保留三位有效数字)。
(2)液态水中,水存在自偶电离:H2O+H2O H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为___________ 。
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是___________ 。若保持温度不变,关于该所得溶液,下列说法正确的是___________ 。
A.加入少量冰醋酸,c( )与c(
)与c( )均减小
)均减小
B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c( )与c(
)与c( )的比值减小
)的比值减小
D.加入少量Na2SO4固体,c(Ac-)减小
(1)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++
 ,
,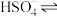 H++
H++ 。
。①25℃时,Na2SO4溶液的pH
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数
(2)液态水中,水存在自偶电离:H2O+H2O
 H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是
A.加入少量冰醋酸,c(
 )与c(
)与c( )均减小
)均减小B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c(
 )与c(
)与c( )的比值减小
)的比值减小D.加入少量Na2SO4固体,c(Ac-)减小
您最近一年使用:0次



