名校
解题方法
1 . 常温下,磷酸钠溶液中含磷微粒的分布随pH的变化如图所示,M、N、P三点对应的pH分别为a、b、c,其中δ表示含磷微粒的物质的量分数。下列说法错误的是
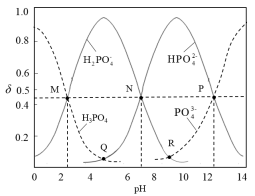

A.常温下, 的一级电离平衡常数Ka1=10-a 的一级电离平衡常数Ka1=10-a |
B.常温下,溶液中水电离出的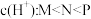 |
C.Q点与R点对应溶液的pH差: |
D.用磷酸标准溶液滴定NaOH溶液,选择酚酞作指示剂,终点时溶质主要为 |
您最近一年使用:0次
2021-02-03更新
|
1094次组卷
|
7卷引用:专题18 酸碱混合图像为载体考查离子平衡-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
(已下线)专题18 酸碱混合图像为载体考查离子平衡-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(练)河南省新乡市2020-2021学年高二上学期期末考试化学试题湖北省仙桃中学、天门中学(B班)2021-2022学年高二上学期期中考试化学试题江西省宜春市铜鼓中学2021-2022学年高二下学期第一次月考(实验班)化学试卷湖南省衡阳市第八中学2022-2023学年高二下学期5月月考化学试题
2 . 某二元酸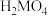 在水中分两步电离:
在水中分两步电离: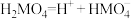 ,
, 。常温下,向20 mL
。常温下,向20 mL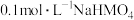 溶液中滴入
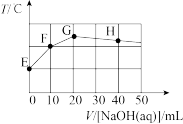
溶液中滴入 溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确的是
溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确的是
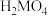 在水中分两步电离:
在水中分两步电离: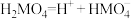 ,
, 。常温下,向20 mL
。常温下,向20 mL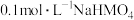 溶液中滴入
溶液中滴入 溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确的是
溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确的是
| A.该NaOH溶液pH=13 |
| B.从G点到H点水的电离平衡正向移动 |
C.图象中E点对应的溶液中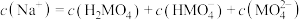 |
D.若F点对应的溶液pH=2,则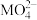 的水解平衡常数约为 的水解平衡常数约为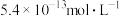 |
您最近一年使用:0次
2021-01-23更新
|
591次组卷
|
6卷引用:解密10 水溶液中离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练
(已下线)解密10 水溶液中离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)山东省烟台市2021届高三上学期期末考试化学试题安徽省滁州市明光中学2020-2021学年高二下学期开学考试化学试题山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题山东省滕州市第二中学2022-2023学年高三上学期11月定时检测化学试题
3 . 25℃时,体积均为100mL、浓度均为的两种一元碱MOH和ROH的溶液中,分别通入HCl气体, 随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的变化)( )
随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的变化)( )
 随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的变化)( )
随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的变化)( )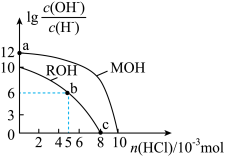
| A.MOH是强碱,ROH是弱碱 |
| B.a点由水电离产生的c(H+)和c(OH-)的乘积为1×10-26 |
| C.b点溶液中:c(Cl-)>c(R+)>c(H+)>c(OH-) |
| D.c点溶液的pH=7,且所含溶质为ROH和RCl |
您最近一年使用:0次
2020-05-19更新
|
186次组卷
|
5卷引用:第26讲 水的电离和溶液的pH (精讲)-2021年高考化学一轮复习讲练测
第26讲 水的电离和溶液的pH (精讲)-2021年高考化学一轮复习讲练测(已下线)第22讲 水的电离与溶液的pH(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)【校级联考】湖北省七市州教科研协作体2019届高三下学期三月联合考试理科综合化学试题天津市红桥区2020届高三下学期居家学习线上检测第一次模拟化学试题
名校
解题方法
4 . 常温下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1盐酸,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加盐酸体积的关系如图所示,下列说法正确的是( )

| A.常温下,Kb(NH3·H2O)约为1×10-3 |
| B.b=20.00 |
| C.R、Q两点对应溶液均呈中性 |
| D.R到N、N到Q所加盐酸体积相等 |
您最近一年使用:0次
2020-01-04更新
|
578次组卷
|
4卷引用:2020届高三《新题速递·化学》1月第02期(考点07-10)
真题
名校
5 . 实验测得0.5 mol·L−1CH3COONa溶液、0.5 mol·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
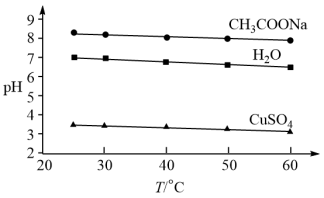

| A.随温度升高,纯水中c(H+)>c(OH−) |
| B.随温度升高,CH3COONa溶液的c(OH−)减小 |
| C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果 |
| D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同 |
您最近一年使用:0次
2019-06-09更新
|
10469次组卷
|
77卷引用:专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编
(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编(已下线)专题8.3 盐类水解(讲)-《2020年高考一轮复习讲练测》(已下线)专题8.3 盐类水解(练)-《2020年高考一轮复习讲练测》2020届高考化学小题狂练(全国通用版)专练16 盐类的水解(已下线)考点14 化学基本理论——《备战2020年高考精选考点专项突破题集》专题2.3 水溶液中的离子平衡(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)易错16 盐类水解规律及应用-备战2021年高考化学一轮复习易错题(已下线)第27讲 盐类水解 (精练)-2021年高考化学一轮复习讲练测(已下线)第27讲 盐类水解(精讲)——2021年高考化学一轮复习讲练测(已下线)小题必刷32 盐类的水解影响因素及应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时42 盐类的水解影响因素及应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题3.3.2 影响盐类水解的主要因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)第23讲 盐类水解(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第23讲 盐类水解(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向25 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点微专题(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)第3讲 盐类的水解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)第三单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第23讲 盐类水解 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(11-16)(已下线)题型136 盐类水解平衡及影响因素(已下线)专题16 水溶液中的离子平衡(已下线)T12-电解质溶液(已下线)第4讲 盐类的水解2019年北京高考化学试题山东省实验中学东校区2020届高三10月阶段性检测化学试题上海交通大学附中2019-2020学年高三上学期期中考试化学试题黑龙江省哈尔滨市第六中学2020届高三上学期第三次调研考试化学试题江西省赣州市宁师中学2020届高三12月月考化学试题西藏自治区拉萨市那曲第二高级中学2020届高三全真模拟联考理综化学试题云南省昆明市官渡区第一中学2020届高三上学期开学考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3章 综合检测高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测(已下线)3.3.2+影响盐类水解的主要因素和盐类水解的应用-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 高考帮北京五中2021届高三上学期第二次月考化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关广东省广州市广大附中、广外2020-2021学年高二上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP409】【化学】(已下线)【浙江新东方】99辽宁省大连市普兰店区第三十八中学2021届高三上学期第四次考试化学试题(已下线)第03章 水溶液中的离子反应与平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)安徽省池州市第一中学2020-2021学年高二12月月考化学试题浙江省杭州市西湖高级中学2020-2021学年高二上学期期末考试化学试题浙江省舟山中学2020-2021学年高三上学期10月月考化学试题选择性必修1(SJ)专题3专题培优专练甘肃省嘉峪关市第一中学2020-2021学年高二下学期期中考试化学试题北京朝阳市陈经纶中学2021-2022学年高三上学期10月月考化学试题辽宁省大连市2021-2022学年高二上学期期中考试化学试题吉林省长春市第二十九中学2022届高三上学期第二次质量检测化学试题(已下线)3.3.2 影响盐类水解的主要因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)第三章 综合拔高练云南省玉溪市江川区第二中学2021-2022学年高二上学期12月考试化学试题北京师范大学附属中学2020-2021学年高二上学期期中考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期中考试化学试题首都师范大学附属中学2022-2023高二上学期期中练习化学试题上海市吴淞中学2022-2023学年高三上学期期中考试化学试题北京市第四十三中学2021-2022学年高三上学期期中考试化学试题广西钦州市第四中学2022-2023学年高二上学期11月考试化学试题 四川省内江市第六中学2022-2023学年高二下学期第一次月考化学试题河南省南阳市2022-2023学年高二下学期期末考试化学试题北京市第一○一中学2023-2024学年高二上学期期中练习化学试题【精品卷】3.3.2 影响盐类水解的主要因素课堂例题-人教版2023-2024学年选择性必修1北京市第十四中学2023-2024学年高三上学期期中考试化学试题 北京市第八中学2022-2023学年高二上学期期中考试化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(三)化学试题江西省宜春市丰城市第九中学2023-2024学年高一下学期第一次月考化学试题(日新班)上海市洋泾中学2023-2024学年高二下学期5月月考-化学试卷
6 . 关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
A.c(NH ):③>① ):③>① |
| B.水电离出的c(H+):②>① |
C.①和②等体积混合后的溶液:c(H+)=c(OH )+c(NH3·H2O) )+c(NH3·H2O) |
D.①和③等体积混合后的溶液:c(NH )>c(Cl )>c(Cl )>c(OH )>c(OH )>c(H+) )>c(H+) |
您最近一年使用:0次
2019-01-30更新
|
1654次组卷
|
35卷引用:专题3 溶液中的离子反应 综合评价(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
(已下线)专题3 溶液中的离子反应 综合评价(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)2009年普通高等学校招生统一考试理综试题化学部分(四川卷)(已下线)2010-2011学年内蒙古赤峰二中高二上学期期末考试化学试卷(已下线)2011届陕西省西安中学高三第十三次模拟考试(理综)化学试题(已下线)2011-2012学年广西桂林十八中高二上学期期中考试化学(理)试卷(已下线)2012-2013学年陕西省宝鸡中学高二第一次月考化学试卷(已下线)2013-2014学年浙江省湖州市高二上学期期末考试化学试卷(已下线)2013-2014四川省雅安中学高二4月月考化学试卷2014-2015黑龙江省绥化市三校高二上学期期末联考化学试卷2014-2015吉林省长春外国语学校高二上学期期末化学试卷2015届山东省邹城市第一中学高三4月高考模拟理综化学试卷2015-2016学年山西省祁县中学高二上期中考试化学试卷2016届河北省冀州中学高三上学期第四次月考化学试卷2015-2016学年内蒙古杭锦后旗奋斗中学高二下期末考化学黑龙江省牡丹江市第一高级中学2017-2018学年高二上学期期中考试化学(理)试题河南省安阳市第三十六中学2017-2018学年高二上学期期中考试化学试题广东省深圳高中联考联盟2017-2018学年高二上学期期末考试化学试题【全国百强校】贵州省思南中学2018-2019学年高二上学期第二次月考化学试题【市级联考】吉林省公主岭市2018-2019学年高二上学期期末考试化学试题四川省遂宁二中2020届高三上学期第二次月考化学试题福建省莆田第一中学2018-2019学年高二下学期期初考试化学试题上海市复旦中学2019-2020学年高二上学期第一次月考化学试题山西省长治市第二中学2019-2020学年高二上学期期中考试化学试题陕西省西安中学2019-2020学年高二12月月考化学试题陕西省黄陵中学高新部2019-2020学年高二上学期期末考试化学试题2020年春季人教版高中化学选修4第三章《水溶液中的离子平衡》测试卷云南省曲靖市罗平县第三中学2019-2020学年高二上学期期末考试化学试题四川省遂宁市第二中学校2017-2018学年高二下学期期中考试化学试题新疆哈密市第十五中学2019-2020学年高二下学期期中考试化学试题黑龙江省伊春市伊美区第二中学2019-2020学年高二上学期期末考试化学试题宁夏贺兰县景博中学2020-2021学年高二上学期第二次月考化学试题河南省南阳市第一中学校2021-2022学年高二上学期第三次月考化学试题四川省内江市第三中学2021-2022学年高二下学期期中考试化学试题山东省青岛第六十八中学2023-2024学年高二上学期期中考试化学试卷西省西安市铁一中学2023-2024学年高二上学期期中质量检测化学试题
名校
7 . 今年春天以来,内蒙古自治区降水较常年偏少、气温偏高。进入7月以后,全区过半地域最高温度超过30℃以上,中西部地区有17个站点,最高温度超过35℃,阿拉善盟极高温度达到40℃。旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是______________________ 。
(2)在由水电离产生的c(H+)=1×10-14molL-1的溶液中①NH4+、A13+、Br-、SO42-;②Na+、Mg2+、Cl-、NO3-;③K+、Ba2+、Cl-、NO3-;④K+、 Na+、HCO3-、SO42-四组离子中。一定可以大量共存的是______ (填序号,下同),可能大量共存的是_____________ 。
(3)在下列中,水既不作氧化剂又不作还原剂是_____________ (填序号)。
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O==4NaOH+O2↑
C.CaH2+2H2O==Ca(OH)2+2H2↑ D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(4)将钠、钾分别投入有少量相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为_____________ 。
(5)三氟化氮(NF3)是一种无色无味的气体,27.0mL NF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:_________________ 。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是
(2)在由水电离产生的c(H+)=1×10-14molL-1的溶液中①NH4+、A13+、Br-、SO42-;②Na+、Mg2+、Cl-、NO3-;③K+、Ba2+、Cl-、NO3-;④K+、 Na+、HCO3-、SO42-四组离子中。一定可以大量共存的是
(3)在下列中,水既不作氧化剂又不作还原剂是
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O==4NaOH+O2↑
C.CaH2+2H2O==Ca(OH)2+2H2↑ D.3Fe+4H2O
 Fe3O4+4H2
Fe3O4+4H2(4)将钠、钾分别投入有少量相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为
(5)三氟化氮(NF3)是一种无色无味的气体,27.0mL NF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:
您最近一年使用:0次
2014高三·全国·专题练习
解题方法
8 . 下表是不同温度下水的离子积常数:
试回答以下问题:
(1)若25℃<T1<T2,则a__________ 1×10-14(填“>”、“<”或“=”),做此判断的理由是______________________________________ 。
(2)25℃时,某Na2SO4溶液中c(SO42—)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=__________ 。
(3)T2℃时,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=__________ 。此溶液中各种离子的浓度由大到小的顺序是____________________________ 。
(4)常温下,设某pH值的硫酸中水电离出的c(H+)=1.0×10-amol/L,设相同pH值的硫酸铝中水电离出的c(H+)=1.0×10-bmol/L,(a、b都是小于14的正数),那么a、b之间满足的关系式是________________ 。
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
试回答以下问题:
(1)若25℃<T1<T2,则a
(2)25℃时,某Na2SO4溶液中c(SO42—)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
(3)T2℃时,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=
(4)常温下,设某pH值的硫酸中水电离出的c(H+)=1.0×10-amol/L,设相同pH值的硫酸铝中水电离出的c(H+)=1.0×10-bmol/L,(a、b都是小于14的正数),那么a、b之间满足的关系式是
您最近一年使用:0次



