解题方法
1 . 已知水在25℃和95℃时,其电离平衡曲线如图所示:
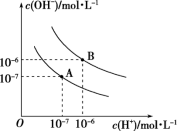
(1)则25℃时水的电离平衡曲线应为_______ (填“A”或“B”),请说明理由:_______ 。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为_______ 。
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_______ 。
(4)95℃时,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
假设溶液混合前后的体积不变,则a=_______ ,实验②所得溶液中由水电离产生的c(OH-)=_______ mol·L-1。
(5)95℃时,将0.1mol·L-1的NaHSO4溶液与0.1mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
①按丁方式混合后,所得溶液显_______ (填“酸”“碱”或“中”)性。
②写出按乙方式混合后,反应的化学方程式:_______ ,所得溶液显_______ (填“酸”“碱”或“中”)性。
③按甲方式混合,所得溶液的pH为_______ (混合时,忽略溶液体积的变化)。
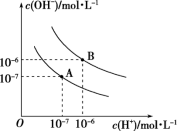
(1)则25℃时水的电离平衡曲线应为
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
(4)95℃时,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
| 实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积不变,则a=
(5)95℃时,将0.1mol·L-1的NaHSO4溶液与0.1mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
| 甲 | 乙 | 丙 | 丁 | |
| 0.1mol·L-1Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
| 0.1mol·L-1NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显
②写出按乙方式混合后,反应的化学方程式:
③按甲方式混合,所得溶液的pH为
您最近一年使用:0次
名校
解题方法
2 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1mol•L-1的(NH4)2SO4溶液中:Na+、Cu2+、Cl-、OH- |
B. =10-12的溶液中:Na+、NO =10-12的溶液中:Na+、NO 、[Al(OH)4]-、CO 、[Al(OH)4]-、CO |
C.水电离的c(H+)=1×10-13mol•L-1溶液中:Na+、K+、NO 、HCO 、HCO |
D.0.1mol•L-1的FeCl3溶液中:K+、Mg2+、SO 、SCN- 、SCN- |
您最近一年使用:0次
解题方法
3 . 室温下,向10mL0.1mol·L-1HA溶液中滴加0.1mol·L-1的NaOH溶液,溶液的酸度(AG)与NaOH溶液体积的关系如图所示。已知:AG=lg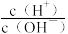 。
。
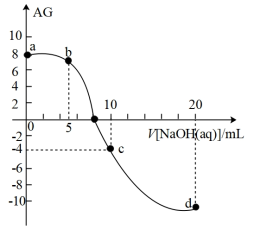
下列说法错误的是
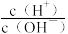 。
。
下列说法错误的是
| A.在a、b、c、d点对应的溶液中,c点时水的电离程度最大 |
| B.b点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-) |
| C.d点对应的溶液中:c(OH-)=c(H+)+c(HA)+c(A-) |
| D.室温下,HA的电离常数Ka约为1.0×10-4 |
您最近一年使用:0次
2022-04-30更新
|
353次组卷
|
3卷引用:河北省保定市部分学校2021-2022学年高三上学期期中考试化学试题
河北省保定市部分学校2021-2022学年高三上学期期中考试化学试题广东省韶关市2021-2022学年高三上学期期中考试化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)
2016·山东临沂·一模
名校
解题方法
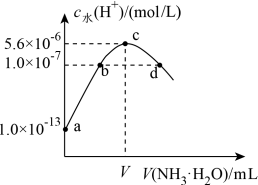
4 . 常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol·L-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析正确的是

| A.V=40 |
| B.c点所示溶液中:c(H+)-c(OH-)=2c(NH3·H2O) |
| C.NH3·H2O的电离常数K=10-4 |
D.d点所示溶液中:c(NH )=2c(SO )=2c(SO ) ) |
您最近一年使用:0次
2022-01-21更新
|
535次组卷
|
16卷引用:解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练
(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)2016届山东省临沂市高三下学期教学质检一模化学试卷2015-2016学年福建省厦门市海沧中学高二下学期期末化学试卷2016-2017学年辽宁省沈阳铁路中学高二上第一次月考化学试卷江西省景德镇市第一中学2016-2017学年高二(素质班)下学期期末考试化学试题【全国百强校】山西省长治市第二中学2018-2019学年高二上学期第二次月考(期中)化学试题百所名校联考-水溶液中的离子平衡夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解中三大守恒的应用2020届高三化学选修4二轮专题练——混合溶液中微粒浓度大小的比较专题【精编23题】江西省南昌市南昌县莲塘第三中学2020-2021学年高二上学期第二次月考化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练新疆乌鲁木齐市第七十中学2022-2023学年高二上学期期中考试化学试题
名校
5 . 常温下,用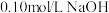 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的
的 溶液和
溶液和 溶液,滴定曲线如图。下列说法正确的是
溶液,滴定曲线如图。下列说法正确的是

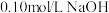 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的
的 溶液和
溶液和 溶液,滴定曲线如图。下列说法正确的是
溶液,滴定曲线如图。下列说法正确的是
A.电离平衡常数: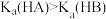 |
| B.水的电离程度:④>①>③>② |
C.点①和点②所示溶液中: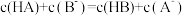 |
D.点③和点④所示溶液中均有: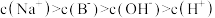 |
您最近一年使用:0次
2021-12-06更新
|
1437次组卷
|
6卷引用:重庆市高2022届高三第四次质量检测考试化学试题
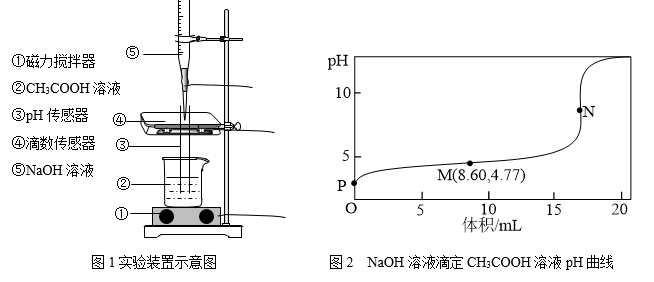
6 . 25℃下,某同学按图1所示,边用磁力搅拌器搅拌边向20.00mL浓度为 的
的 溶液中逐滴加入
溶液中逐滴加入 的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
 的
的 溶液中逐滴加入
溶液中逐滴加入 的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
的NaOH溶液,用pH传感器和滴数传感器同时测定溶液的pH和所用NaOH溶液的体积。实验测得溶液的pH随NaOH溶液体积的变化如图2所示。其中N点为反应终点,此时消耗NaOH溶液的体积为17.20mL。下列说法中错误的是
A.25℃时, 的电离常数 的电离常数 的数量级为 的数量级为 |
B.N点溶液中: |
C.水的电离程度: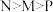 |
D.M点溶液中: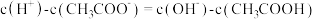 |
您最近一年使用:0次
2021-12-06更新
|
431次组卷
|
3卷引用:河南省部分重点高中2021-2022学年高三上学期12月适应性检测化学试题
河南省部分重点高中2021-2022学年高三上学期12月适应性检测化学试题福建省长汀县第一中学2021-2022学年高三上学期第三次月考化学试题(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
名校
解题方法
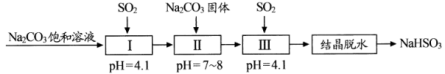
7 . 利用烟道气中的 生产
生产 晶体的工艺流程如下所示。下列说法错误的是
晶体的工艺流程如下所示。下列说法错误的是
 生产
生产 晶体的工艺流程如下所示。下列说法错误的是
晶体的工艺流程如下所示。下列说法错误的是
A. 时,步骤Ⅰ中溶液为 时,步骤Ⅰ中溶液为 溶液 溶液 |
B.步骤Ⅲ所得溶液中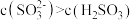 |
C.向 饱和溶液中通入 饱和溶液中通入 的过程,水的电离程度先增大后减小 的过程,水的电离程度先增大后减小 |
D.步骤Ⅱ中发生的反应之一为: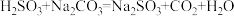 ,则 ,则 的 的 大于 大于 的 的 |
您最近一年使用:0次
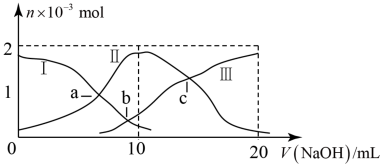
8 . 常温下,向10mL某浓度的二元弱酸 溶液中滴加
溶液中滴加 NaOH溶液,含A微粒的物质的量变化曲线如图所示,下列有关说法不正确的是
NaOH溶液,含A微粒的物质的量变化曲线如图所示,下列有关说法不正确的是
 溶液中滴加
溶液中滴加 NaOH溶液,含A微粒的物质的量变化曲线如图所示,下列有关说法不正确的是
NaOH溶液,含A微粒的物质的量变化曲线如图所示,下列有关说法不正确的是
A.曲线Ⅱ代表 的物质的量 的物质的量 |
B.水的电离程度大小:a点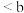 点 点 点 点 |
C. 时,溶液温度最高, 时,溶液温度最高,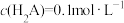 |
D.若c点溶液的 ,则 ,则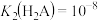 |
您最近一年使用:0次
名校
9 . 图中表示两种等体积的碱性溶液在稀释过程中pH的变化,下列相关说法正确的是
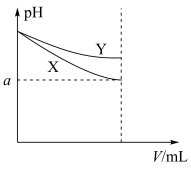

| A.两溶液稀释相同倍数,水电离的OH-浓度可能X>Y,也可能是X<Y |
| B.若图中曲线分别表示CH3COONa溶液和NaClO溶液,则X为CH3COONa溶液[已知Ka(CH3COOH)> Ka(HClO)] |
| C.加水稀释到任何程度,图中a一定大于7 |
| D.若图中曲线分别表示NaOH溶液和氨水,则起始时NaOH溶液浓度更大 |
您最近一年使用:0次
2021-11-15更新
|
884次组卷
|
6卷引用:浙江省A9协作体2021-2022学年高二上学期期中联考化学试题
浙江省A9协作体2021-2022学年高二上学期期中联考化学试题(已下线)期末综合测试卷01-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)安徽省池州市江南中学2021-2022学年高二上学期12月月考化学试题浙江省桐庐中学2021-2022学年高二12月阶段性测试化学试题浙江省衢温“5+1”联盟2021-2022学年高一下学期期中考试化学(创新班)试题浙江省杭州市浙江大学附属中学2021-2022学年高二上学期期末考试化学试题
10 . 已知:①离子浓度为10-5mol/L时可认为沉淀完全;② 。向
。向 和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
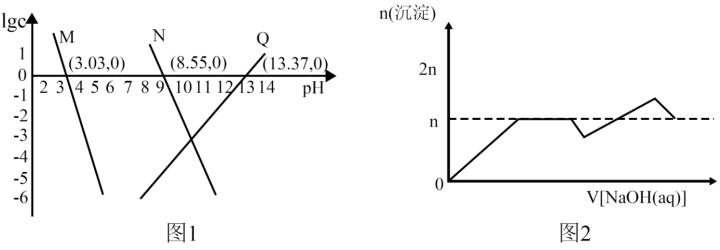
下列说法正确的是:
 。向
。向 和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
下列说法正确的是:
| A.图1中M代表Mg2+ |
B. |
| C.[Al(OH)4]-完全沉淀时,溶液pH=6.37 |
| D.该实验中,沉淀的物质的量随NaOH溶液体积变化图象如图2 |
您最近一年使用:0次
2021-10-13更新
|
2307次组卷
|
2卷引用:湖北省武昌实验中学2022届高三十月阶段性测试化学试题



