名校
解题方法
1 . 室温下,向10.0mL纯碱(可能含有NaHCO3)的稀溶液中逐滴加入0.100mol•L-1盐酸,滴定曲线如图,其中p、q为滴定终点。

下列分析正确 的是

下列分析
A.m处溶液pH>7,原因是 +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
| B.由滴定数据可推知,原纯碱中不含NaHCO3 |
C.p和q处的溶液中,均存在c(Na+)+c(H+)=2c( )+c( )+c( )+c(OH-) )+c(OH-) |
| D.原纯碱稀溶液中c(Na+)=0.215mol•L-1 |
您最近一年使用:0次
2023-04-01更新
|
1022次组卷
|
6卷引用:广西柳州高级中学2023-2024学年高三上学期8月开学考试化学试题
广西柳州高级中学2023-2024学年高三上学期8月开学考试化学试题北京市东城区2023届一模考试化学试题上海市青浦区2022-2023学年高三二模测试化学试题(已下线)专题16 水溶液中的离子平衡(已下线)专题17 水溶液中的离子平衡(已下线)化学-2023年高考押题预测卷01(云南,安徽,黑龙江,山西,吉林五省通用)(含考试版、全解全析、参考答案、答题卡)
名校
解题方法
2 . 三氯化铬是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室可利用下面装置模拟制取三氯化铬( 、
、 为气流控制开关)。
为气流控制开关)。
已知: 气体有毒,遇水发生水解产生两种酸性气体
气体有毒,遇水发生水解产生两种酸性气体
(1)实验装置合理的连接顺序为a—___________ (填仪器接口字母标号)。
(2)步骤如下:
i.连接装置,检查装置气密性,装入药品并通 ;
;
ii.加热反应管至400℃;
iii.控制开关,加热 ,温度保持在50℃~60℃之间;
,温度保持在50℃~60℃之间;
iv.加热石英管继续升温至650℃,直到E中反应基本完成,切断管式炉的电源;
v.停止A装置水浴加热,……;
vi.装置冷却后,结束制备实验。
①步骤i中,开关 、
、 的状态分别为
的状态分别为___________ 。
②补全步骤v的操作:___________ ,其目的是___________ 。
(3)从安全的角度考虑,整套装置的不足是___________ 。
(4)装置D中反应的离子方程式为___________ 。
(5)取三氯化铬样品0.300g,配制成250mL溶液。移取25.00mL于碘量瓶中,加热至沸腾后,加适量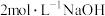 溶液,生成绿色沉淀
溶液,生成绿色沉淀 。冷却后,加足量30%
。冷却后,加足量30%  ,小火加热至绿色沉淀完全溶解。冷却后,加入
,小火加热至绿色沉淀完全溶解。冷却后,加入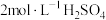 酸化,再加入足量KI溶液,加塞摇匀充分反应后,铬元素只以
酸化,再加入足量KI溶液,加塞摇匀充分反应后,铬元素只以 存在,暗处静置5min后,加入指示剂,用
存在,暗处静置5min后,加入指示剂,用 标准
标准 溶液滴定至终点,消耗标准
溶液滴定至终点,消耗标准 溶液21.00mL(杂质不参加反应)。
溶液21.00mL(杂质不参加反应)。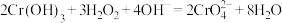 ;
; 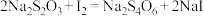
①绿色沉淀完全溶解后,继续加热一段时间再进行后续操作,目的是___________ 。
②样品中无水三氯化铬的质量分数为___________ (结果保留三位有效数字)。
③若将碘量瓶换为锥形瓶,则样品中无水三氯化铬质量分数的测量结果___________ (填“偏高”、“偏低”或“无影响”)。
 、
、 为气流控制开关)。
为气流控制开关)。

已知:
 气体有毒,遇水发生水解产生两种酸性气体
气体有毒,遇水发生水解产生两种酸性气体(1)实验装置合理的连接顺序为a—
(2)步骤如下:
i.连接装置,检查装置气密性,装入药品并通
 ;
;ii.加热反应管至400℃;
iii.控制开关,加热
 ,温度保持在50℃~60℃之间;
,温度保持在50℃~60℃之间;iv.加热石英管继续升温至650℃,直到E中反应基本完成,切断管式炉的电源;
v.停止A装置水浴加热,……;
vi.装置冷却后,结束制备实验。
①步骤i中,开关
 、
、 的状态分别为
的状态分别为②补全步骤v的操作:
(3)从安全的角度考虑,整套装置的不足是
(4)装置D中反应的离子方程式为
(5)取三氯化铬样品0.300g,配制成250mL溶液。移取25.00mL于碘量瓶中,加热至沸腾后,加适量
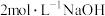 溶液,生成绿色沉淀
溶液,生成绿色沉淀 。冷却后,加足量30%
。冷却后,加足量30%  ,小火加热至绿色沉淀完全溶解。冷却后,加入
,小火加热至绿色沉淀完全溶解。冷却后,加入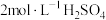 酸化,再加入足量KI溶液,加塞摇匀充分反应后,铬元素只以
酸化,再加入足量KI溶液,加塞摇匀充分反应后,铬元素只以 存在,暗处静置5min后,加入指示剂,用
存在,暗处静置5min后,加入指示剂,用 标准
标准 溶液滴定至终点,消耗标准
溶液滴定至终点,消耗标准 溶液21.00mL(杂质不参加反应)。
溶液21.00mL(杂质不参加反应)。
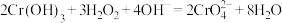 ;
; 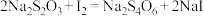
①绿色沉淀完全溶解后,继续加热一段时间再进行后续操作,目的是
②样品中无水三氯化铬的质量分数为
③若将碘量瓶换为锥形瓶,则样品中无水三氯化铬质量分数的测量结果
您最近一年使用:0次
2023-03-24更新
|
1006次组卷
|
4卷引用:广西桂林市恭城民族高级中学2023-2024学年上学期高三12月化学试卷
广西桂林市恭城民族高级中学2023-2024学年上学期高三12月化学试卷山东省枣庄市2023届高三二模考试化学试题(已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(实验综合题)山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高三下学期第二次模拟化学试题
名校
3 . 用0.1000mol/LNa2SO4标准溶液滴定20.00mLBaCl2溶液,测得溶液电导率σ及-lgc(Ba2+)随滴入Na2SO4标准溶液的体积V(Na2SO4)的变化关系如图所示。下列说法不正确的是
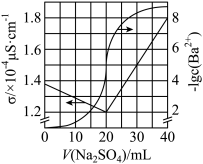
| A.BaCl2溶液的浓度为0.1000mol/L |
| B.Ksp(BaSO4)=10-10 |
| C.等浓度的Na+比Ba2+导电能力差 |
| D.若实验所用BaCl2溶液是用粗产品配制得来,则0.5000g粗产品中BaCl2•2H2O的质量分数为97.6% |
您最近一年使用:0次
2023-03-20更新
|
1919次组卷
|
7卷引用:化学02(15+4模式)2024年1月“九省联考”考前化学猜想卷
名校
4 . 某学生用 的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)______ A→F;
(2)若无上述B步骤操作,则测定结果会______ ;(填“偏高”、“偏低”、“无影响”)
(3)判断到达滴定终点的现象是:______ ;
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为2.50m,滴定后液面如图,则此时消耗标准溶液的体积为______ ;
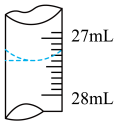
(5)乙学生做了三组平行实验,数据记录如下:选取下述合理数据,计算出待测溶液的物质的量浓度为______ ;(保留四位有效数字)
 的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)
(2)若无上述B步骤操作,则测定结果会
(3)判断到达滴定终点的现象是:
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为2.50m,滴定后液面如图,则此时消耗标准溶液的体积为

(5)乙学生做了三组平行实验,数据记录如下:选取下述合理数据,计算出待测溶液的物质的量浓度为
实验序号 | 待测HCl溶液的体积/mL |
| |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.29 |
2 | 25.00 | 1.00 | 31.00 |
3 | 25.00 | 1.00 | 27.31 |
您最近一年使用:0次
解题方法
5 . 已知草酸晶体(H2C2O4•XH2O)可溶于水,并可与酸性高锰酸钾溶液完全反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑。
现用氧化还原滴定法测定草酸晶体的结晶水分子数X,步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100mL待测草酸溶液;
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,三次结果如表:
已知H2C2O4的相对分子质量为90,请回答下列问题:
(1)滴定时,KMnO4标准溶液应该装在_____ (填“酸式”或“碱式”)滴定管中。
(2)在整个实验过程 中,不需要的仪器或用品是_____ (填序号)。
①100mL容量瓶 ②烧杯 ③滴定管夹 ④漏斗 ⑤玻璃棒 ⑥托盘天平
(3)到达滴定终点的标志是_____ 。
(4)根据上述数据计算X=_____ 。
(5)误差分析(填:偏高、偏低、无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则测得草酸的浓度_____ ;
②若滴定管水洗后直接加入KMnO4标准溶液,则测得草酸的浓度_____ ;
③若滴定管在滴定草酸前有气泡,滴定后气泡消失,则测得草酸的浓度_____ 。
现用氧化还原滴定法测定草酸晶体的结晶水分子数X,步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100mL待测草酸溶液;
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,三次结果如表:
| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
| 标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
(1)滴定时,KMnO4标准溶液应该装在
(2)在
①100mL容量瓶 ②烧杯 ③滴定管夹 ④漏斗 ⑤玻璃棒 ⑥托盘天平
(3)到达滴定终点的标志是
(4)根据上述数据计算X=
(5)误差分析(填:偏高、偏低、无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则测得草酸的浓度
②若滴定管水洗后直接加入KMnO4标准溶液,则测得草酸的浓度
③若滴定管在滴定草酸前有气泡,滴定后气泡消失,则测得草酸的浓度
您最近一年使用:0次
名校
解题方法
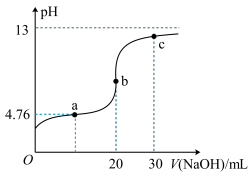
6 . 25°C时,用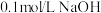 溶液滴定
溶液滴定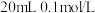 一元弱酸
一元弱酸 溶液,滴定曲线如图所示。已知:
溶液,滴定曲线如图所示。已知: ,下列说法正确的是
,下列说法正确的是
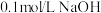 溶液滴定
溶液滴定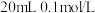 一元弱酸
一元弱酸 溶液,滴定曲线如图所示。已知:
溶液,滴定曲线如图所示。已知: ,下列说法正确的是
,下列说法正确的是
| A.滴定时可选用甲基橙或紫色石蕊试液作指示剂 |
B.c点时溶液中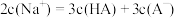 |
C.b点时溶液 |
D.a点时加入的 溶液体积等于10mL 溶液体积等于10mL |
您最近一年使用:0次
2022-12-07更新
|
397次组卷
|
3卷引用:广西三新联盟2022-2023学年高二上学期11月联考化学试题
名校
解题方法
7 . 下列由实验现象得出的结论不正确的是
| 操作 | 现象及结论 | |
| A | 向氯化铁溶液中加入过量的 溶液,充分反应后,再滴入几滴 溶液,充分反应后,再滴入几滴 溶液,溶液颜色变红 溶液,溶液颜色变红 | 验证 与 与 的反应为可逆反应 的反应为可逆反应 |
| B | 将充满 的密闭玻璃球浸泡在热水中 的密闭玻璃球浸泡在热水中 | 玻璃球中红棕色加深,说明反应 的 的 |
| C | 往盛有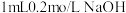 溶液的试管中加入2滴 溶液的试管中加入2滴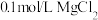 溶液,产生白色沉淀,再滴加2滴 溶液,产生白色沉淀,再滴加2滴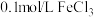 溶液,又产生红褐色沉淀 溶液,又产生红褐色沉淀 | 验证该温度下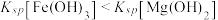 |
| D | 用 的 的 溶液滴定未知浓度的盐酸,选用酚酞做指示剂 溶液滴定未知浓度的盐酸,选用酚酞做指示剂 | 滴定终点颜色变化:溶液由无色变为浅红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-07更新
|
139次组卷
|
2卷引用:广西三新联盟2022-2023学年高二上学期11月联考化学试题
8 . 二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)在处理废水时,ClO2 可将废水中的CN-氧化成CO2和N2,写出该反应的离子方程式:_______ 。
(2)某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2.

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是_______ 。
②装置B的作用是_______ 。
③A装置中,装H2SO4溶液的仪器名称为:_______ 。
(3)测定装置C中ClO2溶液的浓度:取10mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入_______ 作指示剂,用0.1000mol·L ‑1的Na2S2O3标准液滴定锥形瓶中的溶液(I2+2 = 2I-+
= 2I-+ ),当看到
),当看到_______ 现象时,测得标准液消耗的体积为20.00mL,通过计算可知C中ClO2溶液的浓度为_______ mol·L-1。
(4)下列操作使测定结果偏高的是_______
(1)在处理废水时,ClO2 可将废水中的CN-氧化成CO2和N2,写出该反应的离子方程式:
(2)某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2.

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
②装置B的作用是
③A装置中,装H2SO4溶液的仪器名称为:
(3)测定装置C中ClO2溶液的浓度:取10mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入
 = 2I-+
= 2I-+ ),当看到
),当看到(4)下列操作使测定结果偏高的是_______
| A.滴定前平视,滴定终点俯视读数 |
| B.盛放Na2S2O3标准溶液的滴定管未用标准液润洗 |
| C.用C中溶液润洗锥形瓶,再取10mLC中溶液于锥形瓶中 |
| D.滴定前正常,滴定后滴定管尖嘴内有气泡 |
您最近一年使用:0次
9 . 过氧化钙遇水放出氧气,且过氧化钙本身无毒,不污染环境,是一种用途广泛的优良供氧剂。以大理石(含有少量氧化亚铁和氧化铁杂质)为原料制备过氧化钙的工艺流程如图所示。

回答下列问题:
(1)为了加快大理石和盐酸的反应速率,可以采取的措施为_______ (写出一点)。
(2)为了验证“滤液M”中是否含有 ,可取少量“滤液M”于试管中,向其中加入
,可取少量“滤液M”于试管中,向其中加入_______ 溶液(填试剂名称),溶液变成血红色,则证明“滤液M”中有 。
。
(3)反应Ⅰ是放热反应,不同浓度的 溶液对反应生成
溶液对反应生成 的产率的影响如图所示,
的产率的影响如图所示, 的浓度大于20%后
的浓度大于20%后 的产率反而下降的原因是
的产率反而下降的原因是_______ 。

(4)制备所得的过氧化钙中常含有CaO杂质,实验室可按以下步骤测定 的质量分数:
的质量分数:
步骤1:准确称取0.3900g过氧化钙样品,置于250mL的锥形瓶中;
步骤2:加入10mL蒸馏水和适当过量的磷酸溶液,振荡使样品完全溶解;
步骤3:用 的酸性
的酸性 溶液滴定至终点,记录数据;
溶液滴定至终点,记录数据;
步骤4:平行测定3次(数据记录见下表),计算试样中 的质量分数。
的质量分数。
已知:上述实验过程中反应关系为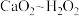 ,
,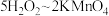 。
。
①滴定时,将酸性 标准液装在如图中的
标准液装在如图中的_______ (填“甲”或“乙”)滴定管中,滴定管用蒸馏水洗涤后,直接加入酸性 标准液进行滴定,则测定的
标准液进行滴定,则测定的 的质量分数会
的质量分数会_______ (填“偏高”“偏低”或“无影响”)。

②在滴定时,眼睛应观察________ 。在锥形瓶下垫一张白纸,其目的是_______ 。
③由表中数据可知,该样品中 的质量分数为
的质量分数为_______ %。(保留整数)
④有一支25mL的酸式滴定管,其中盛有溶液,液面恰好在5.00mL刻度处,现把管内液体全部放出,得到液体的体积_______ 20.00mL(填“大于”“小于”或“等于”)。

回答下列问题:
(1)为了加快大理石和盐酸的反应速率,可以采取的措施为
(2)为了验证“滤液M”中是否含有
 ,可取少量“滤液M”于试管中,向其中加入
,可取少量“滤液M”于试管中,向其中加入 。
。(3)反应Ⅰ是放热反应,不同浓度的
 溶液对反应生成
溶液对反应生成 的产率的影响如图所示,
的产率的影响如图所示, 的浓度大于20%后
的浓度大于20%后 的产率反而下降的原因是
的产率反而下降的原因是
(4)制备所得的过氧化钙中常含有CaO杂质,实验室可按以下步骤测定
 的质量分数:
的质量分数:步骤1:准确称取0.3900g过氧化钙样品,置于250mL的锥形瓶中;
步骤2:加入10mL蒸馏水和适当过量的磷酸溶液,振荡使样品完全溶解;
步骤3:用
 的酸性
的酸性 溶液滴定至终点,记录数据;
溶液滴定至终点,记录数据;步骤4:平行测定3次(数据记录见下表),计算试样中
 的质量分数。
的质量分数。| 实验 | 1 | 2 | 3 |
V(酸性 溶液)/mL 溶液)/mL | 19.50 | 19.48 | 19.52 |
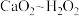 ,
,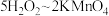 。
。①滴定时,将酸性
 标准液装在如图中的
标准液装在如图中的 标准液进行滴定,则测定的
标准液进行滴定,则测定的 的质量分数会
的质量分数会
②在滴定时,眼睛应观察
③由表中数据可知,该样品中
 的质量分数为
的质量分数为④有一支25mL的酸式滴定管,其中盛有溶液,液面恰好在5.00mL刻度处,现把管内液体全部放出,得到液体的体积
您最近一年使用:0次
2022-11-10更新
|
127次组卷
|
2卷引用:广西北海市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
10 . 硫氰化钾(KSCN) 俗称玫瑰红酸钾,是一种用途广泛的化学药品。某实验小组模拟工业制备硫氰化钾的方法,设计实验如图:
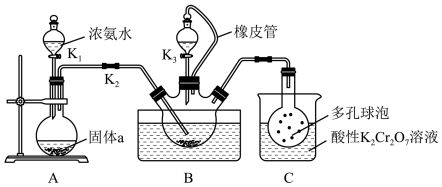
已知:CS2是一种不溶于水、密度大于水的非极性试剂。请回答下列问题:
I.制备NH4SCN溶液
(1)装浓氨水的仪器名称是___________ 。
(2)装置A用于制备NH3,圆底烧瓶内的固体a可以是___________ 。
(3)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应CS2+ 3NH3 NH4SCN+NH4HS。实验开始时,打开K2和K1,水浴加热三颈烧瓶,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是
NH4SCN+NH4HS。实验开始时,打开K2和K1,水浴加热三颈烧瓶,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是___________ 。一段时间后,当观察到三颈烧瓶内液体不再分层时,停止通入气体,反应完成。
II.制备KSCN溶液
(4)关闭K1,加热三颈烧瓶,保持水浴温度为100℃一段时间,使分解反应(NH4HS=NH3↑+H2S↑)进行完全后,再打开K3,继续保持水浴温度为100℃,缓缓滴入稍过量的KOH溶液,制得KSCN溶液。装置C中酸性K2Cr2O7溶液除能将H2S气体氧化成硫酸外,还可以___________ 。
III.制备KSCN晶体
(5)先通过过滤除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有___________ (填标号)。
A.坩埚 B.蒸发皿 C.分液漏斗 D.玻璃棒 E.烧杯
(6)测定晶体中KSCN的含量:称取3.0g样品,配成250mL溶液。量取25. 00mL溶液加入锥形瓶中,加入适量稀硝酸,再加入几滴Fe (NO3) 3溶液作指示剂,用0. 1000mol/L AgNO3标准溶液滴定,达到滴定终点,三次滴定平均消耗AgNO3标准溶液24.00mL。[已知: SCN-+Ag+=AgSCN↓(白色) ]
①晶体中KSCN的质量分数为___________ (计算结果保留三位有效数字)。
②滴定达到终点后,发现滴定管尖嘴处悬挂有一滴AgNO3标准溶液,则测得KSCN的质量分数___________ (填“偏大”、“偏小”或“无影响”)。

已知:CS2是一种不溶于水、密度大于水的非极性试剂。请回答下列问题:
I.制备NH4SCN溶液
(1)装浓氨水的仪器名称是
(2)装置A用于制备NH3,圆底烧瓶内的固体a可以是
(3)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应CS2+ 3NH3
 NH4SCN+NH4HS。实验开始时,打开K2和K1,水浴加热三颈烧瓶,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是
NH4SCN+NH4HS。实验开始时,打开K2和K1,水浴加热三颈烧瓶,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是II.制备KSCN溶液
(4)关闭K1,加热三颈烧瓶,保持水浴温度为100℃一段时间,使分解反应(NH4HS=NH3↑+H2S↑)进行完全后,再打开K3,继续保持水浴温度为100℃,缓缓滴入稍过量的KOH溶液,制得KSCN溶液。装置C中酸性K2Cr2O7溶液除能将H2S气体氧化成硫酸外,还可以
III.制备KSCN晶体
(5)先通过过滤除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有
A.坩埚 B.蒸发皿 C.分液漏斗 D.玻璃棒 E.烧杯
(6)测定晶体中KSCN的含量:称取3.0g样品,配成250mL溶液。量取25. 00mL溶液加入锥形瓶中,加入适量稀硝酸,再加入几滴Fe (NO3) 3溶液作指示剂,用0. 1000mol/L AgNO3标准溶液滴定,达到滴定终点,三次滴定平均消耗AgNO3标准溶液24.00mL。[已知: SCN-+Ag+=AgSCN↓(白色) ]
①晶体中KSCN的质量分数为
②滴定达到终点后,发现滴定管尖嘴处悬挂有一滴AgNO3标准溶液,则测得KSCN的质量分数
您最近一年使用:0次
2022-10-01更新
|
190次组卷
|
2卷引用:广西玉林市普通高中2021-2022学年高二下学期期末考试理科综合化学试题



