1 . 从废定影液[主要含有 、
、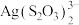 、
、 、
、 等微粒]中回收Ag和
等微粒]中回收Ag和 的主要步骤:向该废定影液中加入NaOH调节pH在7.5~8.5之间,然后再加入稍过量
的主要步骤:向该废定影液中加入NaOH调节pH在7.5~8.5之间,然后再加入稍过量 溶液沉银,过滤、洗涤及干燥,灼烧
溶液沉银,过滤、洗涤及干燥,灼烧 制Ag;滤液中通入
制Ag;滤液中通入 氧化
氧化 ,用苯萃取分液。下列有关从废定影液中回收Ag和
,用苯萃取分液。下列有关从废定影液中回收Ag和 的说法正确的是
的说法正确的是
 、
、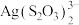 、
、 、
、 等微粒]中回收Ag和
等微粒]中回收Ag和 的主要步骤:向该废定影液中加入NaOH调节pH在7.5~8.5之间,然后再加入稍过量
的主要步骤:向该废定影液中加入NaOH调节pH在7.5~8.5之间,然后再加入稍过量 溶液沉银,过滤、洗涤及干燥,灼烧
溶液沉银,过滤、洗涤及干燥,灼烧 制Ag;滤液中通入
制Ag;滤液中通入 氧化
氧化 ,用苯萃取分液。下列有关从废定影液中回收Ag和
,用苯萃取分液。下列有关从废定影液中回收Ag和 的说法正确的是
的说法正确的是| A.过滤时,为加快滤液流下,可以用玻璃棒搅拌漏斗中的液体 |
B.配制 溶液时,向其中加入少量NaOH溶液, 溶液时,向其中加入少量NaOH溶液, 的值增大 的值增大 |
C.燃烧 生成Ag和 生成Ag和 , , 既是还原剂又是氧化剂 既是还原剂又是氧化剂 |
| D.分液时,先放出水层,再从分液漏斗下口放出含有苯和溴的有机层 |
您最近一年使用:0次
解题方法
2 . 用废铜屑(含Cu,CuO、Fe2O3等)制备胆矾的流程如下:
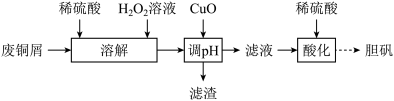
下列说法不正确的是

下列说法不正确的是
| A.“溶解”时,铜发生反应的离子方程式为Cu+2H++H2O2= Cu2++2H2O |
| B.“调pH” ,可用NaOH溶液代替CuO |
C.“滤液”中c(Cu2+)·c2(OH-)≤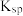 [Cu(OH)2] [Cu(OH)2] |
| D.“酸化”时,加入稀硫酸的目的是抑制Cu2+的水解 |
您最近一年使用:0次
名校
解题方法
3 . 以硫铁矿(主要成分为FeS2含有少量CuS杂质为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

(1)在一定条件下,SO2转化为SO3的反应为2SO2+O2 2SO3,该反应的平衡常数表达式为K=
2SO3,该反应的平衡常数表达式为K=___________ ;过量的SO2与NaOH溶液反应的化学方程式为___________ 。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是___________ 。
(3)通氯气氧化Fe2+时,发生的主要反应的离子方程式为___________ 。
(4)在氧化步骤后,为了分离溶液中的Fe3+、Cu2+,先调节pH使氢氧化铁完全沉淀,过滤后用盐酸溶解,得到FeCl3溶液。查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp =3.0×10-18,当溶液中离子浓度小于1×10-5 mol/L时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol/L,则Cu(OH)2开始沉淀时溶液的pH为___________ ,Fe3+完全沉淀时溶液的pH为___________ ( 已知1g2=0.3),上述方案应调节pH范围:___________ 。

(1)在一定条件下,SO2转化为SO3的反应为2SO2+O2
 2SO3,该反应的平衡常数表达式为K=
2SO3,该反应的平衡常数表达式为K=(2)酸溶及后续过程中均需保持盐酸过量,其目的是
(3)通氯气氧化Fe2+时,发生的主要反应的离子方程式为
(4)在氧化步骤后,为了分离溶液中的Fe3+、Cu2+,先调节pH使氢氧化铁完全沉淀,过滤后用盐酸溶解,得到FeCl3溶液。查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp =3.0×10-18,当溶液中离子浓度小于1×10-5 mol/L时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol/L,则Cu(OH)2开始沉淀时溶液的pH为
您最近一年使用:0次
名校
4 . 根据下列实验操作过程中颜色变化所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将NaClO溶液滴入品红溶液中,品红溶液缓慢褪色;若同时加入食醋,红色很快褪去 | ClO-的氧化性随pH的减小而增强 |
| B | 向NaCl与NaBr混合溶液中滴加AgNO3溶液,观察到出现淡黄色沉淀 | Ksp(AgBr)<Ksp(AgCl) |
| C | 向滴有酚酞的氨水中加入CH3COONH4固体,溶液的红色变浅 | CH3COONH4溶液呈酸性 |
| D | 向含AgCl和AgBr的饱和溶液中加入足量浓AgNO3 溶液,产生两种颜色沉淀,但以白色为主 | 溶液中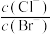 减小 减小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列说法正确的是
| A.氯化钠和氯化铯晶体中氯离子的配位数相同 |
| B.常温下,反应2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)能自发进行,该反应ΔH<0 |
C.反应C(s)+H2O(g) CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变 CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变 |
| D.0.1 mol·L-1 NH4Cl溶液加水稀释,c(OH-)减小 |
您最近一年使用:0次
2020-11-07更新
|
147次组卷
|
2卷引用:江苏省镇江市镇江中学2020-2021学年高二下学期期中考试化学试题
解题方法
6 . 下列说法说法正确的是
| A.外接电源保护水中钢闸门时,应将钢闸门与电源的正极相连 |
| B.向Na2CO3溶液中加入少量BaCl2固体,CO32-水解程度增大,溶液的pH减小 |
C.如图表示常温下稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水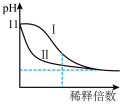 |
| D.2NO(g)+2CO(g)===N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0 |
您最近一年使用:0次
名校
7 . 有关下列两种溶液的说法中,正确的是( )
①0.1mol/L CH3COONa溶液 ②0.1mol/L CH3COOH溶液
①0.1mol/L CH3COONa溶液 ②0.1mol/L CH3COOH溶液
| A.相同温度下,溶液中水的电离度:溶液①>溶液② |
| B.等体积混合溶液①和溶液②,所得溶液中c(Na+)>c( CH3COO-)>c(H+)>c(OH-) |
C.加水稀释溶液①,溶液中 不变 不变 |
D.向溶液①中加入少量的CH3COONa固体则 减小 减小 |
您最近一年使用:0次
2020-01-06更新
|
124次组卷
|
4卷引用:江苏省镇江市吕叔湘中学2019-2020学年高二下学期4月诊断考试化学试题
11-12高二上·湖北荆州·期末
名校
8 . 物质的量浓度相同的下列溶液中,c(NH4+)最大的是
| A.NH4Cl | B.CH3COONH4 | C.NH4HCO3 | D.NH4HSO4 |
您最近一年使用:0次
2019-02-25更新
|
1624次组卷
|
26卷引用:2014-2015江苏省扬中高级中学高二第一学期化学试卷
2014-2015江苏省扬中高级中学高二第一学期化学试卷(已下线)2010—2011学年湖北省荆州中学高二上学期期末考试化学试卷(已下线)2010—2011学年云南省昆明三中高二下学期期末考试化学试卷(已下线)2011-2012年湖南株洲市南方中学高二上学期期末考试理科化学试卷(已下线)2012年鲁科版高中化学选修4 3.2弱电解质的电离、盐类的水练习卷(已下线)2012-2013学年江苏省淮安市涟水县第一中学高一下期末考试化学卷(已下线)2013-2014学年江苏省南师附中江宁分校高二上学期选修期末化学试卷(已下线)2013-2014学年甘肃省兰州一中高二上学期期末考试化学试卷2014-2015福建省八县一中高二上学期期末考试化学试卷2015-2016学年河北邯郸魏县一中、曲周县一中高二上期中化学试卷2015-2016学年河北省邢台二中高二上学期第二次月考化学试卷2015-2016学年河北省永年县第二中学高二上学期12月月考化学试卷2015-2016学年河北省唐山市高二上学期期末考试化学试卷2016-2017学年甘肃省武威二中高二上10月月考化学试卷(已下线)2018年11月11日——《每日一题》 人教 必修4-每周一测【全国百强校】山西省太原市第五中学2018-2019学年高二(理)上学期12月月考化学试题【区级联考】重庆市九龙坡区2018-2019学年高二上学期教育质量全面监测化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期期中考试(B班)化学试题河南省项城市第三高级中学2020-2021学年高二上学期第三次考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期开学考试化学试题广西南宁市上林县中学2020-2021学年高二上学期期末考试化学试题上海市上海中学东校2020届高三上学期期中考试化学试题陕西省渭南市咸林中学2021-2022学年高二上学期第三阶段检测化学试题青海省西宁市湟源县第一中学2020-2021学年高二上学期期中考试化学试题宁夏银川市唐徕中学2022-2023学年高二下学期3月月考化学试题江西省宜春市宜丰中学2023-2024学年高二上学期12月月考化学试题
名校
9 . 下列实验操作、现象与所得结论一致的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸,并用激光笔照射 | 溶液变红褐色,出现 丁达尔效应 | 产生了 Fe(OH)3胶体 |
| B | 向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
| c | 将溴乙烷和NaOH的乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-24更新
|
573次组卷
|
4卷引用:2017届江苏省丹阳高级中学高三下学期期中考试化学试卷
名校
10 . 下列说法正确的是
| A.铅蓄电池充电时,阳极质量增大 |
| B.0.1mol ·L-lCH3COONa溶液加热后,溶液的pH减小 |
| C.标准状况下,11.2L苯中含有的碳原子数为3×6.02×1023 |
| D.室温下,稀释0.1mol·L-1氨水,c(H+)·c(NH3·H2O)的值减小 |
您最近一年使用:0次
2017-03-24更新
|
458次组卷
|
4卷引用:2017届江苏省丹阳高级中学高三下学期期中考试化学试卷



