名校
解题方法
1 . 一种脱除烟气中 并除去水溶液中
并除去水溶液中 的方法如下图甲所示。室温下用NaOH溶液吸收
的方法如下图甲所示。室温下用NaOH溶液吸收 ,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度
,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度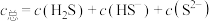 ,含硫微粒分布百分数如下图乙所示。已知室温时
,含硫微粒分布百分数如下图乙所示。已知室温时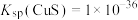

室温时,下列说法正确的是
 并除去水溶液中
并除去水溶液中 的方法如下图甲所示。室温下用NaOH溶液吸收
的方法如下图甲所示。室温下用NaOH溶液吸收 ,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度
,过程中气体挥发和溶液体积的变化可忽略。吸收液中含硫微粒的浓度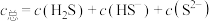 ,含硫微粒分布百分数如下图乙所示。已知室温时
,含硫微粒分布百分数如下图乙所示。已知室温时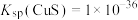

室温时,下列说法正确的是
A.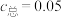 mol⋅L-1的吸收液中: mol⋅L-1的吸收液中: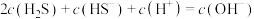 |
B. mol⋅L-1的吸收液中: mol⋅L-1的吸收液中: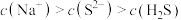 |
C.除铜后所得溶液中一定存在: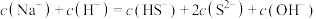 |
D.反应 的平衡常数 的平衡常数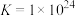 |
您最近一年使用:0次
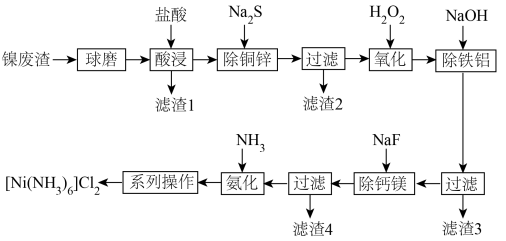
2 . [Ni(NH3)6]Cl2在有机合成中有广泛应用。以镍废渣(主要含Ni、CuO、FeO、ZnO、Al2O3、MgO、CaCO3和SiO2)为原料制备[Ni(NH3)6]Cl2的工艺流程如下。回答下列问题: 都不能氧化
都不能氧化 。
。
②25℃时,几种氢氧化物和氟化物的 如表所示:
如表所示:
③25℃时,几种金属硫化物的 如表所示:
如表所示:
(1)“酸浸”之前“球磨”,目的是___________ ,“酸浸”时适当加热可以提高反应速率,但是温度过高,速率反而减小,其原因是___________ 。
(2)“除铜锌”时,测得溶液中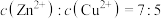 ,最先沉淀的离子是
,最先沉淀的离子是___________ (填离子符号,下同),若溶液中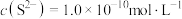 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是___________ (当溶液中某离子的浓度小于或等于 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。
(3)Na2S溶液呈碱性的原因是___________ (用离子方程式表示)。
(4)“除铁铝”中, 时,
时,
___________  。
。
(5)已知常温下, ,则NaF的水解常数
,则NaF的水解常数
___________ ;“除钙镁”时,不能选用玻璃仪器,其原因是___________ 。
 都不能氧化
都不能氧化 。
。②25℃时,几种氢氧化物和氟化物的
 如表所示:
如表所示:| 物质 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | CaF2 | MgF2 |
 |  | 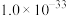 | 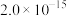 |  |  |
 如表所示:
如表所示:| 金属硫化物 | FeS | NiS | CuS | ZnS |
 | 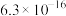 |  |  | 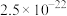 |
(1)“酸浸”之前“球磨”,目的是
(2)“除铜锌”时,测得溶液中
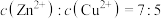 ,最先沉淀的离子是
,最先沉淀的离子是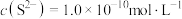 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。(3)Na2S溶液呈碱性的原因是
(4)“除铁铝”中,
 时,
时,
 。
。(5)已知常温下,
 ,则NaF的水解常数
,则NaF的水解常数
您最近一年使用:0次
2024-01-19更新
|
123次组卷
|
2卷引用:江西省部分学校2023-2024学年高三上学期12月月考化学试题
3 . 草酸亚铁 作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
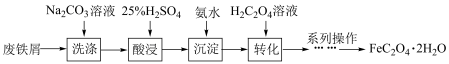
Ⅰ、 为淡黄色固体,难溶于水。
为淡黄色固体,难溶于水。
Ⅱ、25℃时,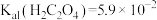 、
、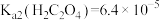 。
。
Ⅲ、25℃时,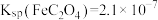 、
、 。
。
(1)用热的饱和碳酸钠溶液洗涤废铁屑的原因是_____ 。
(2)由题中信息判断,25℃时,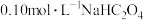 溶液中存在:
溶液中存在: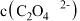
_____  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(3)“转化”步骤在如图所示的装置中进行。

仪器X的名称是_____ ,导管A的作用是_____ 。
(4)“转化”步骤的离子方程式为_____。
(5)说明“转化”步骤中不能用 溶液代替
溶液代替 溶液的原因
溶液的原因_____ 。
(6)流程图中“系列操作”指的是_____ 。
A.过滤、洗涤、干燥
B.蒸发结晶、趁热过滤、洗涤、干燥
C.蒸发浓缩、冷却结晶、过滤、洗涤、干燥
上述制备的草酸亚铁晶体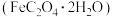 含有
含有 杂质,测定其纯度步骤如下:
杂质,测定其纯度步骤如下:
①准确称取 草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
②取20.00mL①中所得的溶液,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。
③向滴定后的溶液中加入适量锌粉充分反应后,过滤,洗涤,洗涤液并入滤液中。
④继续用 标准溶液滴定步骤③中所得滤液至终点,消耗
标准溶液滴定步骤③中所得滤液至终点,消耗 。
。
已知:

(7)配制上述100mL溶液,用到的玻璃仪器除了玻璃棒、烧杯外,还有_____ 。
(8)步骤②滴定终点的现象为_____ ;步骤③中加入锌粉的目的是_____ 。
(9)草酸亚铁晶体样品的纯度为_____ 。(用 、
、 、
、 、
、 表示)
表示)
 作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
作为一种化工原料,可广泛用于生产锂离子电池材料、感光材料。以废铁屑为原料生产草酸亚铁的流程如下:
Ⅰ、
 为淡黄色固体,难溶于水。
为淡黄色固体,难溶于水。Ⅱ、25℃时,
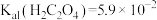 、
、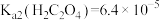 。
。Ⅲ、25℃时,
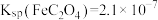 、
、 。
。(1)用热的饱和碳酸钠溶液洗涤废铁屑的原因是
(2)由题中信息判断,25℃时,
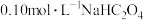 溶液中存在:
溶液中存在: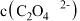
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。(3)“转化”步骤在如图所示的装置中进行。

仪器X的名称是
(4)“转化”步骤的离子方程式为_____。
A.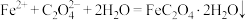 |
B.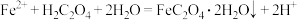 |
C.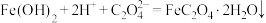 |
D.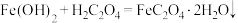 |
(5)说明“转化”步骤中不能用
 溶液代替
溶液代替 溶液的原因
溶液的原因(6)流程图中“系列操作”指的是
A.过滤、洗涤、干燥
B.蒸发结晶、趁热过滤、洗涤、干燥
C.蒸发浓缩、冷却结晶、过滤、洗涤、干燥
上述制备的草酸亚铁晶体
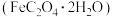 含有
含有 杂质,测定其纯度步骤如下:
杂质,测定其纯度步骤如下:①准确称取
 草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。
草酸亚铁晶体样品,溶于稀硫酸中,配成100mL溶液。②取20.00mL①中所得的溶液,用
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。③向滴定后的溶液中加入适量锌粉充分反应后,过滤,洗涤,洗涤液并入滤液中。
④继续用
 标准溶液滴定步骤③中所得滤液至终点,消耗
标准溶液滴定步骤③中所得滤液至终点,消耗 。
。已知:


(7)配制上述100mL溶液,用到的玻璃仪器除了玻璃棒、烧杯外,还有
(8)步骤②滴定终点的现象为
(9)草酸亚铁晶体样品的纯度为
 、
、 、
、 、
、 表示)
表示)
您最近一年使用:0次
名校
4 . 已知常温下水溶液中 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ]随pH变化曲线如图1;溶液中
]随pH变化曲线如图1;溶液中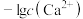 和
和 关系如图2.用
关系如图2.用
 溶液滴定20.00mL
溶液滴定20.00mL
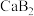 溶液,下列说法错误的是
溶液,下列说法错误的是

 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ]随pH变化曲线如图1;溶液中
]随pH变化曲线如图1;溶液中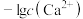 和
和 关系如图2.用
关系如图2.用
 溶液滴定20.00mL
溶液滴定20.00mL
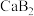 溶液,下列说法错误的是
溶液,下列说法错误的是
| A.曲线d表示δ(HB) |
B. 的水解平衡常数 的水解平衡常数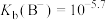 |
| C.滴定过程中溶液会变浑浊 |
D.滴定过程中始终存在: |
您最近一年使用:0次
2023-04-10更新
|
1860次组卷
|
12卷引用:河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题
河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题河北省邢台市2022-2023学年高三下学期4月第一次模拟考试化学试题(已下线)专题15 水溶液中的离子平衡山东省东营市第一中学2023届高三下学期二模化学试题东北育才学校高中部2023届高三下学期适应性考试化学试题重庆市七校2023-2024学年高三上学期开学考试化学试题湖南省长郡中学2024届高三上学期月考卷(一)化学试题湖南省长沙市长郡中学2024届高三上学期9月月考化学试题江西省宜丰中学创新部2023-2024学年高二上学期第一次(10月)月考化学试题四川省宜宾市叙州区第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)化学(九省联考考后提升卷,河南卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点18 电解质溶液图像分析
名校
5 . 二元有机酸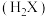 的电离常数
的电离常数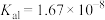 、
、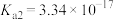 。
。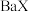 难溶于水,常温下,将
难溶于水,常温下,将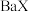 溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中
溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中 与
与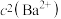 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是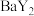 易溶于水。
易溶于水。
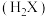 的电离常数
的电离常数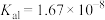 、
、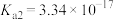 。
。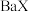 难溶于水,常温下,将
难溶于水,常温下,将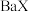 溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中
溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中 与
与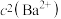 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是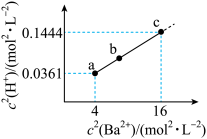
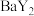 易溶于水。
易溶于水。A.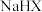 溶液显碱性 溶液显碱性 |
B.溶度积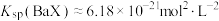 |
C.b点: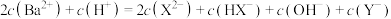 |
D.若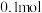 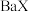 溶于 溶于 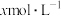 HY溶液中得到氢离子浓度与 HY溶液中得到氢离子浓度与 点相等,则 点相等,则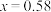 |
您最近一年使用:0次
2023-03-25更新
|
855次组卷
|
2卷引用:辽宁省辽阳市2023届高三一模化学试题
名校
解题方法
6 . 醋酸钠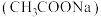 是一种常用的防腐剂和缓冲剂。
是一种常用的防腐剂和缓冲剂。
(1)配制 溶液,需要称量醋酸钠晶体(
溶液,需要称量醋酸钠晶体( ,
,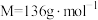 )的质量为
)的质量为_______ 。实验需要的仪器有天平、药匙、玻璃棒、量筒、_______ (从下列图中选择,写出名称)。 水解程度的影响。
水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为 ):
):
i.实验_______ 和_______ (填序号),探究加水稀释对 水解程度的影响;
水解程度的影响;
ii.实验1和3,探究加入 对
对 水解程度的影响;
水解程度的影响;
iii.实验1和4,探究温度对 水解程度的影响。
水解程度的影响。
①根据甲同学的实验方案,补充数据:
_______ 。
②实验测得 ,该结果不足以证明加入
,该结果不足以证明加入 促进了
促进了 的水解。根据
的水解。根据_______ (填一种微粒的化学式)的浓度增大可以说明加入 能促进
能促进 的水解。
的水解。
③已知 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测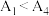 ,但实验结果为
,但实验结果为 。实验结果与预测不一致的原因是
。实验结果与预测不一致的原因是_______ 。
(3)小组通过测定不同温度下 的水解常数
的水解常数 确定温度对
确定温度对 水解程度的影响。
水解程度的影响。
查阅资料: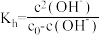 ,
, 为
为 溶液起始浓度。
溶液起始浓度。
试剂: 溶液、
溶液、 盐酸、
盐酸、 计。
计。
实验:测定40℃下 水解常数
水解常数 ,完成下表中序号7的实验。
,完成下表中序号7的实验。
在50℃和60℃下重复上述实验。
数据处理:40℃,
_______ (用含 、
、 、
、 的计算式表示)
的计算式表示)
实验结论: ,温度升高,促进
,温度升高,促进 水解。
水解。
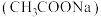 是一种常用的防腐剂和缓冲剂。
是一种常用的防腐剂和缓冲剂。(1)配制
 溶液,需要称量醋酸钠晶体(
溶液,需要称量醋酸钠晶体( ,
,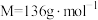 )的质量为
)的质量为
 水解程度的影响。
水解程度的影响。甲同学设计实验方案如下(表中溶液浓度均为
 ):
):i.实验
 水解程度的影响;
水解程度的影响;ii.实验1和3,探究加入
 对
对 水解程度的影响;
水解程度的影响;iii.实验1和4,探究温度对
 水解程度的影响。
水解程度的影响。| 序号 | 温度 | 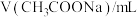 |  | 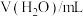 |  |
| 1 | 25℃ | 40.0 | 0 | 0 |  |
| 2 | 25℃ | 4.0 | 0 | 36.0 |  |
| 3 | 25℃ | 20.0 | 10.0 |  |  |
| 4 | 40℃ | 40.0 | 0 | 0 |  |

②实验测得
 ,该结果不足以证明加入
,该结果不足以证明加入 促进了
促进了 的水解。根据
的水解。根据 能促进
能促进 的水解。
的水解。③已知
 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测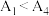 ,但实验结果为
,但实验结果为 。实验结果与预测不一致的原因是
。实验结果与预测不一致的原因是(3)小组通过测定不同温度下
 的水解常数
的水解常数 确定温度对
确定温度对 水解程度的影响。
水解程度的影响。查阅资料:
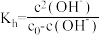 ,
, 为
为 溶液起始浓度。
溶液起始浓度。试剂:
 溶液、
溶液、 盐酸、
盐酸、 计。
计。实验:测定40℃下
 水解常数
水解常数 ,完成下表中序号7的实验。
,完成下表中序号7的实验。| 序号 | 实验 | 记录的数据 |
| 5 | 取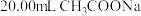 溶液,用 溶液,用 盐酸滴定至终点 盐酸滴定至终点 | 消耗盐酸体积为 |
| 6 | 测40℃纯水的 |  |
| 7 |  |
数据处理:40℃,

 、
、 、
、 的计算式表示)
的计算式表示)实验结论:
 ,温度升高,促进
,温度升高,促进 水解。
水解。
您最近一年使用:0次
2023-03-16更新
|
2404次组卷
|
5卷引用:广东省广州市2023届高三一模考试化学试题
广东省广州市2023届高三一模考试化学试题(已下线)专题19 实验综合题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(实验综合题)广东省广州市2022-2023学年高三普通高中毕业班综合测试(一)化学试题 广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题
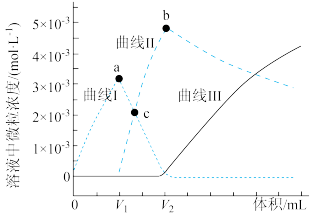
7 .  时,某实验小组利用虚拟感应器技术探究用
时,某实验小组利用虚拟感应器技术探究用 的碳酸钠溶液滴定
的碳酸钠溶液滴定 的
的 溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中 的逸出)如图所示。下列说法正确的是
的逸出)如图所示。下列说法正确的是
已知: 时,
时, 的
的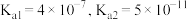 ;
;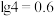 。
。
 时,某实验小组利用虚拟感应器技术探究用
时,某实验小组利用虚拟感应器技术探究用 的碳酸钠溶液滴定
的碳酸钠溶液滴定 的
的 溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中 的逸出)如图所示。下列说法正确的是
的逸出)如图所示。下列说法正确的是已知:
 时,
时, 的
的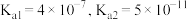 ;
; 。
。
A.碳酸钠的水解常数 |
B.曲线I为 浓度变化曲线, 浓度变化曲线, |
| C.a点和b点溶液中,水的电离程度较大的是a点 |
D.c点溶液 |
您最近一年使用:0次
2023-01-12更新
|
512次组卷
|
3卷引用:湖南省益阳市2022-2023学年高三上学期期末质量检测化学试题
名校
8 . I、常温下,有浓度均为 的下列4种溶液:
的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③ 溶液 ④
溶液 ④ 溶液
溶液
(1)这4种溶液pH由大到小的顺序是______ (填序号)
(2)若分别向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③_____ ④(填“>”“<”或“=”)。
(3)向NaCN溶液中通入少量 ,则发生反应的离子方程式为
,则发生反应的离子方程式为______ 。
(4)泡沫灭火器中通常装有 溶液和
溶液和 溶液,请写出这两种溶液混合时反应的离子方程式:
溶液,请写出这两种溶液混合时反应的离子方程式:______ 。
(5)已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数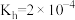 ,当溶液中
,当溶液中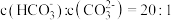 时,溶液的pH=
时,溶液的pH=________ 。
II、某同学用酸性 溶液测定绿矾产品中
溶液测定绿矾产品中 含量:请回答下列问题:
含量:请回答下列问题:
反应原理为: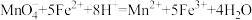 (
( 在溶液中为无色)
在溶液中为无色)
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L 溶液滴定至终点
溶液滴定至终点
(6)若甲学生在实验过程中,记录滴定前后滴定管内液面读数如图所示,则此时消耗标准溶液的体积为_________ mL。

(7)此滴定实验达到终点的颜色变化为______ 。
(8)重复滴定4次,每次消耗酸性 标准溶液的体积如表所示:
标准溶液的体积如表所示:
计算上述样品中 的质量分数为
的质量分数为______ 。( ,
,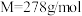 ,小数点后保留一位)
,小数点后保留一位)
(9)若滴定前平视读数,滴定终点时仰视读数,则所测 含量:
含量:______ 。(填“无影响”、“偏高”或“偏低”)。
 的下列4种溶液:
的下列4种溶液:①NaCN溶液 ②NaOH溶液 ③
 溶液 ④
溶液 ④ 溶液
溶液| HCN |  |  |
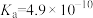 | 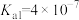 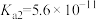 | 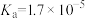 |
(2)若分别向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
(3)向NaCN溶液中通入少量
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为(4)泡沫灭火器中通常装有
 溶液和
溶液和 溶液,请写出这两种溶液混合时反应的离子方程式:
溶液,请写出这两种溶液混合时反应的离子方程式:(5)已知25℃时,
 第一步水解的平衡常数
第一步水解的平衡常数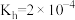 ,当溶液中
,当溶液中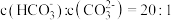 时,溶液的pH=
时,溶液的pH=II、某同学用酸性
 溶液测定绿矾产品中
溶液测定绿矾产品中 含量:请回答下列问题:
含量:请回答下列问题:反应原理为:
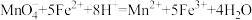 (
( 在溶液中为无色)
在溶液中为无色)a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L
 溶液滴定至终点
溶液滴定至终点(6)若甲学生在实验过程中,记录滴定前后滴定管内液面读数如图所示,则此时消耗标准溶液的体积为

(7)此滴定实验达到终点的颜色变化为
(8)重复滴定4次,每次消耗酸性
 标准溶液的体积如表所示:
标准溶液的体积如表所示:| 第一次 | 第二次 | 第三次 | 第四次 | |
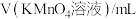 | 17.10 | 19.98 | 20.00 | 20.02 |
 的质量分数为
的质量分数为 ,
,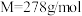 ,小数点后保留一位)
,小数点后保留一位)(9)若滴定前平视读数,滴定终点时仰视读数,则所测
 含量:
含量:
您最近一年使用:0次
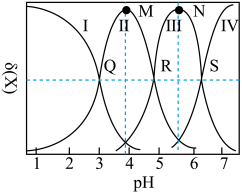
9 . 均苯三甲酸是一种重要的有机三元弱酸,可表示为 。向
。向 的
的 溶液中加入
溶液中加入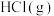 或
或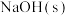 时(忽略溶液体积的变化),各微粒的分布系数
时(忽略溶液体积的变化),各微粒的分布系数 随溶液
随溶液 变化的曲线如图所示:
变化的曲线如图所示:
已知:①[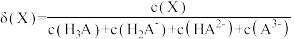 ,X为
,X为 、
、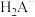 、
、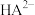 或
或 ]
]
②(
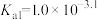 、
、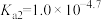 、
、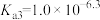 )
)
 。向
。向 的
的 溶液中加入
溶液中加入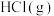 或
或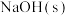 时(忽略溶液体积的变化),各微粒的分布系数
时(忽略溶液体积的变化),各微粒的分布系数 随溶液
随溶液 变化的曲线如图所示:
变化的曲线如图所示:已知:①[
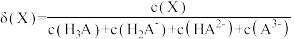 ,X为
,X为 、
、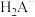 、
、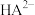 或
或 ]
]②(

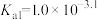 、
、 、
、 )
)
A.若用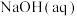 滴定 滴定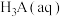 至恰好生成 至恰好生成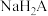 ,可选甲基橙做指示剂 ,可选甲基橙做指示剂 |
B.N点的 |
C.常温下,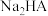 的水解常数 的水解常数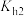 的数量级为 的数量级为 |
D.R点满足: |
您最近一年使用:0次
2022-11-25更新
|
1559次组卷
|
6卷引用:广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题1-16)
名校
解题方法
10 . 常温下,向0.1mol•L-1的乙二胺(H2NCH2CH2NH2)溶液中不断通入HCl气体,溶液中三种含氮微粒的物质的量分数δ与pOH的关系图如图。已知:①乙二胺为无色液体,有类似氨的性质,常温下Kb1=10-4.07,Kb2=10-7.15;②假设溶液体积保持不变。下列说法中不正确 的是{已知:pOH=-lgc(OH-)}
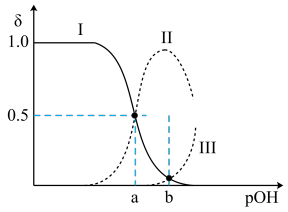

A.曲线Ⅱ代表的微粒符号为H2NCH2CH2NH |
| B.b点的对应pOH=5.61 |
| C.pOH=a时,c(Cl-)>0.05mol•L-1 |
| D.在0.1mol•L-1H2NCH2CH2NH3Cl溶液中:c([H2NCH2CH2NH3]+)>c([H3NCH2CH2NH3]2+)>c(H2NCH2CH2NH2) |
您最近一年使用:0次
2022-10-08更新
|
1170次组卷
|
2卷引用:新疆乌鲁木齐市第十二中学2023-2024学年高三上学期11月月考化学试题



