1 . 已知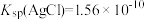 ,
,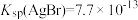 ,
, 。某溶液中含有
。某溶液中含有 、
、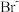 和
和 ,浓度均为0.010
,浓度均为0.010 ,向该溶液中逐滴加入0.010
,向该溶液中逐滴加入0.010 的
的 溶液时,三种阴离子产生沉淀的先后顺序为
溶液时,三种阴离子产生沉淀的先后顺序为
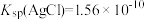 ,
,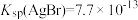 ,
, 。某溶液中含有
。某溶液中含有 、
、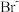 和
和 ,浓度均为0.010
,浓度均为0.010 ,向该溶液中逐滴加入0.010
,向该溶液中逐滴加入0.010 的
的 溶液时,三种阴离子产生沉淀的先后顺序为
溶液时,三种阴离子产生沉淀的先后顺序为A. | B. |
C. | D.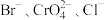 |
您最近一年使用:0次
2023-12-31更新
|
248次组卷
|
100卷引用:江西省靖安中学2020-2021学年高二上学期第二次月考化学试题
江西省靖安中学2020-2021学年高二上学期第二次月考化学试题2013年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅰ卷)(已下线)2013-2014学年湖南省常德市一中高二上学期第二次检测理科化学试卷(已下线)2013-2014重庆市重庆八中下学期高二期中考试化学试卷(已下线)2013-2014福建省安溪八中高二下学期期末考试化学试卷2014-2015河南省濮阳市一中高二上学期第三次质量检测化学试卷2014-2015河南省濮阳市一中高二上学期第三次月考化学试卷2014-2015湖北省武汉华中师大附高二上学期期末化学试卷2014-2015广西桂林市第十八中学高二下学期期中考试化学试卷2015-2016学年山西省太原五中高二上12月月考化学试卷12015-2016学年山西省太原五中高二上12月月考化学试卷22015-2016学年黑龙江省哈尔滨三中高二上期末化学试卷2015-2016学年贵州省凯里一中高二上学期期末化学试卷2015-2016学年宁夏育才中学高二上期末考试化学试卷2016届山东省寿光现代中学高三下学期开学检测化学试卷2016届山东省青岛市高三上学期期末考试化学试卷2015-2016学年湖南省株洲十八中高二上学期期末理化学试卷2015-2016学年福建省龙海市程溪中学高二下学期期中化学试卷2015-2016学年广西桂林十八学高二下期中化学试卷2016-2017学年河北省邯郸一中高二上期中化学卷2016-2017学年宁夏育才中学高二上月考二化学卷22016-2017学年西藏拉萨中学高二上期末化学试卷2016-2017学年河北省张家口市高二上学期期末考试化学试卷2016-2017学年河北省邯郸市高二上学期期末考试化学试卷广西桂林市桂林中学2016-2017学年高二下学期期中考试化学试题四川省成都市双流中学2016-2017学年高二5月月考化学试题内蒙古北京八中乌兰察布分校2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题八对接高考精练--难溶电解质的沉淀溶解平衡福建省福州市第八中学2016-2017学年高二下学期期末考试(理)化学试题河北省定州中学2017-2018学年高二上学期开学考试化学试题贵州省遵义航天高级中学2017-2018学年高二上学期第三次月考理综(理)化学试题天津市静海县第一中学2017-2018学年高二12月学生学业能力调研考试化学试题山西省大同市第一中学2017-2018学年高二上学期期末考试化学试题(已下线)2018年11月15日 《每日一题》人教选修4-溶度积的应用【全国百强校】甘肃省天水市一中2018-2019学年高二(理)上学期第二学段考试化学试题安徽省滁州市定远县民族中学2018-2019学年高二上学期12月月考化学试题内蒙古集宁一中西校区2017-2018学年高二上学期期中考试化学试题云南省保山市第一中学2018-2019学年高二下学期期末化学试题安徽省太和第一中学2019-2020学年高二上学期第一次月考(飞越班)化学试题(已下线)2019年11月14日 《每日一题》人教版(选修4)——溶度积的应用夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——溶度积常数及相关计算(强化练习)重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期10月月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 课时1 沉淀溶解平衡及其应用鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第03章 物质在水溶液中的行为 (B卷能力提升卷) -2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)内蒙古通辽市开鲁县第一中学2021届高三上学期第一次月考化学试题人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 方法帮黑龙江省鹤岗市第一中学2020-2021学年高二10月月考化学试题黑龙江绥化市第一中学2020-2021学年高二上学期第一次月考化学试题 (已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题(已下线)第28讲 难溶电解质的溶解平衡 (精练)-2021年高考化学一轮复习讲练测重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)练习14 难溶电解质的沉淀溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)云南省陆良县2019届高三毕业班第二次教学质量摸底考化学试题山东省德州市2020-2021学年高二上学期反应原理月考(B)化学试题吉林省长春市第二十九中学2020-2021学年高二上学期期末考试化学试题吉林省长春市清蒲中学2020-2021学年度高二上学期期末化学试题甘肃省民勤县第一中学2020-2021学年高二下学期(理)开学考试化学试题山西省潞城第一中学2020-2021学年高二下学期3月月考化学试卷题江苏省盐城市阜宁中学2020-2021学年高二下学期期中考试化学试题云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题四川省绵阳市2020-2021学年高二下学期期末考试化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第24讲 沉淀溶解平衡(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)四川省绵阳市盐亭中学2021-2022学年高二下学期4月月考化学试题四川省遂宁市第二中学校2021-2022学年高二下学期半期考试化学试题(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题湖南省长沙市明德中学2022-2023学年高二上学期期中考试化学试题广东省江门市第一中学2022-2023学年高二上学期第二次月考化学试题(已下线)3.4 沉淀溶解平衡-同步学习必备知识山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题河北省邯郸市永年区第二中学2022-2023学年高二上学期12月月考化学试题黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期期中化学试题黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题广东番禺中学2022-2023学年高二上学期期末测试化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)第2课时 沉淀的溶解与生成、转化及应用第1课时 沉淀溶解平衡与溶度积河南省郑州市宇华实验学校2023-2024学年高三上学期开学(摸底)考试化学试题第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用新疆奎屯市第一高级中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省泸州市合江县马街中学校2023-2024学年高二上学期11月期中化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)陕西省咸阳市武功县普集高级中学2023-2024学年高二上学期12月月考化学试题陕西省汉中市西乡县第一中学2023-2024学年高二上学期12月月考化学试题宁夏石嘴山市第三中学2023-2024学年高二上学期第二次月考化学试题四川省眉山市仁寿县2023-2024学年高二上学期12月联考化学试题河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
10-11高二下·浙江杭州·期中
名校
解题方法
2 . 下列化学原理的应用,可以用沉淀溶解平衡原理来解释的是
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强
②误将钡盐[ 、
、 ]当作食盐食用后,常用0.5%的
]当作食盐食用后,常用0.5%的 溶液解毒
溶液解毒
③石灰岩(喀斯特地貌)溶洞的形成
④ 不能作“钡餐”,而
不能作“钡餐”,而 可以
可以
⑤泡沫灭火器灭火原理
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强
②误将钡盐[
 、
、 ]当作食盐食用后,常用0.5%的
]当作食盐食用后,常用0.5%的 溶液解毒
溶液解毒 ③石灰岩(喀斯特地貌)溶洞的形成
④
 不能作“钡餐”,而
不能作“钡餐”,而 可以
可以 ⑤泡沫灭火器灭火原理
| A.②③④ | B.①②③ | C.③④⑤ | D.①②③④⑤ |
您最近一年使用:0次
2022-04-06更新
|
1220次组卷
|
55卷引用:2010—2011学年浙江省杭州师范大学附属中学高二下学期期中考试化学试卷
(已下线)2010—2011学年浙江省杭州师范大学附属中学高二下学期期中考试化学试卷(已下线)2011-2012年山西省平遥中学高二上学期期中考试化学(理)试卷河北省衡水中学2016-2017学年高一下学期三调考试化学试题吉林省延边第二中学2017-2018学年高二上学期第二次月考化学试题2017-2018学年四川省乐山四校高二第二学期半期联考化学试题【全国百强校】河北省辛集中学2018-2019学年高二上学期期中考试化学试题(已下线)2019年1月7日 《每日一题》人教选修4-沉淀的生成与溶解【全国百强校】河北省冀州市中学2018-2019学年高二上学期第五次月考化学试题2019年10月20日《每日一题》2020年高考化学一轮复习—— 每周一测黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期中考试化学试题北京市2019—2020学年高二上学期期中考试化学试题(选修4人教版)苏教版选修四化学反应原理专题3第四单元 难溶电解质的沉淀溶解平衡 同步检测试卷山西省太原市太原师范学院附属中学2019-2020学年高二上学期12月月考理科化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡湖南省常德市淮阳中学2019-2020学年高二下学期期中考试化学试题(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡原理的应用(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)湖北省武汉市钢城四中2020-2021学年高二上学期期中考试化学试题陕西省宝鸡市宝鸡中学2020-2021学年高二上学期阶段考试(一)化学试题山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题江西省遂川中学2021-2022学年高二上学期第二次月考化学(A卷)试题(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(精讲)-2022年一轮复习讲练测选择性必修1(SJ)专题3第四单元 沉淀溶解平衡课时1 沉淀溶解平衡及其应用(已下线)专题3.4.2 沉淀溶解平衡的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)黑龙江省哈尔滨市第一六二中学2021-2022学年高二上学期期末考试化学试题(已下线)第10练 沉淀溶解平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)黑龙江省大庆中学2021-2022学年高二下学期开学考试化学试题江苏省天一中学2021-2022学年高二上学期期末考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高二下学期开学考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)山西省太原师范学院附属中学2022-2023学年高二上学期12月月考化学试题山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡3.4.1沉淀溶解平衡原理 课后(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)作业(二十一) 沉淀溶解平衡的应用
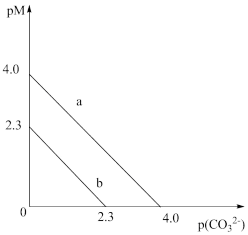
3 . T℃时,两种碳酸盐 (M表示
(M表示 或
或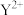 )的沉淀溶解平衡曲线如图所示。已知:
)的沉淀溶解平衡曲线如图所示。已知: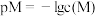 ,
,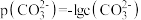 ,
,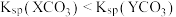 。下列说法正确的是
。下列说法正确的是
 (M表示
(M表示 或
或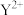 )的沉淀溶解平衡曲线如图所示。已知:
)的沉淀溶解平衡曲线如图所示。已知: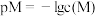 ,
,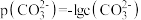 ,
,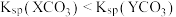 。下列说法正确的是
。下列说法正确的是
A.a表示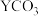 的沉淀溶解平衡曲线 的沉淀溶解平衡曲线 |
B. |
C.T℃时,向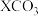 悬浊液中加入饱和 悬浊液中加入饱和 溶液,可能有 溶液,可能有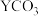 生成 生成 |
D.T℃时,向饱和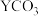 溶液中加入 溶液中加入 溶液,一定能产生 溶液,一定能产生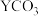 沉淀 沉淀 |
您最近一年使用:0次
2021-12-13更新
|
123次组卷
|
7卷引用:江西省赣县第三中学2020-2021学年高二上学期11月强化训练(三)化学试题
4 . 已知25℃时, 的平衡常数
的平衡常数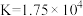 ,
,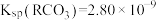 ,下列叙述中正确的是
,下列叙述中正确的是
 的平衡常数
的平衡常数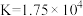 ,
,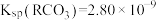 ,下列叙述中正确的是
,下列叙述中正确的是A.25℃时,RSO4的Ksp的为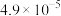 |
B.将浓度均为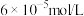 的RCl2、Na2CO3溶液等体积混合后可得到RCO3沉淀 的RCl2、Na2CO3溶液等体积混合后可得到RCO3沉淀 |
C.向c( )=c( )=c( )的混合液中滴加RCl2溶液,首先析出RSO4沉淀 )的混合液中滴加RCl2溶液,首先析出RSO4沉淀 |
| D.相同温度下,RCO3在水中的Ksp大于在Na2CO3溶液中的Ksp |
您最近一年使用:0次
2021-11-16更新
|
1002次组卷
|
16卷引用:江西省新余市第一中学2019-2020学年高二上学期第二次段考试化学试题
江西省新余市第一中学2019-2020学年高二上学期第二次段考试化学试题【全国百强校】湖南省长沙市长郡中学2018届高三高考押题卷(二)理综化学试题(已下线)《考前20天终极攻略》-5月23日 溶液中的离子平衡辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)3.4 难溶电解质的溶解平衡(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)江西省赣州市赣县第三中学2021-2022学年高二上学期12月月考化学试卷辽宁省辽东南协作体2021-2022学年高二上学期期中考试化学试题河北省唐山市第一中学2021-2022学年高二上学期12月月考化学试题(已下线)3.4.2 沉淀溶解平衡的应用(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)第三章 水溶液中的离子反应与平衡(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)作业(二十) 沉淀溶解平衡与溶度积湖南省长沙市第一中学2023-2024学年高二下学期入学考试化学试题
2018高三上·全国·专题练习
名校
5 . 下表是Fe2+、Fe3+、Zn2+被OH-完全沉淀时溶液的pH。某硫酸锌酸性溶液中含有少量Fe2+、Fe3+杂质,为制得纯净的ZnSO4,应加入的试剂是
| 金属离子 | Fe2+ | Fe3+ | Zn2+ |
| 完全沉淀时的pH | 7.7 | 4.5 | 6.5 |
| A.H2O2、ZnO | B.氨水 |
| C.KMnO4、ZnCO3 | D.NaOH溶液 |
您最近一年使用:0次
2021-10-28更新
|
1049次组卷
|
28卷引用:2018年10月12日 《每日一题》一轮复习-盐类水解的应用
(已下线)2018年10月12日 《每日一题》一轮复习-盐类水解的应用陕西省西安中学2019-2020学年高二上学期期末考试化学试题(已下线)第02讲 物质的分离和提纯(精练)——2021年高考化学一轮复习讲练测鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡(已下线)第27讲 盐类水解(精讲)——2021年高考化学一轮复习讲练测黑龙江省哈尔滨市宾县第一中学2020-2021学年高二上学期第三次月考化学试题江西省鹰潭市第一中学2021-2022学年高二上学期创新班10月月考化学试题选择性必修1 专题3素养检测(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时42 盐类的水解影响因素及应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)河北省邯郸市永年区第二中学2021-2022学年高二12月月考化学试题黑龙江省大庆市东风中学2021-2022学年高二下学期开学考试化学试题黑龙江省黑河市五校(嫩江市第一中学,嫩江市职业高中,黑河七中,伊拉哈中学,海江中学)2021-2022学年高二上学期期末联考化学试题(已下线)第23讲 盐类水解 (练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省哈尔滨市宾县第一中学校2021-2022学年高二上学期第二次月考化学试题宁夏贺兰县景博中学2022-2023学年高二上学期第二次月考化学试题北京市清华大学附属中学2022-2023学年高二上学期期末化学试题辽宁省营口市大石桥市第三高级中学等2校2022-2023学年高二上学期期末考试化学试题上海市嘉定区第二中学2022-2023学年高二下学期第一次质量检测化学试题(已下线)第13讲 盐类的水解-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)辽宁省营口市2022-2023学年高二上学期期末考试化学试题辽宁省沈阳市第十中学2021-2022学年高二上学期第一次月考化学试题广东省江门市2023-2024学年高二上学期1月期末考试化学试题北京市第九中学2023-2024学年高二下学期2月开学考化学试题黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第三次考试(期末)化学试卷
名校
解题方法
6 . 下列实验操作能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 制备Fe(OH)3胶体 | 将FeCl3溶液加入稀氨水中并加热煮沸 |
| B | 比较Cu(OH)2、Mg(OH)2溶解度的大小 | 向10mL0.1mol/LNaOH溶液中先加入1mL0.1mol/LMgCl2溶液,再加入1mL0.1mol/LCuCl2溶液 |
| C | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水冲洗 |
| D | 比较碳酸和硅酸的酸性强弱 | 石灰石与浓盐酸混合共热,将所得气体通入硅酸钠溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-09更新
|
196次组卷
|
5卷引用:江西省吉安市第一中学2021-2022学年高二上学期期中考试(理科)化学试题
江西省吉安市第一中学2021-2022学年高二上学期期中考试(理科)化学试题(已下线)2020年海南卷化学高考真题变式题9-14(已下线)2020年海南卷化学高考真题变式题9-14黑龙江省青冈县第一中学校2022届高三上学期第一次模拟考试化学试题吉林省长春市第二十九中学2022届高三上学期第二次质量检测化学试题
名校
解题方法
7 . 氮、磷对水体的污染情况越来越受到人们的重视。回答下列问题:
(1)常温下,在 约为9时,用澄清石灰水可将水体中的
约为9时,用澄清石灰水可将水体中的 转化为
转化为 沉淀除去,该反应的离子方程式为
沉淀除去,该反应的离子方程式为_______ 。
(2)除去地下水中的硝态氮通常用还原剂将其还原为 。
。
①Prusse等提出的用 作催化剂,常温下,在
作催化剂,常温下,在 为4.0~6.0时,可直接用
为4.0~6.0时,可直接用 将
将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。研究发现用 和
和 的混合气体代替
的混合气体代替 ,
, 的去除效果比只用
的去除效果比只用 时更好,其原因是
时更好,其原因是_______ 。
②在 约为5时,用纳米
约为5时,用纳米 粉可将
粉可将 还原为
还原为 ,
, 粉被氧化为
粉被氧化为 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为_______ 。
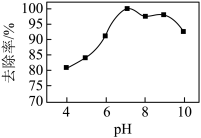
(3)实验测得相同条件下,用次氯酸钠脱除水体中的氨态氮的过程中(
 ),
), 与氨态氮的去除率关系如图所示,在
与氨态氮的去除率关系如图所示,在 大于9时,
大于9时, 越大,去除率越小,其原因是
越大,去除率越小,其原因是_______ 。
(1)常温下,在
 约为9时,用澄清石灰水可将水体中的
约为9时,用澄清石灰水可将水体中的 转化为
转化为 沉淀除去,该反应的离子方程式为
沉淀除去,该反应的离子方程式为(2)除去地下水中的硝态氮通常用还原剂将其还原为
 。
。①Prusse等提出的用
 作催化剂,常温下,在
作催化剂,常温下,在 为4.0~6.0时,可直接用
为4.0~6.0时,可直接用 将
将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为 和
和 的混合气体代替
的混合气体代替 ,
, 的去除效果比只用
的去除效果比只用 时更好,其原因是
时更好,其原因是②在
 约为5时,用纳米
约为5时,用纳米 粉可将
粉可将 还原为
还原为 ,
, 粉被氧化为
粉被氧化为 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为(3)实验测得相同条件下,用次氯酸钠脱除水体中的氨态氮的过程中(

 ),
), 与氨态氮的去除率关系如图所示,在
与氨态氮的去除率关系如图所示,在 大于9时,
大于9时, 越大,去除率越小,其原因是
越大,去除率越小,其原因是
您最近一年使用:0次
2021-09-14更新
|
395次组卷
|
10卷引用:山东省临沂市第一中学2020届高三10月月考化学试题
山东省临沂市第一中学2020届高三10月月考化学试题2019年湖北省黄冈市高三11月新高考备考监测联考化学试题山东省新高考备考监测2020届高三10月联考化学试题(已下线)考点11 弱电解质的电离及溶液pH-2020年高考化学命题预测与模拟试题分类精编江西省丰城市第九中学2022-2023学年高三上学期摸底考(日新班)化学试题广东省普通高中2022届高三9月阶段性质量检测化学试题(已下线)第14周 周测卷-备战2022年高考化学周测与晚练(新高考专用)吉林省长春吉大附中实验学校2021-2022学年高三上学期第三次摸底考试化学试题黑龙江省牡丹江市第二高级中学2022-2023学年高三上学期第三次月考化学试题(已下线)第3讲 氧化还原反应
名校
解题方法
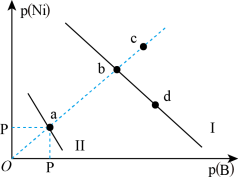
8 . 已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;p(Ni)=-lgc(Ni2+),p(B)=-lgc(S2-)或-lgc(CO )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
 )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
| A.常温下NiCO3的溶解度大于NiS的溶解度 |
| B.向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动 |
| C.对于曲线Ⅰ,在b点加热,b点向c点移动 |
D.P为3.5且对应的阴离子是CO |
您最近一年使用:0次
2021-09-05更新
|
3068次组卷
|
42卷引用:【全国市级联考】江西省南昌市2018届高三第三次模拟考试理综化学试题
【全国市级联考】江西省南昌市2018届高三第三次模拟考试理综化学试题四川省资阳市高中2018届高三第二次诊断性考试理科综合化学试题西北师大附中2018届下学期高三年级第二次模拟理综化学试卷西藏自治区拉萨中学2018届高三第七次月考理综化学试题【全国市级联考】河北省保定市2018届高三第二次模拟考试理科综合化学试题【全国百强校】广东省阳春市第一中学2018届高三第九次月考理综化学试题【市级联考】湖北省十堰市2019届高三下学期模拟化学试题四川省泸县第四中学2019届高三下学期三诊模拟理科综合化学试题辽宁省六校协作体2020届高三上学期期中考试化学试题步步为赢 高二化学寒假作业:综合检测(一)福建省厦门外国语学校2020届高三12月月考化学试题2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】吉林省梅河口市第五中学2020届高三下学期模拟考试化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编鲁科版(2019)选择性必修1化学反应原理 综合训练高中必刷题高二选择性必修1化学反应原理综合训练(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)第三章 水溶液中的离子平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过素养 学科素养拓展训练人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 过素养 学科素养拓展训练山东省临朐县实验中学2020-2021学年高二上学期12月月结学情检测化学试题江西省九江市第一中学2021-2022学年高二上学期第二次月考化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)选择性必修1(SJ)专题3专题培优专练选择性必修1 化学反应原理综合训练(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)3.4.2 沉淀溶解平衡原理的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2021年高考全国乙卷化学试题变式题陕西省宝鸡市陈仓区2022届高三上学期第一次教学质量检测化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)湖南省株洲市第一中学2021-2022学年高三下学期期中考试化学试题陕西省汉中中学2021-2022学年高二上学期第四次月考化学试题吉林省长春市第五中学2022-2023学年高二上学期期中考试化学试题湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)T13-溶液中的离子平衡浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题
9 . 已知表数据:
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH | 9.6 | 6.4 | 3.4 |
| A.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀 |
B.该溶液中c(SO ):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4 ):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4 |
| C.向该溶液中加入适量氯水,并调节pH到3.4后过滤,可获得纯净的CuSO4溶液 |
| D.在pH=5的溶液中Fe3+不能大量存在 |
您最近一年使用:0次
2021-09-03更新
|
438次组卷
|
8卷引用:2016-2017学年江西省宜春市奉新一中高二上月考二化学卷
2016-2017学年江西省宜春市奉新一中高二上月考二化学卷2016届辽宁省东北育才学校高三上学期第二次模拟测试化学试卷黑龙江省哈尔滨市第三中学2018届高三第三次验收考试化学试题河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)选择性必修1 综合检测(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)浙江省温州市2021-2022学年高二上学期12月普通高中学考适应性测试化学试题(已下线)第22讲 沉淀溶解平衡的应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
解题方法
10 . 某探究小组设计如下线路处理废液和资源回收:
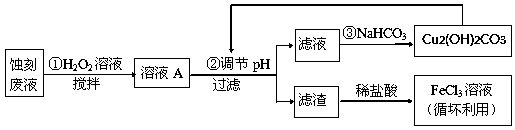
(1)用少量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:___________ 。
(2)FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:___________ 。
(3)步骤①中加入H2O2溶液的目的是:___________ 。
(4)已知:生成氢氧化物沉淀的pH
根据表中数据推测调节pH的范围是:___________ 。
(5)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:___________ ,该过程中调节溶液的pH为5,则c(Fe3+)为:___________ mol·L-1.(已知:Ksp[Fe(OH)3]= 3.80×10-38)

(1)用少量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:
(2)FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:
(3)步骤①中加入H2O2溶液的目的是:
(4)已知:生成氢氧化物沉淀的pH
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.3 |
根据表中数据推测调节pH的范围是:
(5)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:
您最近一年使用:0次



