解题方法
1 . Ⅰ.在0.1 mol·L-1的重铬酸钾(K2Cr2O7)溶液中存在如下平衡:
Cr2O +H2O
+H2O 2HCrO4
2HCrO4 2CrO
2CrO +2H+
+2H+
(1)在强碱溶液中,铬元素的主要存在形式为_______ (填离子符号),向重铬酸钾溶液中加入适量稀硫酸,溶液中c(Cr2O )/c(CrO
)/c(CrO )将
)将_______ (填“增大”、“减小”或“不变”)。
Ⅱ.已知某溶液中只存在OH-、H+、NH 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH )>c(H+)>c(OH-) ②c(Cl-)>c(NH
)>c(H+)>c(OH-) ②c(Cl-)>c(NH )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c(NH )>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH
)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)
(2)若溶液中只溶解了一种溶质,则该溶质是_______ ,上述四种离子浓度的大小顺序为_______ (选填序号)。
(3)若上述关系中③是正确的,则溶液中的溶质为_______ ;
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______ c(NH3·H2O) (填“大于”“小于”或“等于”)。
III.重金属离子对河流造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(5)你认为往废水中投入_______(填字母序号),沉淀效果最好。
(6)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=_______ 。
Cr2O
 +H2O
+H2O 2HCrO4
2HCrO4 2CrO
2CrO +2H+
+2H+(1)在强碱溶液中,铬元素的主要存在形式为
 )/c(CrO
)/c(CrO )将
)将Ⅱ.已知某溶液中只存在OH-、H+、NH
 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:①c(Cl-)>c(NH
 )>c(H+)>c(OH-) ②c(Cl-)>c(NH
)>c(H+)>c(OH-) ②c(Cl-)>c(NH )>c(OH-)>c(H+)
)>c(OH-)>c(H+)③c(NH
 )>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH
)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)(2)若溶液中只溶解了一种溶质,则该溶质是
(3)若上述关系中③是正确的,则溶液中的溶质为
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
III.重金属离子对河流造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
| A.NaOH | B.Na2S | C.KI | D.Ca(OH)2 |
您最近一年使用:0次
2 . 回答下列问题:
(1)氯化铁水溶液呈酸性,原因是(用离子方程式表示 ) ___________ 。
(2)电离平衡常数可用来衡量弱电解质的电离程度。已知如下表数据( )
)
①25℃时,等物质的量浓度的3种溶液:a.NaCN溶液b.Na2CO3溶液c.CH3COONa溶液,其pH由大到小的顺序为___________ (填序号 ) 。
②25℃时,向 溶液中通入少量的
溶液中通入少量的 ,发生反应的
,发生反应的离子方程式为 ___________ 。
(3)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
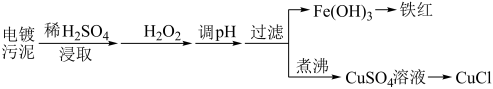
①酸浸后加入 的目的是
的目的是___________ ,调 的最适宜范围为
的最适宜范围为___________ 。
②调pH过程中加入的试剂最好是___________ 。
A.NaOH B.CuO C.NH3⋅H2O D.Cu2(OH)2CO3
③向 溶液中加入一定量的
溶液中加入一定量的 、
、 ,可以生成白色的
,可以生成白色的 沉淀,反应的化学方程式
沉淀,反应的化学方程式___ 。
(1)氯化铁水溶液呈酸性,原因是(
(2)电离平衡常数可用来衡量弱电解质的电离程度。已知如下表数据(
 )
)| 化学式 |  |  |  |
| 电离平衡常数 | 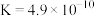 |  | 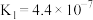  |
②25℃时,向
 溶液中通入少量的
溶液中通入少量的 ,发生反应的
,发生反应的(3)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
 的目的是
的目的是 的最适宜范围为
的最适宜范围为②调pH过程中加入的试剂最好是
A.NaOH B.CuO C.NH3⋅H2O D.Cu2(OH)2CO3
③向
 溶液中加入一定量的
溶液中加入一定量的 、
、 ,可以生成白色的
,可以生成白色的 沉淀,反应的化学方程式
沉淀,反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式正确 的是
A.往 溶液中滴加 溶液中滴加 溶液: 溶液: |
B.氢氧化铁溶于氢碘酸中: |
C.向 溶液中加入足量 溶液中加入足量 溶液:Mg(HCO3)2+2OH-=MgCO3↓+CO 溶液:Mg(HCO3)2+2OH-=MgCO3↓+CO +2H2O +2H2O |
D.往 中加入饱和 中加入饱和 溶液:CO 溶液:CO +BaSO4=BaCO3+SO +BaSO4=BaCO3+SO |
您最近一年使用:0次
2022-05-18更新
|
50次组卷
|
4卷引用:江西省赣州市赣县第三中学2021-2022学年高二上学期12月月考化学试卷
4 . 已知常温下 ,
,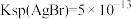 ,下列有关说法不正确的是
,下列有关说法不正确的是
 ,
,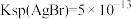 ,下列有关说法不正确的是
,下列有关说法不正确的是| A.在饱和AgCl、AgBr的混合溶液中: c(Cl-): c(Br-)=360 |
| B.AgCl在水中溶解度及Ksp均比在NaCl溶液中的小 |
| C.向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀 |
| D.在含有AgCl、AgBr固体悬浊液中加入少量NaBr固体,c(Cl-)增大 |
您最近一年使用:0次
名校
5 . 化学与社会、生产、生活密切相关,下列说法不正确的是
| A.可先用纯碱溶液处理锅炉水垢中的CaSO4 |
| B.在环保领域,碱性废水可利用烟道气中和 |
| C.生活中使用的泡沫灭火器是利用了硫酸铝和碳酸钠溶液水解的性质 |
| D.实验中常将FeCl3晶体溶于较浓盐酸中配制FeCl3溶液 |
您最近一年使用:0次
2022-04-09更新
|
62次组卷
|
2卷引用:江西省山江湖协作体2021-2022学年高二上学期联考(统招班)化学试题
名校
解题方法
6 . 下列化学原理的应用,可以用沉淀溶解平衡原理来解释的是
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强
②误将钡盐[ 、
、 ]当作食盐食用后,常用0.5%的
]当作食盐食用后,常用0.5%的 溶液解毒
溶液解毒
③石灰岩(喀斯特地貌)溶洞的形成
④ 不能作“钡餐”,而
不能作“钡餐”,而 可以
可以
⑤泡沫灭火器灭火原理
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强
②误将钡盐[
 、
、 ]当作食盐食用后,常用0.5%的
]当作食盐食用后,常用0.5%的 溶液解毒
溶液解毒 ③石灰岩(喀斯特地貌)溶洞的形成
④
 不能作“钡餐”,而
不能作“钡餐”,而 可以
可以 ⑤泡沫灭火器灭火原理
| A.②③④ | B.①②③ | C.③④⑤ | D.①②③④⑤ |
您最近一年使用:0次
2022-04-06更新
|
1220次组卷
|
55卷引用:江西省遂川中学2021-2022学年高二上学期第二次月考化学(A卷)试题
江西省遂川中学2021-2022学年高二上学期第二次月考化学(A卷)试题(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(精讲)-2022年一轮复习讲练测选择性必修1(SJ)专题3第四单元 沉淀溶解平衡课时1 沉淀溶解平衡及其应用(已下线)专题3.4.2 沉淀溶解平衡的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题(已下线)2010—2011学年浙江省杭州师范大学附属中学高二下学期期中考试化学试卷(已下线)2011-2012年山西省平遥中学高二上学期期中考试化学(理)试卷河北省衡水中学2016-2017学年高一下学期三调考试化学试题吉林省延边第二中学2017-2018学年高二上学期第二次月考化学试题2017-2018学年四川省乐山四校高二第二学期半期联考化学试题【全国百强校】河北省辛集中学2018-2019学年高二上学期期中考试化学试题(已下线)2019年1月7日 《每日一题》人教选修4-沉淀的生成与溶解【全国百强校】河北省冀州市中学2018-2019学年高二上学期第五次月考化学试题2019年10月20日《每日一题》2020年高考化学一轮复习—— 每周一测黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期中考试化学试题北京市2019—2020学年高二上学期期中考试化学试题(选修4人教版)苏教版选修四化学反应原理专题3第四单元 难溶电解质的沉淀溶解平衡 同步检测试卷山西省太原市太原师范学院附属中学2019-2020学年高二上学期12月月考理科化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡湖南省常德市淮阳中学2019-2020学年高二下学期期中考试化学试题(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡原理的应用(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)湖北省武汉市钢城四中2020-2021学年高二上学期期中考试化学试题陕西省宝鸡市宝鸡中学2020-2021学年高二上学期阶段考试(一)化学试题山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高二上学期期末考试化学试题(已下线)第10练 沉淀溶解平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)黑龙江省大庆中学2021-2022学年高二下学期开学考试化学试题江苏省天一中学2021-2022学年高二上学期期末考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高二下学期开学考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第三章 水溶液中的离子反应与平衡(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)山西省太原师范学院附属中学2022-2023学年高二上学期12月月考化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡3.4.1沉淀溶解平衡原理 课后(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)作业(二十一) 沉淀溶解平衡的应用
7 . 关于沉淀溶解平衡和溶度积常数,下列说法不正确的是
| A.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| B.已知25℃时Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=4.0×104 |
| C.将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]>Ksp(CaSO4) |
| D.已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水调混合液的pH=11,产生沉淀,则此时溶液中的c(Mg2+)=1.8×10-5mol·L-1 |
您最近一年使用:0次
2022-03-10更新
|
487次组卷
|
3卷引用:江西省抚州市南城县第二中学2021-2022年高二上学期第二次月考化学试题
名校
解题方法
8 . 下列方程式书写正确的是
A. 的水解方程式: 的水解方程式: +2H2O⇌H2CO3+2OH- +2H2O⇌H2CO3+2OH- |
B.CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+ (aq) (aq) |
C.NaHSO4在熔融状态下的电离方程式:NaHSO4=Na++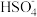 |
D.H2SO4溶液与NaOH溶液发生中和反应的热化学方程式为 已知H2SO4溶液与NaOH溶液发生反应的中和热为57.3kJ/mol:H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq) △H=-57.3kJ/mol 已知H2SO4溶液与NaOH溶液发生反应的中和热为57.3kJ/mol:H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq) △H=-57.3kJ/mol |
您最近一年使用:0次
名校
解题方法
9 . 下列实验操作、实验现象、解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 向盛有 溶液的试管中滴加 溶液的试管中滴加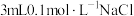 溶液,再向其中滴加一定量 溶液,再向其中滴加一定量 溶液 溶液 | 先有白色沉淀生成,后又产生黄色沉淀 | 常温下,溶度积: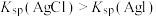 |
| B | 常温下,用 计分别测定 计分别测定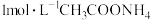 溶液和 溶液和 溶液的 溶液的 | 测得 都等于7 都等于7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| C | 用 试纸测相同浓度的 试纸测相同浓度的 溶液、 溶液、 溶液的 溶液的 |  溶液的 溶液的 约为9, 约为9, 溶液的 溶液的 约为8 约为8 |  的酸性比 的酸性比 强 强 |
| D | 向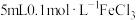 溶液中滴加 溶液中滴加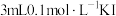 溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴 溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴 溶液 溶液 | 溶液变红 |  与 与 的反应为可逆反应 的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 锌灰是热镀锌厂和电解锌厂在生产过程中产生的一种副产品,主要成分是氧化锌和金属锌,杂质为PbO、FeO、Fe3O4、Cu等。利用锌灰生产皓矾(ZnSO4·7H2O)和ZnO等化工产品的工艺流程之一如下:
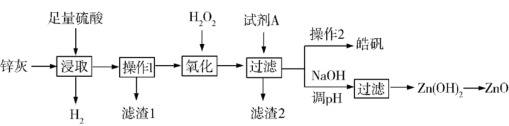
已知pH>11.5时,Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH:
请回答下列问题:
(1)“滤渣1”的主要成分是___________ 。
(2)加入过量H2O2的目的是___________ (结合离子方程式回答),除去剩余H2O2的简便方法是___________ 。
(3)“试剂A”最好是下列物质中的___________。
(4)“操作2”包括蒸发浓缩、___________ 、过滤洗涤。
(5)加NaOH调pH时,应该控制的pH范围是___________ 。

已知pH>11.5时,Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH:
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.5 | 3.2 |
| Fe2+ | 6.5 | 9.0 |
| Zn2+ | 5.6 | 8.1 |
| Pb2+ | 6.6 | 9.1 |
请回答下列问题:
(1)“滤渣1”的主要成分是
(2)加入过量H2O2的目的是
(3)“试剂A”最好是下列物质中的___________。
| A.NH3·H2O | B.Zn | C.NaOH | D.ZnCO3 |
(5)加NaOH调pH时,应该控制的pH范围是
您最近一年使用:0次
2021-12-31更新
|
194次组卷
|
2卷引用:江西省赣州市教育发展联盟2021-2022学年高二上学期第7次联考化学试题



