1 . 利用水钴矿(主要成分为 ,含少量
,含少量 、
、 、MnO、MgO、CaO、
、MnO、MgO、CaO、 等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备工艺流程。
等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备工艺流程。
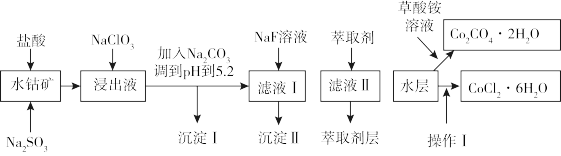
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“浸出”过程中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2) 在浸出液中发生反应的离子方程式为
在浸出液中发生反应的离子方程式为_______ 。
(3)加入 调pH至5.2,目的是
调pH至5.2,目的是_______ ;加萃取剂的目的是除去锰元素,则沉淀Ⅱ的主要成分为_______ (填化学式)。
(4)“操作Ⅰ”包括:将水层加入浓盐酸调整pH为2〜3,_______ 、_______ 、过滤、洗涤、减压烘干等过程。
(5)将5.49g草酸钴晶体( )置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
经测定,整个受热过程,只产生水蒸气和 气体,则在290〜320℃温度范围,剩余固体物质的化学式为
气体,则在290〜320℃温度范围,剩余固体物质的化学式为_______ 。(已知: 的摩尔质量为
的摩尔质量为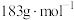 )
)
 ,含少量
,含少量 、
、 、MnO、MgO、CaO、
、MnO、MgO、CaO、 等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备工艺流程。
等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备工艺流程。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |  |
| 开始沉淀pH | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀pH | 3.7 | 9. 6 | 9.2 | 5.2 | 9.8 |
(1)“浸出”过程中
 发生反应的离子方程式为
发生反应的离子方程式为(2)
 在浸出液中发生反应的离子方程式为
在浸出液中发生反应的离子方程式为(3)加入
 调pH至5.2,目的是
调pH至5.2,目的是(4)“操作Ⅰ”包括:将水层加入浓盐酸调整pH为2〜3,
(5)将5.49g草酸钴晶体(
 )置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。| 温度范围/℃ | 固体质量/g |
| 150〜210 | 4.41 |
| 290〜320 | 2.41 |
 气体,则在290〜320℃温度范围,剩余固体物质的化学式为
气体,则在290〜320℃温度范围,剩余固体物质的化学式为 的摩尔质量为
的摩尔质量为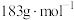 )
)
您最近一年使用:0次
2 . 测定水样中 浓度的实验步骤如下:
浓度的实验步骤如下:
①向锥形瓶中加入25.00mL处理后的水样,加入几滴 溶液;
溶液;
②加入 溶液(过量),充分摇匀;
溶液(过量),充分摇匀;
③用 标准溶液进行滴定,至终点时消耗标准溶液
标准溶液进行滴定,至终点时消耗标准溶液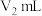 。
。
已知: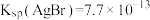 ;
; (白色),
(白色),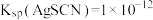 。下列说法错误的是
。下列说法错误的是
 浓度的实验步骤如下:
浓度的实验步骤如下:①向锥形瓶中加入25.00mL处理后的水样,加入几滴
 溶液;
溶液;②加入
 溶液(过量),充分摇匀;
溶液(过量),充分摇匀;③用
 标准溶液进行滴定,至终点时消耗标准溶液
标准溶液进行滴定,至终点时消耗标准溶液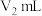 。
。已知:
 ;
; (白色),
(白色),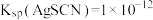 。下列说法错误的是
。下列说法错误的是| A.到达滴定终点时,溶液变为红色 |
| B.该滴定法需在酸性条件下进行 |
C.根据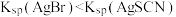 可知,反应 可知,反应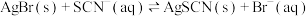 不能发生 不能发生 |
D.该水样中 的浓度 的浓度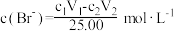 |
您最近一年使用:0次
解题方法
3 . 下列指定反应的离子方程式正确的是
A.向 溶液中通入过量 溶液中通入过量 : : |
B.酸化 和 和 的混合溶液: 的混合溶液: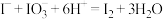 |
C.氧化亚铁溶于稀硝酸: |
D.氢氧化镁溶于氯化铵溶液: |
您最近一年使用:0次
4 . 下列实验操作、现象能得出相应结论的是
| 编号 | 实验操作 | 现象 | 结论 |
| A | 将少量Zn片放入FeCl3溶液中 | Zn片逐渐溶解,溶液由黄色逐渐变浅绿色 | 证明Zn的金属性比Fe强 |
| B | 取少量待测液于试管中,先加盐酸酸化,再加 溶液 溶液 | 先无明显现象,后有白色沉淀产生 | 原溶液中一定含有 |
| C | 向 溶液中滴入5滴同浓度 溶液中滴入5滴同浓度 溶液后再滴入5滴同浓度 溶液后再滴入5滴同浓度 溶液 溶液 | 先出现白色沉淀,后出现红褐色沉淀 |  |
| D | 向某钾盐中滴加浓盐酸 | 产生的气体可以使品红溶液褪色 | 该钾盐为 或 或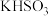 或二者的混合物 或二者的混合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-23更新
|
343次组卷
|
2卷引用:江西省鹰潭市2022届高三下学期第一次模拟考试理科综合化学试题
名校
5 . 下列装置或操作不能达到目的的是

| A.①:制取无水MgCl2 | B.②:测定锌与稀硫酸反应的速率 |
| C.③:验证AgCl和AgI的Ksp大小 | D.④:研究浓度对反应速率的影响 |
您最近一年使用:0次
2022-01-23更新
|
467次组卷
|
6卷引用:江西省上饶市第一中学2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
6 . 一定温度下,两种碳酸盐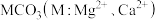 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
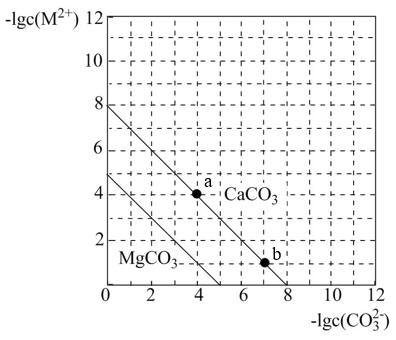
注: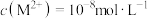 时,
时,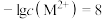 ;
;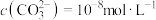 时。
时。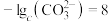
下列说法不正确 的是
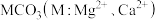 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
注:
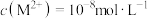 时,
时,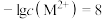 ;
;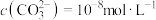 时。
时。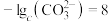
下列说法
A.该温度下, 的 的 |
B.该温度下,溶解度: |
C.欲使a点移动到b点,可向 浊液中加入适量 浊液中加入适量 固体 固体 |
D.反应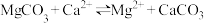 ,正向转化比逆向转化更难实现 ,正向转化比逆向转化更难实现 |
您最近一年使用:0次
2022-01-21更新
|
357次组卷
|
4卷引用:江西省赣州市赣县第三中学2021-2022学年高二下学期开学考试化学试卷
7 . 能正确表示下列变化的离子方程式是
| A.AgCl悬浊液中滴入Na2S溶液:2Ag++S2-=Ag2S↓ |
B.氢氧化钡溶液中滴加少量硫酸氢钠溶液:Ba2++2OH-+2H++ =BaSO4↓+2H2O =BaSO4↓+2H2O |
C.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3 =Al2(CO3)3↓ =Al2(CO3)3↓ |
| D.将标准状况下的22.4LCl2通入含2molFeI2的FeI2溶液中:Cl2+2I-=2Cl-+I2 |
您最近一年使用:0次
8 . 请回答下列问题:
(1)84消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈___________ 性(填“酸”“碱”或“中”),原因可用离子方程式表示为___________ 。
(2)常温下,某柠檬水的pH为3,则其中的c(OH-)为___________ 。
(3)浓度均为0.1mol/L的盐酸、硫酸和醋酸,其中pH最小的是___________ 。
(4)在某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则c(Ba2+)___________ (填“增大”“减小”或“不变”,下同),Ksp___________ 。
(1)84消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈
(2)常温下,某柠檬水的pH为3,则其中的c(OH-)为
(3)浓度均为0.1mol/L的盐酸、硫酸和醋酸,其中pH最小的是
(4)在某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则c(Ba2+)
您最近一年使用:0次
9 . 下列实验操作能达到实验目的的是
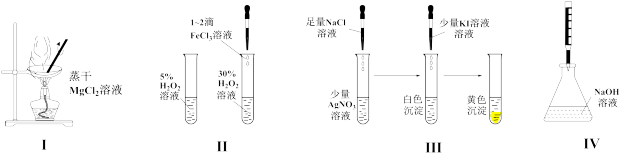

| A.装置I:从MgCl2溶液中提取MgCl2·6H2O固体 |
| B.装置II:探究催化剂对化学反应速率的影响 |
| C.装置III:验证AgCl和AgI的Ksp大小 |
| D.装置IV:用标准盐酸溶液滴定NaOH溶液的浓度 |
您最近一年使用:0次
2021-12-19更新
|
378次组卷
|
4卷引用:江西省宜春市铜鼓中学2021-2022学年高二下学期第一次月考(实验班)化学试卷
名校
10 . 某科研人员以废镍催化剂(主要成分为 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
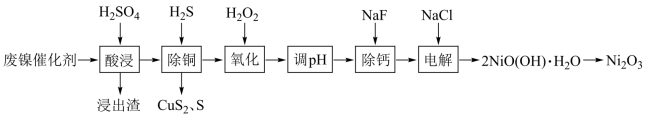
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的 如表:
如表:
回答下列问题:
(1)浸出渣主要成分为___________ 、___________ (填化学式)。
(2)“除铜”时, 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)“氧化”的目的是将溶液中的 氧化为
氧化为 ,温度需控制在
,温度需控制在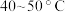 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是___________ 。
(4)“调 ”时,
”时, 的控制范围为
的控制范围为___________ 。
(5)“除钙”后,若溶液中 浓度为
浓度为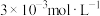 ,则
,则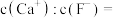
___________ 。[已知常温下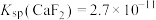 ]
]
 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的
 如表:
如表: |  |  |
| 1.5 | 6.5 | 7.7 |
| 3.7 | 9.7 | 9.2 |
回答下列问题:
(1)浸出渣主要成分为
(2)“除铜”时,
 与
与 反应的离子方程式为
反应的离子方程式为(3)“氧化”的目的是将溶液中的
 氧化为
氧化为 ,温度需控制在
,温度需控制在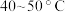 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是(4)“调
 ”时,
”时, 的控制范围为
的控制范围为(5)“除钙”后,若溶液中
 浓度为
浓度为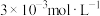 ,则
,则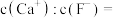
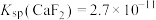 ]
]
您最近一年使用:0次
2021-12-09更新
|
982次组卷
|
4卷引用:江西省六校2021-2022学年高二上学期期末联考化学试题



