1 . 氨是重要的基础化工原料,工业上常用于制备氨水、亚硝酸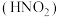 、连二次硝酸
、连二次硝酸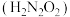 、尿素
、尿素 等多种含氮的化工产品。
等多种含氮的化工产品。
(1)已知: 时,连二次硝酸
时,连二次硝酸 的电离常数为
的电离常数为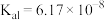 、
、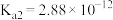 ;往
;往 溶液中滴加氢氧化钠溶液至
溶液中滴加氢氧化钠溶液至 ,
, 、
、 、离子浓度由大到小的顺序为
、离子浓度由大到小的顺序为___________ 。
(2)常温下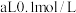 的
的 和
和 的
的 混合,混合后溶液呈中性,
混合,混合后溶液呈中性, 的电离常数为
的电离常数为___________ (用含a、b的式子表示)
(3)向浓度均为 的
的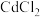 和
和 混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中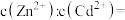
___________ 。[已知: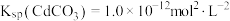 ,
,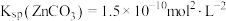 ]
]
可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。
(4)羟基磷灰石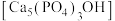 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: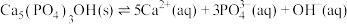 。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:___________
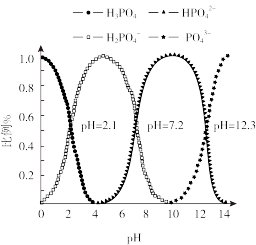
(5)常温下,向磷酸溶液中滴加 溶液,含磷微粒的分布比例与
溶液,含磷微粒的分布比例与 的关系如图所示。
的关系如图所示。 溶液显酸性,下列有关分析正确的是___________。
溶液显酸性,下列有关分析正确的是___________。
(6)联氨(又称联肼, 无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为:
无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为:____________ 平衡常数值为___________ (已知: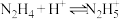 的
的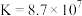 ;
;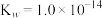 )。
)。
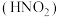 、连二次硝酸
、连二次硝酸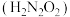 、尿素
、尿素 等多种含氮的化工产品。
等多种含氮的化工产品。(1)已知:
 时,连二次硝酸
时,连二次硝酸 的电离常数为
的电离常数为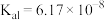 、
、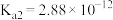 ;往
;往 溶液中滴加氢氧化钠溶液至
溶液中滴加氢氧化钠溶液至 ,
, 、
、 、离子浓度由大到小的顺序为
、离子浓度由大到小的顺序为(2)常温下
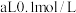 的
的 和
和 的
的 混合,混合后溶液呈中性,
混合,混合后溶液呈中性, 的电离常数为
的电离常数为(3)向浓度均为
 的
的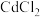 和
和 混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中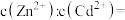
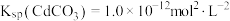 ,
,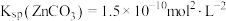 ]
]可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为
 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。(4)羟基磷灰石
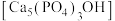 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: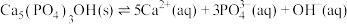 。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:(5)常温下,向磷酸溶液中滴加
 溶液,含磷微粒的分布比例与
溶液,含磷微粒的分布比例与 的关系如图所示。
的关系如图所示。 溶液显酸性,下列有关分析正确的是___________。
溶液显酸性,下列有关分析正确的是___________。
A.溶液中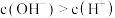 |
B. 的电离程度大于其水解程度 的电离程度大于其水解程度 |
C. c(Na+)+ c(H+)=c(H2PO )+2c(HPO )+2c(HPO )+3c(PO )+3c(PO )+c(OH—) )+c(OH—) |
| D.溶液中水的电离程度比纯水大 |
(6)联氨(又称联肼,
 无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为:
无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为: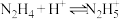 的
的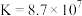 ;
;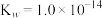 )。
)。
您最近一年使用:0次
名校
解题方法
2 . 化学与社会、生活密切相关。下列说法不正确的是
A.锅炉水垢中含有的 ,可先用 ,可先用 溶液处理,后用酸除去 溶液处理,后用酸除去 |
B.用 作沉淀剂,除去水中的 作沉淀剂,除去水中的 和 和 |
| C.疫苗一般应冷藏存放,以减小蛋白质变性的速率。 |
| D.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可改变产生尾气的反应方向 |
您最近一年使用:0次
3 . 常温下,Ksp(MnS)=2.5×10-13,Ksp(FeS)=6.3×10-18。FeS和MnS在水中的沉淀溶解平衡曲线如图所示(X2+表示Fe2+或Mn2+),下列说法错误的是

| A.曲线Ⅱ表示MnS的沉淀溶解平衡曲线 |
| B.升高温度,曲线Ⅱ上的c点可沿虚线平移至e点 |
C.常温下,反应MnS(s)+Fe2+(aq) FeS(s)+Mn2+(aq)的平衡常数K≈4×104 FeS(s)+Mn2+(aq)的平衡常数K≈4×104 |
| D.向b点溶液中加入少量Na2S固体,溶液组成由b点沿Ⅰ线向a点方向移动 |
您最近一年使用:0次
2022-03-29更新
|
716次组卷
|
7卷引用:江西省宜春市铜鼓中学2021-2022学年高二下学期开学考化学试题
名校
4 . 室温下进行下列实验,根据实验操作和现象,所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 乙醇钠的水溶液呈强碱性 | C2H5O-结合H+的能力强 |
| B | 将某黄色溶液滴在KI淀粉试纸上,试纸变蓝 | 原溶液中一定含有Cl2 |
| C | 分别向等物质的量浓度的苯酚钠溶液和碳酸钠溶液中滴加酚酞,后者红色更深 | 酸性:碳酸强于苯酚 |
| D | 向盛有2mL一定浓度的Na3[Ag(S2O3)2]溶液的试管中,滴入5滴2mol•L-1的KI溶液,产生黄色沉淀 | [Ag(S2O3)2]3-具有较强的还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 某NiO的废料中有FeO、CuO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4和Ni的流程如下:

已知:有关金属离子生成氢氧化物沉淀所需的pH如下表:
(1)滤渣1的主要成分为_______ 。
(2)从滤液2中获得NiSO4∙6H2O的实验操作_______ 、_______ 、过滤、洗涤、干燥。
(3)用离子方程式解释加入H2O2的作用______ 。
(4)加NiO调节溶液的pH至3.2,则生成沉淀的离子方程式_______ 。
(5)电解浓缩后的滤液2可获得金属镍,其基本反应原理如图:

若一段时间后,在A、B两极均收集到11.2L气体(标准状况下),能得到Ni______ g。

已知:有关金属离子生成氢氧化物沉淀所需的pH如下表:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀时pH | 1.5 | 3.6 | 7.3 | 7.0 | 9.6 |
| 完全沉淀时pH | 3.8 | 4.7 | 9.3 | 9.0 | 12.0 |
(1)滤渣1的主要成分为
(2)从滤液2中获得NiSO4∙6H2O的实验操作
(3)用离子方程式解释加入H2O2的作用
(4)加NiO调节溶液的pH至3.2,则生成沉淀的离子方程式
(5)电解浓缩后的滤液2可获得金属镍,其基本反应原理如图:

若一段时间后,在A、B两极均收集到11.2L气体(标准状况下),能得到Ni
您最近一年使用:0次
6 . 碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(主要含有SrCO3及少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如图所示。
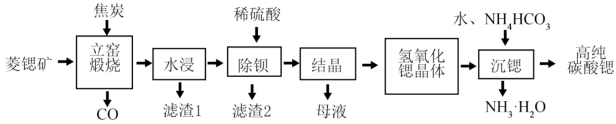
已知:①不溶性碳酸盐高温下分解,生成金属氧化物和CO2,可溶性碳酸盐高温不分解。
②298K时,Ksp[SrCO3]=5.6×10-10、Ksp[CaCO3]=3.36×10-9
③Sr(OH)2在水中的溶解度数据如表:
回答下列问题:
(1)SrCO3中Sr的化合价____ 。
(2)向“立窑煅烧”中投料前,将菱锶矿、焦炭混合粉碎的目的是____ (任写两点)。
(3)“水浸”中用____ (填“冷水”、“热水”),“滤渣1”中含有焦炭、MgO和____ (填化学式)。
(4)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为____ 。
(5)“沉锶”中反应的化学方程式为____ 。
(6)计算298K时,反应CaCO3(s)+Sr2+(aq) SrCO3(s)+Ca2+(aq)平衡常数的数值是
SrCO3(s)+Ca2+(aq)平衡常数的数值是____ 。

已知:①不溶性碳酸盐高温下分解,生成金属氧化物和CO2,可溶性碳酸盐高温不分解。
②298K时,Ksp[SrCO3]=5.6×10-10、Ksp[CaCO3]=3.36×10-9
③Sr(OH)2在水中的溶解度数据如表:
| 温度/℃ | 10 | 60 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 8.42 | 44.5 | 91.2 |
回答下列问题:
(1)SrCO3中Sr的化合价
(2)向“立窑煅烧”中投料前,将菱锶矿、焦炭混合粉碎的目的是
(3)“水浸”中用
(4)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
(5)“沉锶”中反应的化学方程式为
(6)计算298K时,反应CaCO3(s)+Sr2+(aq)
 SrCO3(s)+Ca2+(aq)平衡常数的数值是
SrCO3(s)+Ca2+(aq)平衡常数的数值是
您最近一年使用:0次
7 . 通过下列实验操作和实验现象,得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将丙烯通入碘水中 | 碘水褪色 | 丙烯与碘发生加成反应 |
| B | 向FeSO4溶液中滴加苯酚稀溶液 | 溶液未变紫色 | FeSO4溶液未变质 |
| C | 向待测溶液中滴加淀粉溶液,再滴加新制氯水 | 先无明显变化,后溶液变蓝色 | 待测溶液中存在I- |
| D | 向2mL0.1mol·L-1AgNO3溶液中滴加3滴相同浓度的NaCl溶液,然后再滴加3滴相同浓度的KI溶液 | 先产生白色沉淀,然后产生黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 表中实验操作、现象与结论对应关系均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY强 |
| B | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测得pH=3.2 | NaHSO3溶液呈酸性,证明HSO 在水中的电离程度小于水解程度 在水中的电离程度小于水解程度 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 向浓度均为0.1mol/L的NaCl和NaI的混合溶液中滴加少量0.1mol/L的AgNO3溶液 | 产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-16更新
|
694次组卷
|
9卷引用:江西省临川第二中学2022-2023学年高二上学期第三次月考化学试题
江西省临川第二中学2022-2023学年高二上学期第三次月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题广东省江门市培英高级中学2022-2023学年高二上学期期中考试化学试题广东省梅州市兴宁市沐彬中学2021-2022学年高二下学期期中考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期10月月考化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题湖南省衡阳县2022-2023学年高二上学期期末考试化学试题广东省惠州市华罗庚中学2023-2024学年高二下学期5月期中考试化学试题
解题方法
9 . 钨有“烈火金刚”的美称,以其高熔点、高比重、高硬度的特点,广泛应用于机械加工、冶金、采矿行业、电光源、建筑工业、兵器工业、航天航空等领域,是一种重要的战略资源,可以说没有钨就没有发达的现代工业。含钨的矿物有黑钨矿和白钨矿,白钨矿主要含CaWO4、Fe2O3、SiO2等,从白钨矿提取钨的工艺流程如下图所示。
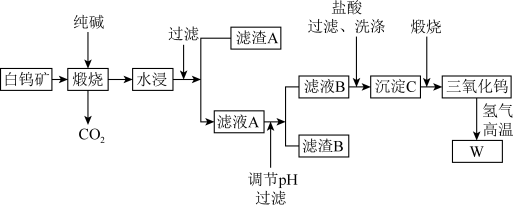
(1)写出CaWO4在煅烧时生成Na2WO4发生反应的化学方程式:_______ 。
(2)在“水浸”时,为加快浸出速率,写出一种可以采取的措施:_______ 。
(3)写出滤渣A的一种用途_______ 。
(4)调节pH的目的:_______ 。
(5)洗涤沉淀C的操作为:_______ 。
(6)为了获取高纯度的金属钨,不宜用碳而必须用氢气做还原剂的原因除了碳和金属钨在高温下会反应生成碳化钨,还存在的原因有_______ (写出一种合理的原因即可)。
(7)钨酸的酸性很弱,难溶于水,写出往滤液B中加入盐酸所发生的反应离子方程式:_______ 。

(1)写出CaWO4在煅烧时生成Na2WO4发生反应的化学方程式:
(2)在“水浸”时,为加快浸出速率,写出一种可以采取的措施:
(3)写出滤渣A的一种用途
(4)调节pH的目的:
(5)洗涤沉淀C的操作为:
(6)为了获取高纯度的金属钨,不宜用碳而必须用氢气做还原剂的原因除了碳和金属钨在高温下会反应生成碳化钨,还存在的原因有
(7)钨酸的酸性很弱,难溶于水,写出往滤液B中加入盐酸所发生的反应离子方程式:
您最近一年使用:0次
名校
10 . 已知SrF2属于难溶于水、可溶于酸的盐。常温下,用HCl调节SrF2浊液的pH,测得在不同pH条件下,体系中-1gc(X)(X为Sr2+或F-)与1g[ ]的关系如图所示。
]的关系如图所示。

下列说法错误的是
 ]的关系如图所示。
]的关系如图所示。
下列说法错误的是
A.L1代表-lgc(Sr2+)与lg[ ]的变化曲线 ]的变化曲线 |
| B.Ksp(SrF2)的数量级为10-9 |
| C.a、c两点的溶液中均存在2c(Sr2+)=c(F-)+c(HF) |
| D.c点的溶液中存在c(Cl-)>c(Sr2+)=c(HF)>c(H+) |
您最近一年使用:0次
2022-03-11更新
|
2255次组卷
|
7卷引用:江西师范大学附属中学2022届高三下学期三模理科综合化学试题
江西师范大学附属中学2022届高三下学期三模理科综合化学试题河北省石家庄市2021-2022学年下学期高中毕业班教学质量检测(一)化学试题山东省泰安市2022届高三二轮验收考试化学试题(已下线)专题13 水溶液中的离子平衡-备战2023年高考化学母题题源解密(全国通用)山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题广东省茂名市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)T13-溶液中的离子平衡



