名校
1 . 近期,科学家研发了“全氧电池”,其工作原理如图。

| A.电极a是正极 |
| B.电极b的反应式:O2+4e-+2H2O=4OH- |
| C.该装置可将酸碱反应的化学能转化为电能 |
| D.理论上,当电极a释放出22.4LO2(标况下),KOH溶液质量减少32g |
您最近一年使用:0次
名校
解题方法
2 . I.化学反应中伴随着能量变化,根据相关知识回答下列问题:
(1)下列过程吸热的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为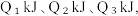 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是___________ (填序号)。
①.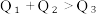 ②.
②. 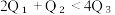 ③.
③. 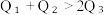 ④.
④. 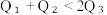
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。___________ 。
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)___________ 。
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为___________ ,___________ (填“电子”或“电流”)是由锌片经导线流向铜片。标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。
(6)某同学想利用反应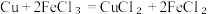 设计一个原电池请在下图
设计一个原电池请在下图___________ (共2处)标出使用的用品。
(1)下列过程吸热的是
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为
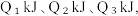 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是①.
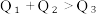 ②.
②. 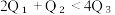 ③.
③. 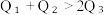 ④.
④. 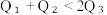
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。
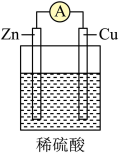
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为
(6)某同学想利用反应
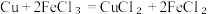 设计一个原电池请在下图
设计一个原电池请在下图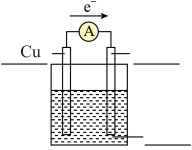
您最近一年使用:0次
解题方法
3 . 在2L恒温恒容密闭容器中投入2molSO2和1molO2在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。___________ ;平衡时,SO2的转化率为___________ 。
(2)下列叙述能判断该反应达到平衡状态的是___________ (填序号)。
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是___________ (填字母)。
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:___________ 。(填“正极”或“负极”)
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为___________ 。

(2)下列叙述能判断该反应达到平衡状态的是
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
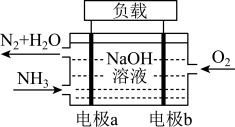
②电解质溶液中OH-离子向
③电极b的电极反应式为
您最近一年使用:0次
解题方法
4 . 人类利用二氧化碳合成淀粉对社会的发展起着重要作用,合成过程首先是利用二氧化碳制备甲醇,合成甲醇的反应为:CO2+3H2 CH3OH+H2O ∆H1。回答下列问题:
CH3OH+H2O ∆H1。回答下列问题:
(1)已知:①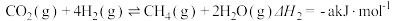
②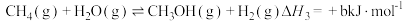
③ 均为大于零的数,且
均为大于零的数,且

___________  (用含
(用含 、
、 的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含
的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含 )电极反应式为
)电极反应式为___________ 。
(2)研究合成甲醇的催化剂时,在其他条件不变仅改变催化剂种类的情况下,对反应器出口产品进行成分分析,结果如图所示。在以上催化剂中,该反应的最佳催化剂为___________ (填化学式)。 的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。
的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。___________ 。
②结合上图及学过的知识推测,有水参与的历程,反应速率加快的原因是___________ 。
(4)在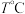 时,将
时,将 和
和 充入容积为
充入容积为 的恒容容器中,只发生
的恒容容器中,只发生 ,测得体系中剩余
,测得体系中剩余 的物质的量随时间变化如图中状态Ⅰ所示。
的物质的量随时间变化如图中状态Ⅰ所示。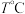 时,
时,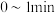 内甲醇的反应速率
内甲醇的反应速率
___________ 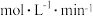 。
。
②该反应的平衡常数表达式为___________ 。
③保持投料量不变,仅改变某一个条件后,测得 随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是___________ 。
 CH3OH+H2O ∆H1。回答下列问题:
CH3OH+H2O ∆H1。回答下列问题:(1)已知:①
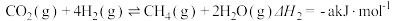
②
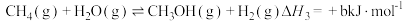
③
 均为大于零的数,且
均为大于零的数,且

 (用含
(用含 、
、 的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含
的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含 )电极反应式为
)电极反应式为(2)研究合成甲醇的催化剂时,在其他条件不变仅改变催化剂种类的情况下,对反应器出口产品进行成分分析,结果如图所示。在以上催化剂中,该反应的最佳催化剂为
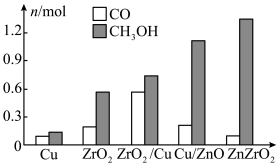
 的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。
的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。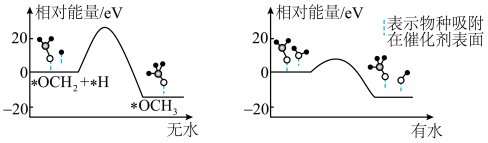
②结合上图及学过的知识推测,有水参与的历程,反应速率加快的原因是
(4)在
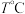 时,将
时,将 和
和 充入容积为
充入容积为 的恒容容器中,只发生
的恒容容器中,只发生 ,测得体系中剩余
,测得体系中剩余 的物质的量随时间变化如图中状态Ⅰ所示。
的物质的量随时间变化如图中状态Ⅰ所示。
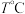 时,
时,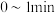 内甲醇的反应速率
内甲醇的反应速率
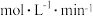 。
。②该反应的平衡常数表达式为
③保持投料量不变,仅改变某一个条件后,测得
 随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
您最近一年使用:0次
5 .  是一种具有强温室效应的分子,将其先转化为合成气
是一种具有强温室效应的分子,将其先转化为合成气 再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。
再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。
(1)已知H2、CO和C10H22(正癸烷, )的燃烧热依次是
)的燃烧热依次是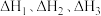 ,则反应
,则反应 的反应热
的反应热
_______ (用含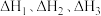 的代数式表示)。
的代数式表示)。
(2)氢气作为理想能源的原因_______ (写出一个原因即可)。
(3)甲烷转化为合成气主要是在催化剂的作用下发生如下反应:
 反应I
反应I
 反应Ⅱ
反应Ⅱ
①向一定温度下的 刚性容器中充入
刚性容器中充入 甲烷和
甲烷和 水蒸气,
水蒸气, 后体系达平衡状态,此时容器中含有
后体系达平衡状态,此时容器中含有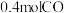 和
和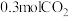 ,则
,则 内反应I的平均速率
内反应I的平均速率 =
=_______  ,写出该温度下反应Ⅱ的平衡常数为
,写出该温度下反应Ⅱ的平衡常数为_______ 。
②在起始投料比一定的密闭容器中,温度对 平衡转化率、
平衡转化率、 选择性、
选择性、 选择性的影响如图所示,其中表示
选择性的影响如图所示,其中表示 选择性的曲线是
选择性的曲线是_______ (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。_______ 。
②若放电一段时间后,消耗氧气2.24L(标准状况),理论上外电路转移电子的物质的量为_______ 。
 是一种具有强温室效应的分子,将其先转化为合成气
是一种具有强温室效应的分子,将其先转化为合成气 再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。
再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。(1)已知H2、CO和C10H22(正癸烷,
 )的燃烧热依次是
)的燃烧热依次是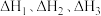 ,则反应
,则反应 的反应热
的反应热
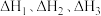 的代数式表示)。
的代数式表示)。(2)氢气作为理想能源的原因
(3)甲烷转化为合成气主要是在催化剂的作用下发生如下反应:
 反应I
反应I 反应Ⅱ
反应Ⅱ①向一定温度下的
 刚性容器中充入
刚性容器中充入 甲烷和
甲烷和 水蒸气,
水蒸气, 后体系达平衡状态,此时容器中含有
后体系达平衡状态,此时容器中含有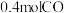 和
和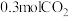 ,则
,则 内反应I的平均速率
内反应I的平均速率 =
= ,写出该温度下反应Ⅱ的平衡常数为
,写出该温度下反应Ⅱ的平衡常数为②在起始投料比一定的密闭容器中,温度对
 平衡转化率、
平衡转化率、 选择性、
选择性、 选择性的影响如图所示,其中表示
选择性的影响如图所示,其中表示 选择性的曲线是
选择性的曲线是 ”、“
”、“ ”或“
”或“ ”)。
”)。

②若放电一段时间后,消耗氧气2.24L(标准状况),理论上外电路转移电子的物质的量为
您最近一年使用:0次
2024-05-12更新
|
113次组卷
|
2卷引用:天津市河北区2023-2024学年高三下学期二模化学试卷
6 . 某实验小组利用如图装置探究电化学法保护铁制品的原理。反应一段时间后,下列说法错误的是
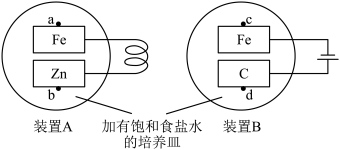

| A.装置A利用的是牺牲阳极法 |
B.取a处溶液,滴加 溶液,有蓝色沉淀 溶液,有蓝色沉淀 |
| C.向c处滴加几滴酚酞溶液,变红 |
| D.在d处上方放置湿润的淀粉-KI试纸,试纸变蓝 |
您最近一年使用:0次
2024-05-11更新
|
759次组卷
|
3卷引用:化学(天津卷02)-2024年高考化学押题预测卷
名校
解题方法
7 . 按要求写出下列反应的方程式:
(1)实验室制氨气的化学方程式:___________ 。
(2)浓硝酸久置呈黄色的原因用化学方程式解释:___________ 。
(3)工业制粗硅的化学方程式:___________ 。
(4)往硅酸钠溶液中通入过量二氧化碳的离子方程式:___________ 。
(5) 与稀硫酸反应的离子方程式:
与稀硫酸反应的离子方程式:___________ 。
(6)澄清石灰水中通入少量 的离子方程式:
的离子方程式:___________ 。
(7)银锌电池是一种常见的化学电源,其反应原理: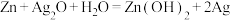 ,其工作原理如图所示。
,其工作原理如图所示。 电极反应式为
电极反应式为___________ 。
(8)将用导线相连的两个铂电极插入 溶液中,然后向两极分别通入
溶液中,然后向两极分别通入 和
和 ,则发生了原电池反应,该原电池中的负极反应式为
,则发生了原电池反应,该原电池中的负极反应式为___________ 。
(1)实验室制氨气的化学方程式:
(2)浓硝酸久置呈黄色的原因用化学方程式解释:
(3)工业制粗硅的化学方程式:
(4)往硅酸钠溶液中通入过量二氧化碳的离子方程式:
(5)
 与稀硫酸反应的离子方程式:
与稀硫酸反应的离子方程式:(6)澄清石灰水中通入少量
 的离子方程式:
的离子方程式:(7)银锌电池是一种常见的化学电源,其反应原理:
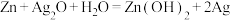 ,其工作原理如图所示。
,其工作原理如图所示。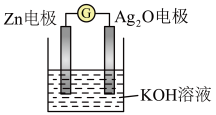
 电极反应式为
电极反应式为(8)将用导线相连的两个铂电极插入
 溶液中,然后向两极分别通入
溶液中,然后向两极分别通入 和
和 ,则发生了原电池反应,该原电池中的负极反应式为
,则发生了原电池反应,该原电池中的负极反应式为
您最近一年使用:0次
名校
解题方法
8 . 流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为 。
。
 。
。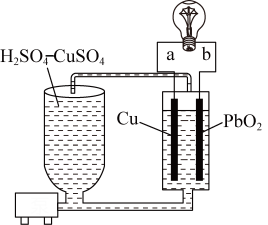
A. 为负极,a为正极 为负极,a为正极 |
B.该电池工作时,电流由电极a流向电极 |
C. 极的电极反应式为 极的电极反应式为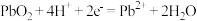 |
D.调节电解质溶液的方法是补充 |
您最近一年使用:0次
9 . 钠基海水电池,如图所示,电极材料为钠基材料和选择性催化材料(能抑制海水中 的吸附和氧化),固体电解质只允许
的吸附和氧化),固体电解质只允许 透过。下列说法正确的是
透过。下列说法正确的是
 的吸附和氧化),固体电解质只允许
的吸附和氧化),固体电解质只允许 透过。下列说法正确的是
透过。下列说法正确的是
| A.放电时,a电极为负极 |
| B.放电时,b电极的电势低于a电极 |
C.充电时,b电极的电极反应式为: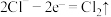 |
| D.充电时,阳极区碱性增强 |
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.判断吸热反应与放热反应
(1)下列变化:①铝片与稀盐酸的反应;② 晶体与
晶体与 晶体混合反应;
晶体混合反应;
③浓硫酸溶于水;④氯酸钾分解制氧气;⑤生石灰与水反应生成熟石灰。属于吸热反应的是______ (填序号),属于放热反应的是______ (填序号)。
(2)反应A+B→C(放热)分两步进行:①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是____________ 。______ 极(填“正”或“负”),发生______ (填“氧化”或“还原”)反应,此电极反应方程式为____________ 。
(4)若反应中溶解了6.5 g锌,则生成的氢气标况下的体积为______ L。
Ⅲ.A、B、C、D均为中学化学常见的纯净物。它们之间有如下的反应关系:______ ,A→C的反应方程式为:____________ 。
(6)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A单质是大气的主要成分,写出反应③的化学方程式:____________ 。
(7)若单质A是太阳能电池用的光伏材料,C、D为钠盐,两种盐中除钠、氧外的元素为同一主族,且溶液均显碱性。
D的化学式是______ ,写出④反应的化学方程式:____________ 。
Ⅳ.某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的酸性呈逐渐增强的趋势:
(8)用离子方程式解释原因:____________ 。
(9)实验室模拟二氧化硫在葡萄酒中的抗氧化过程,向溴水中通入 ,请用离子方程式表示该反应原理
,请用离子方程式表示该反应原理____________ 。
(10)向 溶液中通入
溶液中通入 至饱和,此过程无明显现象,再向溶液中加入一种物质,溶液变浑浊。加入的这种物质
至饱和,此过程无明显现象,再向溶液中加入一种物质,溶液变浑浊。加入的这种物质不可能 是______。
(1)下列变化:①铝片与稀盐酸的反应;②
 晶体与
晶体与 晶体混合反应;
晶体混合反应;③浓硫酸溶于水;④氯酸钾分解制氧气;⑤生石灰与水反应生成熟石灰。属于吸热反应的是
(2)反应A+B→C(放热)分两步进行:①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是
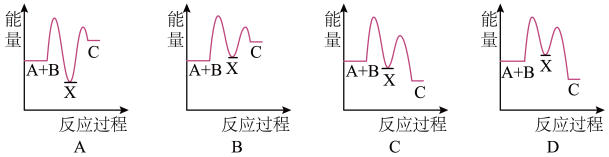

(4)若反应中溶解了6.5 g锌,则生成的氢气标况下的体积为
Ⅲ.A、B、C、D均为中学化学常见的纯净物。它们之间有如下的反应关系:

(6)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A单质是大气的主要成分,写出反应③的化学方程式:
(7)若单质A是太阳能电池用的光伏材料,C、D为钠盐,两种盐中除钠、氧外的元素为同一主族,且溶液均显碱性。
D的化学式是
Ⅳ.某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的酸性呈逐渐增强的趋势:
(8)用离子方程式解释原因:
(9)实验室模拟二氧化硫在葡萄酒中的抗氧化过程,向溴水中通入
 ,请用离子方程式表示该反应原理
,请用离子方程式表示该反应原理(10)向
 溶液中通入
溶液中通入 至饱和,此过程无明显现象,再向溶液中加入一种物质,溶液变浑浊。加入的这种物质
至饱和,此过程无明显现象,再向溶液中加入一种物质,溶液变浑浊。加入的这种物质A. | B. | C. | D. |
您最近一年使用:0次



