解题方法
1 . Cu2+可以与乙二胺(H2N—CH2CH2—NH2)形成配离子(如图),下列说法正确的是
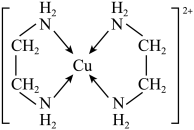

| A.乙二胺中含有σ、π键 |
| B.该配离子中,中心原子的配位数为2 |
C.基态铜原子的价电子排布图为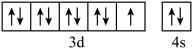 |
| D.沸点:乙二胺>Cl—CH2CH2—Cl |
您最近一年使用:0次
名校
解题方法
2 . 下列性质错误的是
| A.第一电离能: Na<Mg<Al | B.电负性: N<O<F |
| C.离子半径: Cl- >O2- >Na+ | D.沸点:金刚石>NaCl>CO2 |
您最近一年使用:0次
2023-08-26更新
|
71次组卷
|
2卷引用:云南省保山市高(完)中C、D类学校2022-2023学年高二下学期5月份联考化学试题
解题方法
3 . 下列说法正确的是
A. 的空间结构:正四面体 的空间结构:正四面体 | B.Na 位于元素周期表p区 |
| C.2p、 3p、4p能级的轨道数一样多 | D.CH4分子的空间充填模型: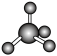 |
您最近一年使用:0次
名校
解题方法
4 . 化学科学需要借助化学专用语言来描述,下列化学用语表达正确的是
A.基态氧原子的价层电子排布式:2s22p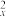 2p 2p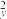 |
B.H2S的电子式: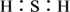 |
C.Be的原子结构示意图: |
D.基态Cr的价层电子的轨道表示式: |
您最近一年使用:0次
名校
5 . ZnS荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方ZnS的晶胞如图所示,其晶胞参数为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.电负性:Zn>S |
| B.S元素在元素周期表中位于s区 |
C.基态Zn原子的价层电子排布式为 |
D.立方ZnS晶体密度为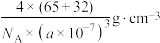 |
您最近一年使用:0次
2023-07-29更新
|
254次组卷
|
3卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三上学期月考(一) 理综化学试题
6 . 下列叙述中,正确的是

| A.在同一能级上运动的电子,其运动状态肯定不同 |
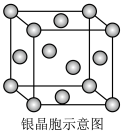
| B.如图所示银的晶胞中有14个银原子 |
| C.11号到18号元素位于元素周期表中同一周期,所以元素的电负性逐渐增大 |
| D.固态时能导电的晶体一定是金属晶体 |
您最近一年使用:0次
名校
解题方法
7 . (Ⅰ)瑞德西韦是一种核苷类似物,具有抗病毒活性,对新型冠状病毒病例展现出较好的疗效。其结构如图所示:
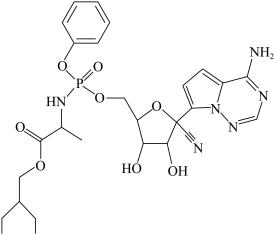
回答下列问题:
(1)该结构中基态P原子价电子的轨道表示式为___________ ,核外电子占据最高能级的电子云轮廓图形状为___________ 。
(2)瑞德西韦组成元素中位于第二周期元素的第一电离能从大到小的顺序为___________ ,分子中氮原子的杂化类型有___________ 。
(3)苯酚(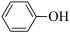 )是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是
)是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是________ 。苯酚与甲苯(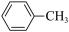 ,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是
,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是___________ 。
(Ⅱ)大力推广磷酸亚铁锂电池新能源汽车对实现“碳达峰”和“碳中和”具有重要意义。电极材料以硫铁矿(主要成分 ,含少量
,含少量 、
、 和
和 )为原料制备,工业流程如图所示。回答下列问题:
)为原料制备,工业流程如图所示。回答下列问题:
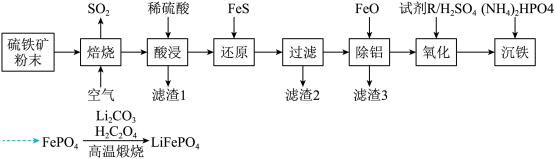
(4) 分子的空间结构名称为
分子的空间结构名称为___________ ,试剂R是一种绿色氧化剂,其中心原子杂化方式是___________ 。
(5)从平衡的角度解释加FeO除铝的原因(结合离子方程式说明)___________ 。
(6)若“沉铁”时溶液中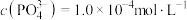 ,则“沉铁”时pH不能高于
,则“沉铁”时pH不能高于___________ ,[已知:常温下,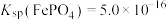 、
、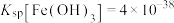 、
、 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。
(7)磷酸亚铁锂( )的晶胞结构如图所示:
)的晶胞结构如图所示:
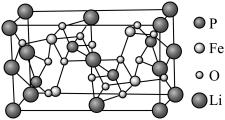
长方体晶胞的长和宽均为 ,高为
,高为 ,
, 为阿伏加德罗常数的值,晶体的密度为
为阿伏加德罗常数的值,晶体的密度为___________  。
。

回答下列问题:
(1)该结构中基态P原子价电子的轨道表示式为
(2)瑞德西韦组成元素中位于第二周期元素的第一电离能从大到小的顺序为
(3)苯酚(
 )是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是
)是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是 ,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是
,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是(Ⅱ)大力推广磷酸亚铁锂电池新能源汽车对实现“碳达峰”和“碳中和”具有重要意义。电极材料以硫铁矿(主要成分
 ,含少量
,含少量 、
、 和
和 )为原料制备,工业流程如图所示。回答下列问题:
)为原料制备,工业流程如图所示。回答下列问题:
(4)
 分子的空间结构名称为
分子的空间结构名称为(5)从平衡的角度解释加FeO除铝的原因(结合离子方程式说明)
(6)若“沉铁”时溶液中
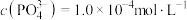 ,则“沉铁”时pH不能高于
,则“沉铁”时pH不能高于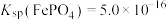 、
、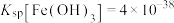 、
、 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。(7)磷酸亚铁锂(
 )的晶胞结构如图所示:
)的晶胞结构如图所示:
长方体晶胞的长和宽均为
 ,高为
,高为 ,
, 为阿伏加德罗常数的值,晶体的密度为
为阿伏加德罗常数的值,晶体的密度为 。
。
您最近一年使用:0次
名校
解题方法
8 . 硫及其化合物用途非常广泛。回答下列问题:
(1)基态S原子的电子占据最高能级的电子云轮廓图为_______ 形。
(2)O和S处于同一主族。 及
及 中,中心原子的杂化方式相同,键长及键角如图1所示。
中,中心原子的杂化方式相同,键长及键角如图1所示。
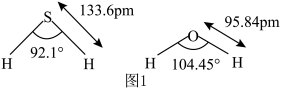
① 分子中的键长比
分子中的键长比 中的键长短,其原因是
中的键长短,其原因是_______ 。
② 分子中的键角
分子中的键角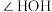 比
比 分子中的键角
分子中的键角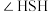 大,其原因是
大,其原因是_______ 。
(3)①单质硫与热的 浓溶液反应的产物之一为
浓溶液反应的产物之一为 。
。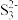 的空间构型为
的空间构型为_______ 。
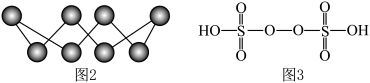
②S单质的常见形式为 ,其环状结构如图2所示,S原子采用的轨道杂化方式是
,其环状结构如图2所示,S原子采用的轨道杂化方式是_______ 。
③钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为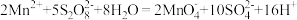 。已知
。已知 的结构如图3所示,上述反应每生成
的结构如图3所示,上述反应每生成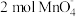 ,
, 层断裂的共价键数目为
层断裂的共价键数目为_______  。
。
(4)噻吩( )广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有
)广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有_______ 个 键。噻吩的沸点为
键。噻吩的沸点为 ,吡咯(
,吡咯(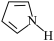 )的沸点在
)的沸点在 之间,后者沸点较高,其原因
之间,后者沸点较高,其原因_______ 。
(1)基态S原子的电子占据最高能级的电子云轮廓图为
(2)O和S处于同一主族。
 及
及 中,中心原子的杂化方式相同,键长及键角如图1所示。
中,中心原子的杂化方式相同,键长及键角如图1所示。
①
 分子中的键长比
分子中的键长比 中的键长短,其原因是
中的键长短,其原因是②
 分子中的键角
分子中的键角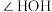 比
比 分子中的键角
分子中的键角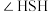 大,其原因是
大,其原因是(3)①单质硫与热的
 浓溶液反应的产物之一为
浓溶液反应的产物之一为 。
。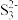 的空间构型为
的空间构型为②S单质的常见形式为
 ,其环状结构如图2所示,S原子采用的轨道杂化方式是
,其环状结构如图2所示,S原子采用的轨道杂化方式是③钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为
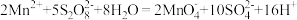 。已知
。已知 的结构如图3所示,上述反应每生成
的结构如图3所示,上述反应每生成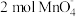 ,
, 层断裂的共价键数目为
层断裂的共价键数目为 。
。
(4)噻吩(
 )广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有
)广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有 键。噻吩的沸点为
键。噻吩的沸点为 ,吡咯(
,吡咯( )的沸点在
)的沸点在 之间,后者沸点较高,其原因
之间,后者沸点较高,其原因
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题:
(1)氟原子激发态的电子排布式有_______ (填标号,后同),其中能量较高的是_______ 。
a. b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为_______ 。
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图_______ (填标号),判断的根据是_______ ;第三电离能的变化图是图_______ (填标号)。

(4)短周期元素X、Y、Z、W的原子序数依次增大。
①元素的电负性:Z_______ (填“大于”“小于”或“等于”)W。
②简单离子半径:W_______ (填“大于”“小于”或“等于”)Y。
③氢化物的稳定性:X_______ (填“大于”“小于”或“等于”)Z。
(1)氟原子激发态的电子排布式有
a.
 b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图

(4)短周期元素X、Y、Z、W的原子序数依次增大。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | 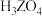 | |||
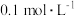 溶液对应的 溶液对应的 | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
名校
解题方法
10 . 下列图示或化学用语表示错误的是
| A | B | C | D |
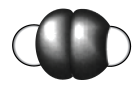 | 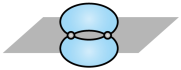 |  | 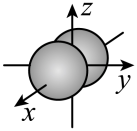 |
| 乙炔的空间填充模型 | 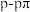 键电子云轮廓图 键电子云轮廓图 |  的结构示意图 的结构示意图 | 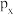 轨道的电子云轮廓图 轨道的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



