解题方法
1 . X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属元素,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法中正确的是( )
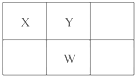

| A.X、W、Q三种元素的氧化物对应的水化物均为强酸 |
| B.Z单质的冶炼方法是电解熔融的Z与Q组成的化合物 |
| C.常温下Q的单质能与X的某种氢化物反应置换出X的单质 |
| D.Q的氢化物的水溶液酸性强于W的氢化物的水溶液酸性,说明非金属性Q>W |
您最近一年使用:0次
名校
2 . 短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是
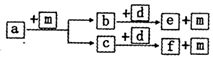

| A.原子半径:W<X<Y<Z |
| B.阴离子的还原性:Y>W |
| C.a—定由W、X两种元素组成 |
| D.图中转化过程d物质在作为反应物时均即为氧化剂又是还原剂 |
您最近一年使用:0次
2017-07-15更新
|
1867次组卷
|
6卷引用:辽宁省实验中学2017-2018学年高一下学期期中考试理科化学试题
名校
3 . X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素。下列说法不正确 的是
| Y | Z | M | ||
| W |
| A.原子半径:W>Y>Z>M>X |
| B.N的一种氧化物可用作油漆和涂料 |
| C.氢化物的沸点:Z小于M |
| D.工业上制备W单质的方法为电解熔融的W的氧化物 |
您最近一年使用:0次
2017-05-25更新
|
1560次组卷
|
4卷引用:辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题
辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题(已下线)专题16 元素周期律和元素周期表(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练
4 . (1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2[常用(en)表示]作用,可形成配离子(如图所示):
请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是____________ ,
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________ 。
②上述配离子中含有的化学键类型有:__________________ 。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为_______ ;其中铜离子的配位数是_______ 。
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为__________________
②Fe元素位于周期表的_____ 区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为____ ;
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为______ 和______ (填化学式)。
③根据VSEPR理论预测ED4-离子的空间构型为_________ 。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的化学式为____________ (写2种)。

请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是
②上述配离子中含有的化学键类型有:
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为
②Fe元素位于周期表的
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为
③根据VSEPR理论预测ED4-离子的空间构型为
您最近一年使用:0次
名校
5 . 下表列出了前20号元素中的某些元素性质的有关数据
元素R的原子半径为1.02×10-10 m,下列有关叙述正确的是
元素标号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | — |
| 最低价态 | — | — | -2 | — | -4 | -3 | -1 | — | -3 | -1 |
| A.以上10种元素的原子中,失去核外第一个电子所需能量最少的是⑧ |
| B.由⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是PCl5和CCl4 |
| C.元素R在周期表中位于第三周期第ⅤI族 |
D.若物质Na2R3是一种含有非极性共价键的离子化合物,则其化合物的电子式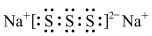 |
您最近一年使用:0次
2017-05-15更新
|
1015次组卷
|
4卷引用:辽宁省六校协作体2016-2017学年高二下学期期中考试化学试题
解题方法
6 . 下表是元素周期表的一部分,针对表中的①~⑩中10种元素用元素符号或化学式填空回答以下问题:
Ⅰ.填写下列空白:
(1)非金属性最强的元素是___________ (填元素符号),
(2)写出①与③形成原子个数比为1:1化合物的电子式:____________ ,该化合物酸性条件下与高锰酸钾反应的离子方程式:__________________________
(3)最高价氧化物对应的水化物中碱性最强的是_______ (填化学式),写出该物质与⑦的最高价氧化物对应的水化物反应的离子方程式为:____________ 。
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式____________________________
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:
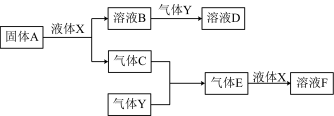
(1)A与液体X反应的化学方程式:____________________________ ;
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:___________________________ ;
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为__________ (用“NA”表示)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)非金属性最强的元素是
(2)写出①与③形成原子个数比为1:1化合物的电子式:
(3)最高价氧化物对应的水化物中碱性最强的是
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:

(1)A与液体X反应的化学方程式:
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为
您最近一年使用:0次
名校
解题方法
7 . 有五个系列同族元素的物质,101.3kPa时测定它们的沸点(℃)如下表所示:
对应表中内容,下列叙述中正确的是
| ① | He -268.8 | Ne -249.5 | (a) -185.8 | Kr 151.7 |
| ② | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| ③ | (c) 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| ④ | CH4 -161.0 | SiH4 -112.0 | GeH4 -90.0 | (e) -52.0 |
| A.系列①物质均为非金属单质,都含有共价键 |
| B.系列②物质的沸点逐渐升高是因为共价键越来越牢固 |
| C.系列③物质的还原性依次减弱 |
| D.系列④中各化合物的热稳定性从左到右逐渐减弱 |
您最近一年使用:0次
2017-05-10更新
|
435次组卷
|
2卷引用:辽宁省鞍山市第一中学2016-2017学年高一下学期期中考试化学试题
名校
8 . 几种短周期元素的原子半径及主要化合价如下表所示:下列叙述不正确的是
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5-3 | -2 | +3 |
| A.离子半径大小:Y2+>M2+>R3 |
| B.Z与M组成的某种化合物能形成酸雨 |
| C.Y与M组成的化合物跟水反应后一定能得强酸 |
| D.X、Y、R的最高价氧化物的水化物两两之间能发生反应 |
您最近一年使用:0次
解题方法
9 . 4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
回答下列问题:
(1)元素x在周期表中的位置是____ ,其单质可采用电解熔融________ 的方法制备。
(2)气体分子(mn)2的电子式为____ ,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为____ 。
(3)已知氰化钠(NaCN),可以与很多金属形成络合物,因此工业上采用氰化法提炼金:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的络合物Na[Au(CN)2],其反应方程式为:①4Au+8NaCN+2H2O+O2=4Na[Au(CN)2]+4NaOH,Na[Au(CN)2]在水溶液中的电离方程式为:②Na[Au(CN)2]=Na++[Au(CN)2]-,然后再用锌从溶液中把金置换出来,锌转化为Na2[Zn(CN)4]。据此,请利用①写出在空气中用氰化钠溶液提取金的电极反应式:正极:____ ,负极:_____ 。
(4)若人不慎氰化钠中毒,可用Na2S2O3缓解,二者反应得到两种含硫元素的离子,其中一种遇到Fe3+可变为红色。写出解毒原理的相关离子方程式____ 。
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是
(2)气体分子(mn)2的电子式为
(3)已知氰化钠(NaCN),可以与很多金属形成络合物,因此工业上采用氰化法提炼金:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的络合物Na[Au(CN)2],其反应方程式为:①4Au+8NaCN+2H2O+O2=4Na[Au(CN)2]+4NaOH,Na[Au(CN)2]在水溶液中的电离方程式为:②Na[Au(CN)2]=Na++[Au(CN)2]-,然后再用锌从溶液中把金置换出来,锌转化为Na2[Zn(CN)4]。据此,请利用①写出在空气中用氰化钠溶液提取金的电极反应式:正极:
(4)若人不慎氰化钠中毒,可用Na2S2O3缓解,二者反应得到两种含硫元素的离子,其中一种遇到Fe3+可变为红色。写出解毒原理的相关离子方程式
您最近一年使用:0次
解题方法
10 . 已知A、B、C、D四种元素分别为短周期元素,表示中三个不同短周期的主族元素,且原子序数依次增
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称____________ ,C元素在元素周期表中的位置_____________ 。
(2)写出BA3的电子式____________ ,BA3跟C的单质在一定条件下反应,能生成化合物BC的化学方程式________________________________ 。
(3)D单质在工业上最重要的用途是_________ ,写出工业上制取D单质的化学方程式__________ 。
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存__________________ ,用化学方程
式说明理由____________________________________ 。
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称
(2)写出BA3的电子式
(3)D单质在工业上最重要的用途是
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存
式说明理由
您最近一年使用:0次



