名校
解题方法
1 . 回答以下关于元素及其化合物的问题。
(1)Na原子核外有________ 种不同能量的电子,其离子最外层电子的轨道表示式________ 。
(2)相同压强下,部分元素氟化物的熔点见下表:
①试解释上表中氟化物熔点差异的原因:___________ 。
② 分子的空间构型为
分子的空间构型为___________ , 中Si—F键间的键角是
中Si—F键间的键角是___________ 。
(3)元素周期表有多种形式。下图分别是三种不同形式元素周期表的局部区域。

①图A中,数值越大,则该元素的___________ (填“金属性”或“非金属性”)越强。写出能说明O、F两元素该性质强弱的化学方程式___________ 。
②根据图B预测,整个周期表中位置最低的元素应位于___________ (放射性元素除外)。图B所示第二周期主族元素中,某元素该性质反常偏高,则该元素原子核外电子排布式为___________ 。
③图C表示的意义是___________ 。
(4)元素周期表中,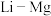 、
、 、
、 处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
(1)Na原子核外有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 |  |  |  |
| 熔点/℃ | 1266 | 1534 | 183 |
②
 分子的空间构型为
分子的空间构型为 中Si—F键间的键角是
中Si—F键间的键角是(3)元素周期表有多种形式。下图分别是三种不同形式元素周期表的局部区域。

①图A中,数值越大,则该元素的
②根据图B预测,整个周期表中位置最低的元素应位于
③图C表示的意义是
(4)元素周期表中,
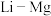 、
、 、
、 处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。A. 易溶于水 易溶于水 | B. |
C. 熔点高 熔点高 | D.晶体硼为分子晶体 |
您最近一年使用:0次
名校
解题方法
2 . 硅在自然界大部分以二氧化硅及硅酸盐的形式存在,它们的基本结构单位是硅氧四面体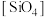 (图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
(图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
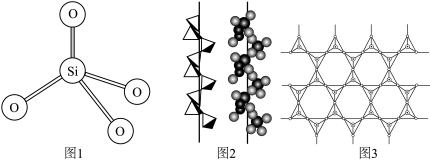
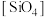 (图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
(图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
A.基态 原子的原子核外的电子有8种空间运动状态 原子的原子核外的电子有8种空间运动状态 |
| B.二氧化硅中硅原子的配位数是4 |
C.图2中Si原子的杂化轨道类型是 |
D.图3硅酸根阴离子结构中硅和氧的原子个数比为 |
您最近一年使用:0次
2023-12-01更新
|
333次组卷
|
3卷引用:安徽省江淮十校2024届高三上学期第二次联考化学试题
3 . 废SCR催化剂(含TiO2、V2O5、WO3等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
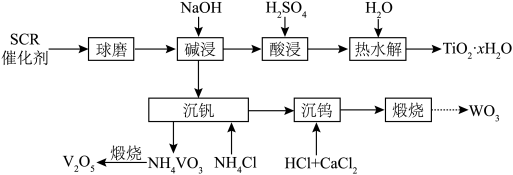
已知:TiO2、V2O5和WO3都能与NaOH溶液反应生成可溶性的NaVO3、Na2WO4和不溶性的Na2TiO3;
回答下列问题:
(1)元素V在周期表中的位置_______ 。在NH4VO3中V元素的化合价是_______ 。
(2)“球磨”的目的是_______ 。
(3)请写出“碱浸”过程中WO3与NaOH溶液反应的离子方程式_______ 。
(4)“酸浸”后钛主要以TiO2+形式存在,“热水解”反应的离子方程式为_______ 。
(5)“煅烧”NH4VO3的化学方程式为_______ 。
(6)“沉钨”中为促进CaWO4尽可能析出完全,需要进行的措施是_______ 。

已知:TiO2、V2O5和WO3都能与NaOH溶液反应生成可溶性的NaVO3、Na2WO4和不溶性的Na2TiO3;
回答下列问题:
(1)元素V在周期表中的位置
(2)“球磨”的目的是
(3)请写出“碱浸”过程中WO3与NaOH溶液反应的离子方程式
(4)“酸浸”后钛主要以TiO2+形式存在,“热水解”反应的离子方程式为
(5)“煅烧”NH4VO3的化学方程式为
(6)“沉钨”中为促进CaWO4尽可能析出完全,需要进行的措施是
您最近一年使用:0次
解题方法
4 . 四种短周期主族元素在元素周期表中的相对位置如图所示,且X、Y、Z和Q四种元素的p轨道电子总数为24。化学家鲍林以Y的电负性作为参照标准,得出了各元素的电负性。下列叙述错误的是
| X | Y | |||
| Z | Q |
| A.最简单氢化物的稳定性:Y>Q>Z |
B. 分子中每个原子最外层都达到8电子稳定结构 分子中每个原子最外层都达到8电子稳定结构 |
| C.最高价氧化物对应水化物的酸性: Z<Q |
D.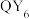 分子呈正八面体形 分子呈正八面体形 |
您最近一年使用:0次
2023-10-28更新
|
341次组卷
|
2卷引用:江西省部分高中学校2023-2024学年高三上学期10月联考化学试题
名校
解题方法
5 . 为维护国家安全和利益,经国务院批准,决定对镓、锗相关物项实施出口管制。镓的某种化合物的晶胞结构如下图所示(晶胞参数为a pm,1 pm=10-10cm,NA表示阿伏加德罗常数)。下列说法正确的是
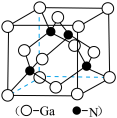

| A.Ga元素位于元素周期表的ds区 |
| B.晶体结构中N的配位数为6 |
| C.该物质的化学式为Ga4N4 |
D.该晶体的密度为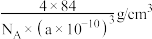 |
您最近一年使用:0次
2023-10-10更新
|
555次组卷
|
2卷引用:重庆市拔尖强基联盟(西南大学附中、育才中学)2023-2024学年高三10月联合考试化学试题
名校
解题方法
6 . 一种La、Ba、Co、O等元素为代表的新型双钙钛矿阴极材料,晶胞结构如图所示,目前已成为低温固体氧化物燃料电池(IT-SOFCs)的一大研究热点(A点为Ba,A’点为La,B点为Co,晶胞为正方体,棱长为a pm)。下列回答错误的是
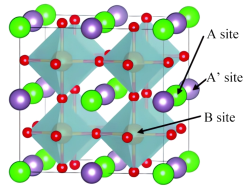

| A.该晶体的化学式为LaBaCo2O6 |
| B.距离Ba等距且最近的La的数目为12 |
C.该晶胞密度为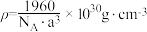 |
| D.Co元素在周期表中的位置为第四周期第Ⅷ族 |
您最近一年使用:0次
真题
解题方法
7 .  是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
(1)Co位于元素周期表第_______ 周期,第_______ 族。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因_______ 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是
常用方法的名称是_______ 。
(4)已知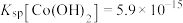 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为_______  。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为_______ 。
(5)导致 比
比 易水解的因素有
易水解的因素有_______ (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: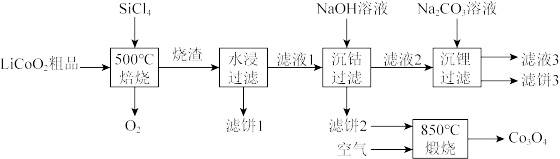
(1)Co位于元素周期表第
(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因(3)鉴别洗净的“滤饼3”和固体
 常用方法的名称是
常用方法的名称是(4)已知
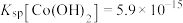 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为 。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为(5)导致
 比
比 易水解的因素有
易水解的因素有a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
您最近一年使用:0次
2023-06-14更新
|
10951次组卷
|
13卷引用:2023年高考湖北卷化学真题
2023年高考湖北卷化学真题(已下线)专题18 工艺流程题(已下线)T16-工业流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第32讲难溶电解质的溶解平衡(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型四 无机化工流程题解题策略-备战2024年高考化学答题技巧与模板构建(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
8 . 钒基笼目金属在超导电性方面有广阔的应用前最。某钒基笼目金属(M)的晶体结构如图所示。
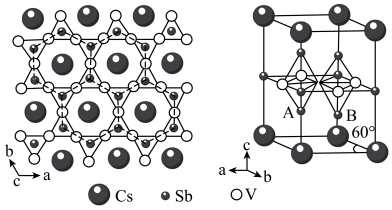
(1)Sb在元素周期表中的位置是___________ 。
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为___________ 。
(3)钒化合物在药物化学及催化化学等领域应用广泛。基态钒原子的价电子排布图为___________ ,钒有+2、+3、+4、+5等多种化合价,其中最稳定的化合价是_________ , 的空间结构为
的空间结构为________ 。
(4)SbH3的键角比NH3的键角小,原因是___________ 。
(5)该钒基笼目金属(M)的化学式为___________ ,与V原子距离最近且等距的V原子________ 个。
(6)已知,该晶胞中距离最近的两个V原子间的距离为2.75 Å,则晶胞体内A、B原子之间的距离为___________ Å ( ≈1.73, 保留两位小数)。
≈1.73, 保留两位小数)。

(1)Sb在元素周期表中的位置是
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为
(3)钒化合物在药物化学及催化化学等领域应用广泛。基态钒原子的价电子排布图为
 的空间结构为
的空间结构为(4)SbH3的键角比NH3的键角小,原因是
(5)该钒基笼目金属(M)的化学式为
(6)已知,该晶胞中距离最近的两个V原子间的距离为2.75 Å,则晶胞体内A、B原子之间的距离为
 ≈1.73, 保留两位小数)。
≈1.73, 保留两位小数)。
您最近一年使用:0次
解题方法
9 .  的晶胞结构如图所示,其中m、n、p、q的原子坐标分别为
的晶胞结构如图所示,其中m、n、p、q的原子坐标分别为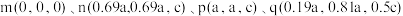 。下列说法正确的是
。下列说法正确的是
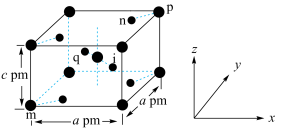
 的晶胞结构如图所示,其中m、n、p、q的原子坐标分别为
的晶胞结构如图所示,其中m、n、p、q的原子坐标分别为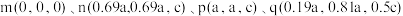 。下列说法正确的是
。下列说法正确的是
A. 位于周期表中第四周期第IIB族 位于周期表中第四周期第IIB族 |
| B.图中标记的微粒中,m、p代表氧原子 |
C.i的原子坐标为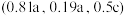 |
D.该晶体的密度为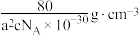 |
您最近一年使用:0次
解题方法
10 . 某化合物由原子序数依次增大的不同主族短周期元素Q、W、X、Y、Z组成,掺杂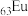 后具有良好荧光性能。已知W和X的原子序数之和等于Z的原子序数,只有W、X、Y
后具有良好荧光性能。已知W和X的原子序数之和等于Z的原子序数,只有W、X、Y
同周期且W、X、Y相邻。下列说法错误的是
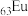 后具有良好荧光性能。已知W和X的原子序数之和等于Z的原子序数,只有W、X、Y
后具有良好荧光性能。已知W和X的原子序数之和等于Z的原子序数,只有W、X、Y同周期且W、X、Y相邻。下列说法错误的是
A.元素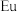 位于第六周期第ⅢB族 位于第六周期第ⅢB族 |
| B.Z、Q组成的化合物具有强还原性 |
| C.Q、Y组成的两种常见二元化合物均为极性分子 |
| D.W、Q组成的化合物沸点均比Y、Q组成的化合物沸点低 |
您最近一年使用:0次



