解题方法
1 . 锰(25Mn)及其化合物是目前前沿科学研究的热点。按要求回答下列问题。
(1)锰元素在元素周期表中的位置是___________ 。
(2)某晶体锰的面心立方晶胞如图所示。
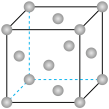
①该晶胞中含Mn原子的个数为___________ ;
②晶体锰中每个Mn原子距离最近的Mn原子数目为___________ 。
③设该晶胞参数棱长为 。则晶体锰的密度为
。则晶体锰的密度为___________  (列算式)
(列算式)
(3)锰的冶炼有多种方法,其中以某锰矿(主要成分为 ,主要杂质有
,主要杂质有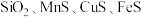 )为原料,设计如下流程可制得金属Mn。
)为原料,设计如下流程可制得金属Mn。
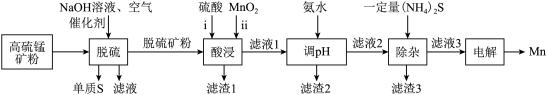
已知:金属硫化物的溶度积常数如下表。
①脱硫步骤:硫化物均转化为单质S,其反应中的氧化剂为___________ ; 能被部分反应而得到的产物为
能被部分反应而得到的产物为___________ 。
②酸浸步骤:ⅰ反应后的溶液中含 ,写出ⅱ反应的离子方程式:
,写出ⅱ反应的离子方程式:___________ ;滤渣1含有的物质有___________ 。若未经脱硫直接酸浸,不利的方面是___________ 。
③调 的目的为去除铁元素,则产生滤渣2的离子方程式:
的目的为去除铁元素,则产生滤渣2的离子方程式:___________ ;
④除杂步骤:滤渣3中主要有___________ 。
⑤电解步骤:惰性阳极产生 的反应式为
的反应式为___________ 。
(1)锰元素在元素周期表中的位置是
(2)某晶体锰的面心立方晶胞如图所示。

①该晶胞中含Mn原子的个数为
②晶体锰中每个Mn原子距离最近的Mn原子数目为
③设该晶胞参数棱长为
 。则晶体锰的密度为
。则晶体锰的密度为 (列算式)
(列算式)(3)锰的冶炼有多种方法,其中以某锰矿(主要成分为
 ,主要杂质有
,主要杂质有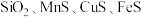 )为原料,设计如下流程可制得金属Mn。
)为原料,设计如下流程可制得金属Mn。
已知:金属硫化物的溶度积常数如下表。
| 物质 | CuS | MnS | FeS |
 |  | 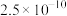 |  |
 能被部分反应而得到的产物为
能被部分反应而得到的产物为②酸浸步骤:ⅰ反应后的溶液中含
 ,写出ⅱ反应的离子方程式:
,写出ⅱ反应的离子方程式:③调
 的目的为去除铁元素,则产生滤渣2的离子方程式:
的目的为去除铁元素,则产生滤渣2的离子方程式:④除杂步骤:滤渣3中主要有
⑤电解步骤:惰性阳极产生
 的反应式为
的反应式为
您最近一年使用:0次
2 . 氧化铈(CeO2)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。下列说法错误的是
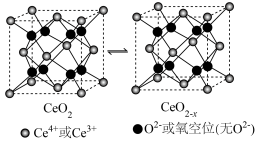

| A.氧元素位于元素周期表中的p区 |
| B.CeO2晶体中与Ce4+相邻且最近的Ce4+有12个 |
| C.O2-占据所有四面体空隙 |
| D.每个CeO2-x晶胞中Ce4+个数为1-2x |
您最近一年使用:0次
2023-04-24更新
|
495次组卷
|
2卷引用:山东省青岛平度市2023届高三高考模拟检测二化学试题
3 . 元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在元素周期表中的位置:___________ ,有关Be性质的推断不正确的是___________ (填序号)。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时, 溶液的
溶液的
(2)已知: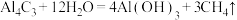 ,写出
,写出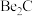 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):___________
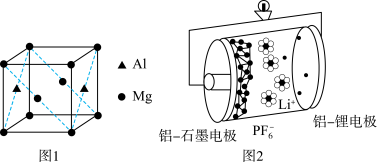
(3)基态铝原子的价电子排布式为___________ ,镁铝合金经过高温淬火获得一种储钠材料,用___________ 法测定其晶胞结构如图1所示,图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___________ ,该立方晶胞的晶胞的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为___________ pm。(列出计算式,可不化简)。
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为: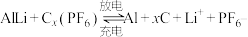 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为___________ ,充电时,应将铝-石墨电极与外接电源的___________ 极相连。
(1)Be元素在元素周期表中的位置:
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时,
 溶液的
溶液的
(2)已知:
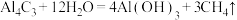 ,写出
,写出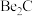 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):(3)基态铝原子的价电子排布式为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为:
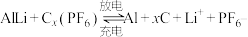 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为
您最近一年使用:0次
4 . 按照要求回答下列问题。
(1)有下列物质: 、
、 、
、 、
、 、
、 、
、 、
、 。
。
①上述物质中既含共价键又含离子键的__________ ;属于共价化合物的是__________ ;
② 溶于水时破坏
溶于水时破坏__________ (填“共价键”或“离子键”,下同), 熔化时破坏
熔化时破坏__________ 。
(2)砷在元素周期表中的位置__________ 。原子序数为115的 中子数为
中子数为__________ 。
(3)向 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为__________ 。可证明非金属性:
__________ S(填“>”或“<”)。
(4)短周期元素Y的一种含氧酸化学式为 ,其结构式可表示为
,其结构式可表示为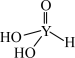 。该酸为
。该酸为__________ 元酸。写出该酸与过量 溶液反应的化学方程式:
溶液反应的化学方程式:__________ 。(用对应元素符号作答。已知信息:氢氧原子结合成的一种原子团“ ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
(1)有下列物质:
 、
、 、
、 、
、 、
、 、
、 、
、 。
。①上述物质中既含共价键又含离子键的
②
 溶于水时破坏
溶于水时破坏 熔化时破坏
熔化时破坏(2)砷在元素周期表中的位置
 中子数为
中子数为(3)向
 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为
(4)短周期元素Y的一种含氧酸化学式为
 ,其结构式可表示为
,其结构式可表示为 。该酸为
。该酸为 溶液反应的化学方程式:
溶液反应的化学方程式: ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
您最近一年使用:0次
2023-03-24更新
|
661次组卷
|
3卷引用:元素周期表
5 . X、Y、Z、W是同周期主族元素,四种元素均是短周期元素,W元素形成的某种单质具有强氧化性,可用于杀菌消毒。四种元素与锂组成的盐是一种新型锂离子电池的电解质,结构如图所示,下列说法正确的是
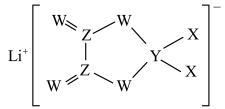

| A.组成这种新型电解质的所有元素均处于元素周期表p区 |
| B.Z元素的含氧酸不可能使酸性高锰酸钾溶液褪色 |
| C.最简单氢化物的沸点: X>W |
| D.同周期中第一电离能比W元素小的有4种元素 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
6 . 元素周期表中的数量应用
(1)甲、乙是元素周期表中同一周期的第ⅡA族和第ⅦA族元素,原子序数分别为m、n,则m、n的关系为_______ 。
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是_______ 。
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为_______ 。
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是_______。
(1)甲、乙是元素周期表中同一周期的第ⅡA族和第ⅦA族元素,原子序数分别为m、n,则m、n的关系为
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是_______。
A. | B.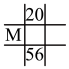 | C.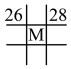 | D.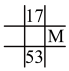 |
您最近一年使用:0次
名校
7 . 三氧化二锑,又称锑白,在工业上作阻燃剂、填充剂等,用途广泛。一种利用辉锑矿粉(含 及少量
及少量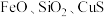 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
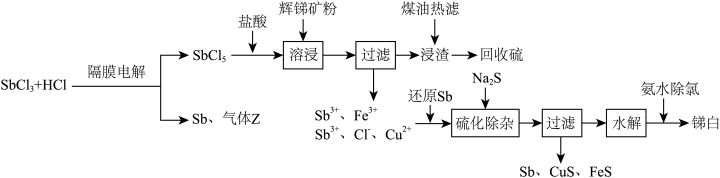
已知:①常温下,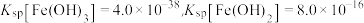 ,
, 。
。
②锑的常见价态为+3、+5价,其中 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。
(1)锑元素的原子序数为51,位于元素周期表第___________ 周期第___________ 族。
(2)溶浸时发生的主要反应的离子方程式为___________ 。
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是___________ 。
(4) 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:___________ ,锑白洗涤后便可干燥保存,检验洗净的试剂为___________ 。
(5)隔膜电解时,气体Z的分子式为___________ ;为平衡两极电荷,应使用___________ 交换膜(填“阴离子”“阳离子”或“质子”),理由是___________ 。
 及少量
及少量 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
已知:①常温下,
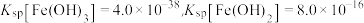 ,
, 。
。②锑的常见价态为+3、+5价,其中
 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。(1)锑元素的原子序数为51,位于元素周期表第
(2)溶浸时发生的主要反应的离子方程式为
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是
(4)
 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:(5)隔膜电解时,气体Z的分子式为
您最近一年使用:0次
2023-02-03更新
|
423次组卷
|
2卷引用:江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题
8 . 某物质结构如图所示,其中X、Y、Z、M、W均为短周期主族元素,且原子序数依次增大。下列说法正确的是
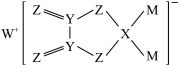

A.原子半径: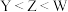 | B.第一电离能: |
C.X和Y原子均为 杂化 杂化 | D.该物质中除W外均是p区元素 |
您最近一年使用:0次
2023-01-10更新
|
695次组卷
|
2卷引用:湖北省部分市州2022-2023学年高三元月联合调研考试化学试题
9 . 下表标出的是元素周期表的一部分元素,回答下列问题:

(1)第三周期中原子半径最小的是___________ 。(用元素符号表示)
(2)表中用字母标出的15种元素中,化学性质最不活泼的是___________ (用元素符号表示),金属性最强的是___________ ,(用元素符号表示)非金属性最强的是___________ ,(用元素符号表示)属于过渡元素的是___________ (用字母表示)。
(3)d,e,f气态氢化物最稳定的为___________ , 最不稳定的为___________ 。(填化学式)
(4)钛被称为继铁、铝之后的第三金属,钛元素在元素周期表中的位置为___________ ,其价电子排布式为___________ 。
(5)请画出26号元素其价电子排布图:___________ 。
(6)d与a反应的产物的分子中心原子的杂化形式为___________ ,该分子是___________ (填“极性”或“非极性”)分子。
(7)写出铜元素在周期表中的位置___________ ,它位于___________ 区。并写出Cu+ 基态电子排布式___________ 。
(8)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态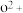 再失去一个电子比气态
再失去一个电子比气态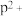 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是___________
(9)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX的晶体结构如图所示。
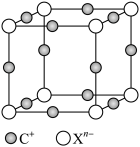
该晶体中阳离子和阴离子个数比为___________ ,晶体中每个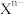 被
被___________ 个等距离的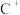 包围。
包围。

(1)第三周期中原子半径最小的是
(2)表中用字母标出的15种元素中,化学性质最不活泼的是
(3)d,e,f气态氢化物最稳定的为
(4)钛被称为继铁、铝之后的第三金属,钛元素在元素周期表中的位置为
(5)请画出26号元素其价电子排布图:
(6)d与a反应的产物的分子中心原子的杂化形式为
(7)写出铜元素在周期表中的位置
(8)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 |
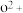 再失去一个电子比气态
再失去一个电子比气态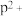 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(9)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX的晶体结构如图所示。

该晶体中阳离子和阴离子个数比为
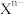 被
被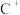 包围。
包围。
您最近一年使用:0次
名校
10 . 下列表格是元素周期表的一部分。请按要求填空(用化学用语填写)
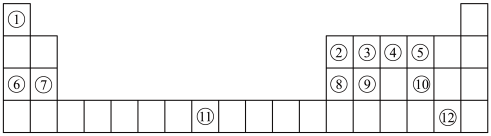
(1)元素①和⑥形成的化合物中存在的化学键类型为_______ 。
(2)用化学方程式表示④的简单氢化物的工业制法_______ 。
(3)写出由③④⑥形成的化合物的电子式_______ 。
(4)列举元素⑨形成的氧化物的一种用途_______ ,元素⑪在周期表中的位置_______ 。
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为_______ 。
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为_______ 。
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为_______ 。

(1)元素①和⑥形成的化合物中存在的化学键类型为
(2)用化学方程式表示④的简单氢化物的工业制法
(3)写出由③④⑥形成的化合物的电子式
(4)列举元素⑨形成的氧化物的一种用途
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol
 ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为
您最近一年使用:0次
2022-11-28更新
|
340次组卷
|
2卷引用:天津市南开中学2022-2023学年高三上学期第二次月考化学试题



