名校
1 . 按要求完成下列问题。
(1)物质A的结构简式为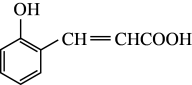 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称_______ 。
(2)有机化合物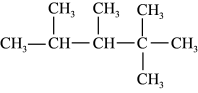 的名称是
的名称是_____ ,其在核磁共振氢谱上有_____ 组峰。
(3)实验室制取乙炔的反应方程式为_______ 。
(4)利用甲苯合成TNT的反应方程式为_______ 。
(5)区分晶体与非晶体最可靠的方法是_______ ,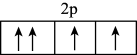 违反了
违反了_______ 。
(1)物质A的结构简式为
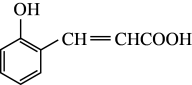 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称(2)有机化合物
 的名称是
的名称是(3)实验室制取乙炔的反应方程式为
(4)利用甲苯合成TNT的反应方程式为
(5)区分晶体与非晶体最可靠的方法是
 违反了
违反了
您最近一年使用:0次
名校
2 . A、B两元素。A元素的M层电子数与K层电子数相等;B元素原子的M层电子数等于其L层电子数的一半。则A为_______ ,B为_______ 。
您最近一年使用:0次
名校
3 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次
2022-03-15更新
|
800次组卷
|
4卷引用:北京师范大学附属中学2021-2022学年高二上学期期末考试化学试题
4 . 1913年,玻尔提出氢原子模型,电子在线性轨道上绕核运行,然而到了1926年,玻尔建立的线性轨道模型被量子力学推翻。量子力学指出,一定空间运动状态的电子并不在玻尔假定的线性轨道上运行,而在核外空间各处都可能出现,但出现的概率不同,即只能用统计的观点指出它在原子核外空间某处出现机会的多少。下图为多电子原子在核外空间出现的概率图:
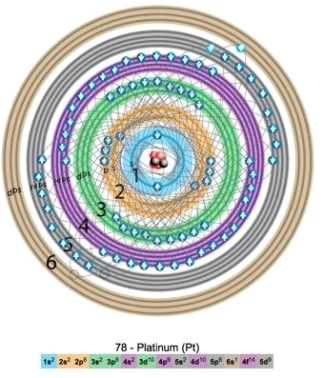
问题:仔细观察图片,你有什么发现?___________

问题:仔细观察图片,你有什么发现?
您最近一年使用:0次
5 . 核外电子排布规律
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按___________ 顺序排列。
(2)电子层最多容纳的电子数
①第n层最多容纳___________ 个电子,K、L、M、N层最多容纳的电子数依次为2、8、18、32。
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为___________ 。
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为___________ 。
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按
(2)电子层最多容纳的电子数
①第n层最多容纳
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为
您最近一年使用:0次
2021高一·全国·专题练习
解题方法
6 . 写出1~18号元素中符合下列条件的原子(或离子)的微粒符号,并画出其结构示意图。
(1)某元素原子L层上的电子数为K层的3倍:___________ 。
(2)某元素原子L层上的电子数为K层的一半:___________ 。
(3)某元素原子得到2个电子后所形成的电子总数与氩原子的电子总数相同的离子:___________ 。
(4)某元素原子的最外层电子数等于次外层电子数的2倍:___________ 。
(1)某元素原子L层上的电子数为K层的3倍:
(2)某元素原子L层上的电子数为K层的一半:
(3)某元素原子得到2个电子后所形成的电子总数与氩原子的电子总数相同的离子:
(4)某元素原子的最外层电子数等于次外层电子数的2倍:
您最近一年使用:0次
7 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ 。
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。I1(Li)> I1(Na),原因是___________ 。I1(Be)> I1(B)> I1(Li),原因是___________ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。I1(Li)> I1(Na),原因是
您最近一年使用:0次
8 . 用周期表中特殊位置的短周期元素符号填空
(1)族序数等于周期数3倍的元素:_______ ;
(2)周期数是族序数3倍的元素是:_______ ;
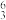 Li、
Li、 Li、
Li、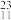 Na、
Na、 Mg、
Mg、 C、
C、 N中,
N中,
(3)_______ 和_______ 互为同位素;
(4)_______ 和_______ 的质量数相等,但不能互称同位素;
(1)族序数等于周期数3倍的元素:
(2)周期数是族序数3倍的元素是:
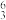 Li、
Li、 Li、
Li、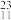 Na、
Na、 Mg、
Mg、 C、
C、 N中,
N中,(3)
(4)
您最近一年使用:0次
名校
9 . 铅的合金可作轴承、电缆外皮之用,还可做体育器材铅球等。铅元素位于元素周期表第六周期IVA,IVA中原子序数最小的元素的原子有___ 种能量不同的电子,其次外层的电子云有___ 种不同的伸展方向。与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是___ (填化学式),气态氢化物沸点最低的是___ (填化学式)。
您最近一年使用:0次
名校
10 . 回答下列问题。
Ⅰ.用“>”或“<”填空:
(1)键长:N-N___________ N=N
(2)键能:2E(C-C)___________ E(C=C)
(3)键角:CO2___________ SO2;
(4)键的极性:C-H___________ N-H。
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO 中的N
中的N___________ 杂化,空间构型___________ ;
(2)BCl3中的B___________ 杂化,空间构型___________ ;
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含___________ 种元素,___ 种核素,___________ 种相对分子质量。
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是___________ 电子,原子轨道呈现___________ 形,它的氢化物的电子式是___________
Ⅰ.用“>”或“<”填空:
(1)键长:N-N
(2)键能:2E(C-C)
(3)键角:CO2
(4)键的极性:C-H
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO
 中的N
中的N(2)BCl3中的B
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是
您最近一年使用:0次



