1 . Fe、Co、Ni、Cu均为第四周期元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为___________ 。在空气中FeO稳定性小于 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是___________ 。
(2) 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有___________ 个;C、N、B的电负性由小到大的顺序为___________ 。
(3)基态 的核外电子排布式为
的核外电子排布式为___________ ; 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式___________ 、___________ 。
(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点、B点原子的分数坐标分别为 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为___________ ;晶胞中C、D间距离d=___________ pm。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为
 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是(2)
 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有(3)基态
 的核外电子排布式为
的核外电子排布式为 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为
您最近半年使用:0次
解题方法
2 . 近年来,我国半导体材料市场发展迅速,其中以氮化嫁、碳化硅、氧化锌、金刚石等为主的材料备受关注。回答下列问题:
(1)基态Ga原子的价电子轨道表示式为___________ ,基态N原子核外电子有___________ 种空间运动状态。Zn在元素周期表中位于___________ 区。
(2)C,N、O的第一电离能由大到小的顺序为___________ 。 的空间结构为
的空间结构为___________ 。
(3)SiC的立方晶胞结构如图1所示,已知;1号C原子的坐标参数为( ,
, ,
, ),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
),晶胞参数为apm。则晶胞中2号C原子的坐标参数为___________ ,C和Si原子的最短距离为___________ pm。
①GaN晶体中N原子的杂化轨道类型为___________ 。
②GaN晶体的密度为___________ g/cm3(列出计算式,用含b、c、NA的代数式表示)。
(1)基态Ga原子的价电子轨道表示式为
(2)C,N、O的第一电离能由大到小的顺序为
 的空间结构为
的空间结构为(3)SiC的立方晶胞结构如图1所示,已知;1号C原子的坐标参数为(
 ,
, ,
, ),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
①GaN晶体中N原子的杂化轨道类型为
②GaN晶体的密度为
您最近半年使用:0次
3 . 镓 、铟
、铟 都是典型的稀有分散元素。回答下列问题:
都是典型的稀有分散元素。回答下列问题:
(1)基态 原子的核外价电子排布式为
原子的核外价电子排布式为_____ ,最高能级电子的电子云形状为_____ 。
(2)一种含镓药物的合成方法如图所示: 原子的杂化方式为
原子的杂化方式为_____ , 化合物
化合物 中含有的
中含有的 键的物质的量为
键的物质的量为_____ 。化合物Ⅰ中所含元素的电负性由大到小的顺序为_____ (用元素符号表示)。
②化合物Ⅱ中 的配位数为
的配位数为_____ ,
_____ 。
(3)一种由 组成的晶体属四方晶系,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞棱边夹角均为 ,其晶胞结构如图。
,其晶胞结构如图。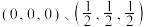 。则C点原子的分数坐标为
。则C点原子的分数坐标为_____ 。
② 表示阿伏加德罗常数的值,该晶体的密度为
表示阿伏加德罗常数的值,该晶体的密度为_____ (用含 的代数式表示)
的代数式表示) 。
。
 、铟
、铟 都是典型的稀有分散元素。回答下列问题:
都是典型的稀有分散元素。回答下列问题:(1)基态
 原子的核外价电子排布式为
原子的核外价电子排布式为(2)一种含镓药物的合成方法如图所示:

 原子的杂化方式为
原子的杂化方式为 化合物
化合物 中含有的
中含有的 键的物质的量为
键的物质的量为②化合物Ⅱ中
 的配位数为
的配位数为
(3)一种由
 组成的晶体属四方晶系,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞棱边夹角均为 ,其晶胞结构如图。
,其晶胞结构如图。
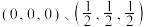 。则C点原子的分数坐标为
。则C点原子的分数坐标为②
 表示阿伏加德罗常数的值,该晶体的密度为
表示阿伏加德罗常数的值,该晶体的密度为 的代数式表示)
的代数式表示) 。
。
您最近半年使用:0次
名校
解题方法
4 . A、B、C、D、E是原子序数依次增大的五种短周期元素,F为第四周期元素。请根据下列相关信息回答问题。
(1)C离子的核外电子的轨道表示式是___________ 。
(2)F位于元素周期表第___________ 族,属于___________ 区。
(3)A、E的最高价氧化物对应的水化物酸性更强的是___________ (填化学式)。
(4)B、C和E元素的电负性由大到小的顺序是___________ (填元素符号)。
(5)常温常压下A的氢化物极易溶于水,从微粒间相互作用的角度分析原因:___________ (写出两条)。
(6)从原子结构的角度解释元素D的第一电离能高于同周期相邻元素的原因:___________ 。
| 元素 | 相关信息 |
| A | 基态原子的p轨道处于半充满状态 |
| B | 原子核外s能级上的电子总数与p能级上的电子总数相等,第一电离能低于同周期相邻元素 |
| C | 在同周期元素中,原子半径最大、电负性最小 |
| D | 电离能/(kJ•mol-1)数据:I1=740;I2=1500;I3=7700;I4=10500…… |
| E | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| F | 在周期表的第7纵列 |
(2)F位于元素周期表第
(3)A、E的最高价氧化物对应的水化物酸性更强的是
(4)B、C和E元素的电负性由大到小的顺序是
(5)常温常压下A的氢化物极易溶于水,从微粒间相互作用的角度分析原因:
(6)从原子结构的角度解释元素D的第一电离能高于同周期相邻元素的原因:
您最近半年使用:0次
名校
5 . 下面关于四种短周期元素的原子比较正确的是
①基态原子的电子排布式: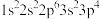 ;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子
;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子
①基态原子的电子排布式:
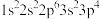 ;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子
;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子| A.最高正化合价:④=①>②>③ | B.原子半径:③>②>①>④ |
| C.电负性;③>②>①>④ | D.第一电离能:④>①>②>③。 |
您最近半年使用:0次
2024-04-11更新
|
182次组卷
|
2卷引用:陕西省西安市铁一中学2023-2024学年高二下学期第一次月考化学试题
6 . 有五种短周期元素,它们的结构或性质等信息如下表所示:
请根据表中信息回答下列问题:
(1)A元素基态原子的核外电子排布式为______________ 。
(2)B元素在元素周期表中的位置为_________ ;离子半径:B___________ (填“>”或“<”)A。
(3)C元素基态原子的核外电子轨道表示式为________ ,其原子核外有_______ 个未成对电子,能量最高的电子排布在_______ 轨道上。
(4)D元素基态原子的核外电子排布式为______  的结构示意图为
的结构示意图为__________ 。
(5)C、E元素的第一电离能的大小关系是_______ (用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是______ (填元素符号),CD3与水反应后的产物是______ (填化学式)。
| 元素 | 结构或性质 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
(1)A元素基态原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素基态原子的核外电子轨道表示式为
(4)D元素基态原子的核外电子排布式为
 的结构示意图为
的结构示意图为(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是
您最近半年使用:0次
名校
解题方法
7 . X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如表。下列说法不正确的是
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层的2倍 |
| Y | Y的基态原子最外层电子排布式为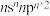 |
| Z | Z存在质量数为23、中子数为12的核素 |
| W | W有多种化合价,其在溶液中生成的白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
| A.W是Fe元素 | B.X的电负性比Y的小 |
C. 中阴离子和阳离子个数比为 中阴离子和阳离子个数比为 | D. 是一种直线形分子 是一种直线形分子 |
您最近半年使用:0次
名校
解题方法
8 . 以下有关元素性质的说法正确的是
| A.①Na、K、Rb,②N、P、As,③O、S、Se,④S、P、Cl,元素的电负性依次增大的是④ |
B.某元素气态基态原子的逐级电离能( )分别为738、1451、7733、10540、13630、17995、21703,该元素位于第ⅢA族 )分别为738、1451、7733、10540、13630、17995、21703,该元素位于第ⅢA族 |
C.下列原子中,①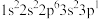 、② 、②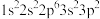 、③ 、③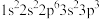 、④ 、④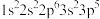 ,对应的第一电离能最大的是④ ,对应的第一电离能最大的是④ |
D.以下原子中,①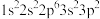 、② 、② 、③ 、③ 、④ 、④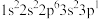 ,半径最大的是① ,半径最大的是① |
您最近半年使用:0次
名校
9 . 已知A、B、C、D、E是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
下列说法正确的是
| 元素 | 元素性质或原子结构 |
| A | 原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B | 原子最高能级的不同轨道都有电子,且自旋状态相同 |
| C | 所有元素中电负性最大的元素 |
| D | 位于周期表中第4纵列 |
| E | 基态原子M层全充满,最高能级的原子轨道半充满的主族元素 |
| A.最高价氧化物对应水化物的酸性强弱:C>B>A |
| B.B元素的原子核外电子有7种空间运动状态 |
| C.D元素基态原子的最高能层有4个电子 |
D.E的基态原子的简化电子排布式为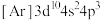 |
您最近半年使用:0次
名校
10 . 现有四种元素,其中两种元素基态原子的电子排布式如下:①1s22s22p63s23p2②1s22s22p63s23p3,另两种元素的价电子排布式为③2s22p3④2s22p4,则下列有关比较中正确的是
| A.原子半径:①>②>④>③ | B.第一电离能:④>③>②>① |
| C.电负性: ④>③>②>① | D.最高正化合价:④>③=②>① |
您最近半年使用:0次
2024-04-08更新
|
267次组卷
|
2卷引用:陕西省宝鸡市金台区2023-2024学年高二上学期期末检测化学试题



