名校
1 . 晶体世界丰富多彩、复杂多样,各类晶体具有的不同结构特点,决定着它们具有不同的性质和用途。氢化铝钠 是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。设阿伏加德罗常数的值为
是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。设阿伏加德罗常数的值为 下列说法错误的是
下列说法错误的是
 是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。设阿伏加德罗常数的值为
是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。设阿伏加德罗常数的值为 下列说法错误的是
下列说法错误的是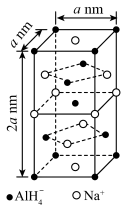
A. 中中心原子 中中心原子 的杂化方式为 的杂化方式为 杂化 杂化 |
B. 晶体中,与 晶体中,与 紧邻且等距的 紧邻且等距的 有4个 有4个 |
C. 晶体的密度为 晶体的密度为 |
D.若 晶胞上下面心处的 晶胞上下面心处的 被 被 取代,得到的晶体的化学式为 取代,得到的晶体的化学式为 |
您最近一年使用:0次
2024-05-30更新
|
225次组卷
|
2卷引用:河北省保定市九校2024届高三下学期二模化学试题
名校
解题方法
2 . 硫酸钴可用于电镀、碱性电池、生产含钴颜料,有着较为广泛的用途.由含钴矿(主要成分为 ,含有少量
,含有少量 的氧化物及有机物等)制备硫酸钴,并实现
的氧化物及有机物等)制备硫酸钴,并实现 元素的回收流程如图:
元素的回收流程如图:
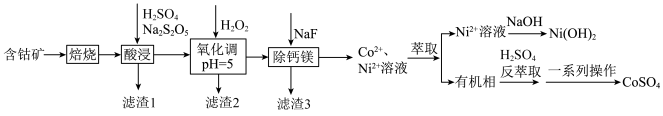
已知:① ;
;
②焦亚硫酸钠 常用作食品抗氧化剂;
常用作食品抗氧化剂;
③氧化性: .
.
回答下列问题:
(1)滤渣1的成分为___________________________ .
(2)酸浸工序发生的主要反应的化学方程式是_______________________ .
(3)氧化调 工序中,
工序中, 的作用是
的作用是__________________ (用离子方程式表示);调 时,最好选择
时,最好选择____________ .
a. b.
b. c.
c.
(4)萃取后, 浓度为
浓度为 ,当沉镍率达到99%时,溶液中
,当沉镍率达到99%时,溶液中 浓度为
浓度为____________  .
.
(5)向除杂后的溶液中,加入有机酸萃取剂 ,发生反应:
,发生反应: ,实验发现,随着
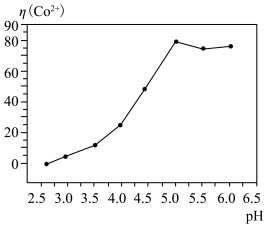
,实验发现,随着 的增大,萃取率逐渐升高,这是由于
的增大,萃取率逐渐升高,这是由于______________________ ,当 时,萃取率最高.
时,萃取率最高.
(6)硫酸钴可用于生产钴酞菁,酞菁和钴酞菁的分子结构如图所示.酞菁分子中所有原子共平面,则氮原子的杂化方式为____________ .钴酞菁分子中,氮原子与钴离子形成____________ 键.

 ,含有少量
,含有少量 的氧化物及有机物等)制备硫酸钴,并实现
的氧化物及有机物等)制备硫酸钴,并实现 元素的回收流程如图:
元素的回收流程如图:
已知:①
 ;
;②焦亚硫酸钠
 常用作食品抗氧化剂;
常用作食品抗氧化剂;③氧化性:
 .
.回答下列问题:
(1)滤渣1的成分为
(2)酸浸工序发生的主要反应的化学方程式是
(3)氧化调
 工序中,
工序中, 的作用是
的作用是 时,最好选择
时,最好选择a.
 b.
b. c.
c.
(4)萃取后,
 浓度为
浓度为 ,当沉镍率达到99%时,溶液中
,当沉镍率达到99%时,溶液中 浓度为
浓度为 .
.(5)向除杂后的溶液中,加入有机酸萃取剂
 ,发生反应:
,发生反应: ,实验发现,随着
,实验发现,随着 的增大,萃取率逐渐升高,这是由于
的增大,萃取率逐渐升高,这是由于 时,萃取率最高.
时,萃取率最高.
(6)硫酸钴可用于生产钴酞菁,酞菁和钴酞菁的分子结构如图所示.酞菁分子中所有原子共平面,则氮原子的杂化方式为

您最近一年使用:0次
2024-03-18更新
|
288次组卷
|
3卷引用:河北省保定市部分高中2023-2024学年高三下学期开学化学试题
解题方法
3 . 硼是一种用途广泛的工业原料,除了用于生产硼砂、硼酸和硼的各种化合物外,在制备储氢材料方面也有重要的用途,试回答下列问题:
(1)Ti(BH4)3是一种储氢材料,由TiCl4和LiBH4反应制得。基态Ti原子的核外电子排布式为___________ , 的价层电子对数是
的价层电子对数是___________ 。
(2)过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1,则Q元素的名称为___________ ;基态Q原子核外成对电子数和未成对电子数之比为___________ 。
(3)氨硼烷(NH3BH3)含氢量高,热稳定性好,是一种具有潜力的固体储氢材料,在四氢呋喃(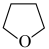 )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: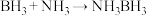 。
。
①测定晶体结构最常用的方法为___________ 。
②常温下,四氢呋喃在水中的溶解度大于环戊烷,其原因可能是___________ 。_
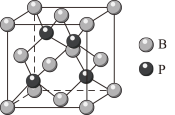
③硼与磷形成的一种晶体结构如图,晶体中离B原子最近的P原子有___________ 个;每个晶胞中的原子总数为___________ 。
(1)Ti(BH4)3是一种储氢材料,由TiCl4和LiBH4反应制得。基态Ti原子的核外电子排布式为
 的价层电子对数是
的价层电子对数是(2)过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1,则Q元素的名称为
(3)氨硼烷(NH3BH3)含氢量高,热稳定性好,是一种具有潜力的固体储氢材料,在四氢呋喃(
 )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: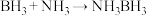 。
。①测定晶体结构最常用的方法为
②常温下,四氢呋喃在水中的溶解度大于环戊烷,其原因可能是
③硼与磷形成的一种晶体结构如图,晶体中离B原子最近的P原子有

您最近一年使用:0次
解题方法
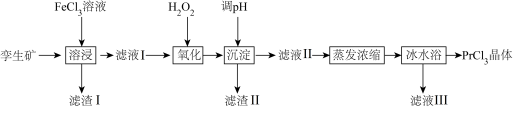
4 . 无水氯化镨( )是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、
)是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、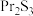 、
、 等)制备氯化镨晶体(
等)制备氯化镨晶体(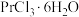 )。
)。
已知:① ;
;
② ;
;
③该条件下,溶液中部分金属离子生成氢氧化物开始沉淀和沉淀完全时的pH如表所示:
④沉淀时加入氨水逐步调节溶液的pH至6.5,此时滤渣Ⅱ中不含Pr的化合物。
回答下列问题:
(1)为了提高镨元素的浸出率,可采取的措施有___________ (填一种即可)。
(2)滤渣Ⅰ的主要成分为 和S:
和S:
①写出 的一种用途:
的一种用途:___________ 。
②S可用来处理体温计破碎时渗出的液态Hg,还可用来制黑火药(由硫黄粉、硝酸钾和木炭混合而成,爆炸时的生成物为硫化钾、氮气和二氧化碳),写出黑火药爆炸时发生反应的化学方程式:___________ 。
(3)加入 的目的是
的目的是___________ ,其发生反应的离子方程式为___________ , 中氧原子的杂化方式为
中氧原子的杂化方式为___________ 。
(4)滤渣Ⅱ的主要成分为___________ (填化学式)。
(5)利用表中的数据求出
___________ 。
(6) 利用电解法可以生产金属错。先将氯化镨与工业纯KCl配成二元电解质体系( ),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。

①M电极与电源的___________ (填“正极”或“负极”)相连。
②电池工作时,每转移 个电子,此时产生的气体的体积为
个电子,此时产生的气体的体积为___________ L(已换算成标准状况下)。
 )是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、
)是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、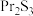 、
、 等)制备氯化镨晶体(
等)制备氯化镨晶体(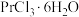 )。
)。
已知:①
 ;
;②
 ;
;③该条件下,溶液中部分金属离子生成氢氧化物开始沉淀和沉淀完全时的pH如表所示:
| 金属离子 |  |  |  |
| 开始沉淀的pH | 5.4 | 2.2 | 7.5 |
沉淀完全( )时的pH )时的pH | 6.4 | 3.2 | 9.0 |
回答下列问题:
(1)为了提高镨元素的浸出率,可采取的措施有
(2)滤渣Ⅰ的主要成分为
 和S:
和S:①写出
 的一种用途:
的一种用途:②S可用来处理体温计破碎时渗出的液态Hg,还可用来制黑火药(由硫黄粉、硝酸钾和木炭混合而成,爆炸时的生成物为硫化钾、氮气和二氧化碳),写出黑火药爆炸时发生反应的化学方程式:
(3)加入
 的目的是
的目的是 中氧原子的杂化方式为
中氧原子的杂化方式为(4)滤渣Ⅱ的主要成分为
(5)利用表中的数据求出

(6) 利用电解法可以生产金属错。先将氯化镨与工业纯KCl配成二元电解质体系(
 ),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
①M电极与电源的
②电池工作时,每转移
 个电子,此时产生的气体的体积为
个电子,此时产生的气体的体积为
您最近一年使用:0次
名校
解题方法
5 . 自然界中不存在氟的单质,得到单质氟的过程中,不少科学家为此献出了宝费的生命。1886年,法国化学家莫瓦桑发明了莫氏电炉,用电解法成功地制取了单质氟,因此荣获1906年诺贝尔化学奖,氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有_______ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为_______ 。
(2)氟气可以用于制取情性强于N2的保护气SF6,也可以用于制取聚合反应的催化剂PF3,PF3可以作为工业制取硅单质的中间物质(SiF4)的原料。
①SiF4分子的空间结构为_______ 。
②S、P、Si的第一电离能由大到小的顺序为_______ 。
(3)氟气可以用于制取高化学稳定性材料聚四氟乙烯的原料四氟乙烯(C2F4),50g四氟乙烯含σ键的数目为_______ 。
(4)工业上电解Al2O3制取单质铝,常利用冰晶石Na3AlF6降低Al2O3的熔点。Na、Al、F的电负性由小到大的顺序为_______ ,工业上不用电解AlCl3制取铝的原因为_______ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取情性强于N2的保护气SF6,也可以用于制取聚合反应的催化剂PF3,PF3可以作为工业制取硅单质的中间物质(SiF4)的原料。
①SiF4分子的空间结构为
②S、P、Si的第一电离能由大到小的顺序为
(3)氟气可以用于制取高化学稳定性材料聚四氟乙烯的原料四氟乙烯(C2F4),50g四氟乙烯含σ键的数目为
(4)工业上电解Al2O3制取单质铝,常利用冰晶石Na3AlF6降低Al2O3的熔点。Na、Al、F的电负性由小到大的顺序为
您最近一年使用:0次
2024-01-11更新
|
87次组卷
|
3卷引用:河北省石家庄市第二十四中学2023-2024学年高二上学期12月月考化学试题
6 . 每谈及CO时总把它与有毒气体并列视之,其实CO也是一种用途相当广泛的化工基础原料。随着化学的日益发展,CO可以合成多种重要的化工产品,如在一定条件:CH2=CH2+CO+H2O→CH3CH2COOH,设NA为阿伏加德罗常数的值,下列说法正确的是
| A.28g由CH2=CH2和CO组成的混合气体中所含原子数可能为4NA |
| B.1molCH3CH2COOH与Na2CO3溶液反应最多产生CO2分子的数目为NA |
| C.标准状况下,22.4LH2O含极性共价键的数目为2NA |
| D.CH3CH2COOH中三个C原子的杂化方式均不相同 |
您最近一年使用:0次
名校
解题方法
7 . Ⅰ、由CO2、甲醇为原料合成绿色化学品碳酸二甲酯(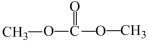 )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
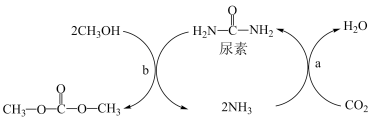
(1)下列说法不正确的是___________ (填字母)。
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.NH3极易溶解在水中,只因氨分子与水分子间形成了氢键
C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅱ、硫元素在化合物中常表现出多种化合价,它的许多化合物在研究和生产中有许多重要用途。回答下列问题:
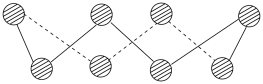
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是___________ 。
(3) 的电子式是
的电子式是___________ ,依据 理论推测
理论推测 的空间构型为
的空间构型为___________ ,常温下 是气体而
是气体而 是液体的原因是
是液体的原因是___________ 。
(4) 的键角
的键角___________  的键角(填“大于”或“小于”),理由是
的键角(填“大于”或“小于”),理由是___________ 。
(5) 在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方
在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方 晶体结构如图所示。
晶体结构如图所示。
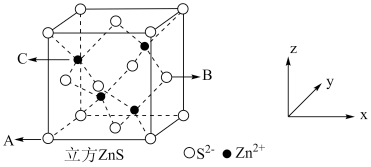
①已知A、B点的原子坐标分别为 和
和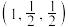 ,则C点的原子坐标为
,则C点的原子坐标为___________ ;
②若晶胞棱长为 ,密度为
,密度为___________  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
(1)下列说法不正确的是
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.NH3极易溶解在水中,只因氨分子与水分子间形成了氢键
C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅱ、硫元素在化合物中常表现出多种化合价,它的许多化合物在研究和生产中有许多重要用途。回答下列问题:
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是

(3)
 的电子式是
的电子式是 理论推测
理论推测 的空间构型为
的空间构型为 是气体而
是气体而 是液体的原因是
是液体的原因是(4)
 的键角
的键角 的键角(填“大于”或“小于”),理由是
的键角(填“大于”或“小于”),理由是(5)
 在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方
在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方 晶体结构如图所示。
晶体结构如图所示。
①已知A、B点的原子坐标分别为
 和
和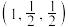 ,则C点的原子坐标为
,则C点的原子坐标为②若晶胞棱长为
 ,密度为
,密度为 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
2022-09-05更新
|
351次组卷
|
6卷引用:河北省昌黎第一中学2023届高三下学期第五次调研考试化学试题
名校
解题方法
8 . NH3与甲醛CH2O反应可以制备乌洛托品(六亚甲基四胺,分子结构为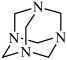 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
(1)基态氮原子的价电子轨道表达式为___________ ,第三电离能I3(C)___________ I3(N)(填“>”或“<)。
(2)NH3的空间构型为___________ ,CH2O中C采取的杂化类型为___________ 。CH2O中碳氢键与NH3中氮氢键相比,键长较长的是___________ 。
(3)乌洛托品为___________ (填“极性”或“非极性”)分子,分子中的所有N原子呈正四面体分布,所有C原子呈___________ 几何体分布,该分子可与H+形成配位键,电子对给予体为___________ 原子。
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为___________ 。乌洛托品比金刚烷(C10H16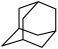 )水溶性更高,理由是
)水溶性更高,理由是___________ 。
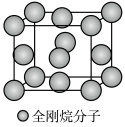
(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为___________ g/cm3。
 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:(1)基态氮原子的价电子轨道表达式为
(2)NH3的空间构型为
(3)乌洛托品为
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为
 )水溶性更高,理由是
)水溶性更高,理由是(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为

您最近一年使用:0次
2022-03-27更新
|
625次组卷
|
5卷引用:河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)
(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)四川省南充市2022届高三 适应性考试(二模)理综化学试题贵州省贵阳市五校2021-2022学年高三下学期联考理科综合化学试题(七)湖南省湘西自治州古丈县第一中学2021-2022学年高三下学期第二次模拟化学试题湖南省邵阳市第二中学2022-2023学年高三上学期第五次月考化学试题
名校
解题方法
9 . 根据所学内容填空:
(1)有下列物质:①HF、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是_______ (填序号,下同),既有 键又有
键又有 键的是
键的是_______ 。
(2)下列分子中,空间构型为正四面体且键角为109°28′的是_______ 。
a. b.
b. c.
c.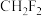 d.
d. e.
e. f.
f.
(3) 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
(4)丙烯腈分子( )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为_______ 。
(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。
① 的酸性比
的酸性比
_______ (填“强”或“弱”)。 离子的空间构型为
离子的空间构型为_______ 。
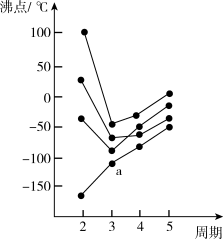
②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (化学式)。
(1)有下列物质:①HF、②
 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体且键角为109°28′的是
a.
 b.
b. c.
c.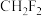 d.
d. e.
e. f.
f.
(3)
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(4)丙烯腈分子(
 )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。
①
 的酸性比
的酸性比
 离子的空间构型为
离子的空间构型为②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是
您最近一年使用:0次
2022-04-09更新
|
433次组卷
|
3卷引用:河北省衡水市第二中学2021-2022学年高二下学期期中考试化学试题
名校
10 . 2020年11月7日是被誉为“中国稀土之父”的徐光宪院士诞辰100周年纪念日,社会各界举行了各式各样的纪念活动。已知钪(Sc)是17种稀土元素之一,钪单质及其化合物用途广泛。请回答下列问题:
(1)与Sc同周期且其基态原子的未成对电子数与Sc原子相同的元素有___________ 种。
(2)元素呈气态时,从它的阳离子中将一个电子移至无穷远处时所需做的功,称为该元素的电离势,单位为电子伏特(ev)。Sc的三种气态离子Sc+、Sc2+、Sc3+的电离势分别为6.54ev、12.80ev、24.76ev,上述三种气态离子的电离势依次增大的原因为___________ 。
(3)我国科学家首次合成并晶体结构表征了稀土金属末端氮宾配合物-钪末端氮宾配合物,该配合物的分子结构如图所示。

①该配合物分子中碳原子的杂化方式为___________ ;与Sc原子形成配位键的N原子个数为___________ 。
②该配合物中各元素第一电离能从大到小的顺序为___________ 。
(1)与Sc同周期且其基态原子的未成对电子数与Sc原子相同的元素有
(2)元素呈气态时,从它的阳离子中将一个电子移至无穷远处时所需做的功,称为该元素的电离势,单位为电子伏特(ev)。Sc的三种气态离子Sc+、Sc2+、Sc3+的电离势分别为6.54ev、12.80ev、24.76ev,上述三种气态离子的电离势依次增大的原因为
(3)我国科学家首次合成并晶体结构表征了稀土金属末端氮宾配合物-钪末端氮宾配合物,该配合物的分子结构如图所示。

①该配合物分子中碳原子的杂化方式为
②该配合物中各元素第一电离能从大到小的顺序为
您最近一年使用:0次
2021-05-30更新
|
265次组卷
|
2卷引用:河北省正中实验中学2020-2021学年高二第二学期第一次月考化学试题



