名校
解题方法
1 . 下列对有关事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 水的沸点比硫化氢的沸点高 | 水分子间形成氢键 |
| B | 在CS2中的溶解度:CCl4>H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
| C | 用质谱仪检测乙酸时,谱图出现了质荷比为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
| D | 稳定性:[Cu(H2O)4]2+<[Cu(NH3)4]2+ | N的电负性小于O的电负性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-19更新
|
309次组卷
|
3卷引用:河南省南阳市华龙高中2023-2024学年高二下学期3月月考化学试题
名校
解题方法
2 . 回答下列问题
(1)钛在元素周期表中的位置___________ ,基态钛原子的价层电子轨道表示式为___________ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有___________ 种。下列状态的钛元素形成得微粒中,电离其最外层的一个电子所需能量最小的是___________ (填序号)。
A.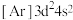 B.
B.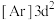 C.
C.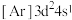 D.
D.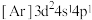
(2)第三周期元素中第一电离能介于Al和P的元素有___________ 种。与Co同周期,基态原子有1个未成对电子的元素有___________ 种。
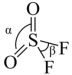
(3) 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
(4) 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为___________ ,其主要原因是___________ 。
(5)铜离子的一种配合物化学式为 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为___________ 。
(6)醋酸 中C原子的杂化类型为
中C原子的杂化类型为___________ 。
(7)等物质的量的 和
和 中,σ键数目之比
中,σ键数目之比___________ 。
(1)钛在元素周期表中的位置
A.
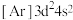 B.
B.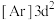 C.
C.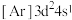 D.
D.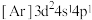
(2)第三周期元素中第一电离能介于Al和P的元素有
(3)
 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是
(4)
 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为(5)铜离子的一种配合物化学式为
 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为(6)醋酸
 中C原子的杂化类型为
中C原子的杂化类型为(7)等物质的量的
 和
和 中,σ键数目之比
中,σ键数目之比
您最近一年使用:0次
名校
3 . 有四种短周期元素,它们的结构、性质等信息如下表所述:
完成下列填空:
(1)A的离子结构示意图是_____________ ,元素 D在周期表中的位置是_____________________ 。
(2)基态 A原子第一电离能_________ 基态 B原子第一电离能(填“>”、“<”或“=”),基态 C原子核外电子共有_________ 种空间运动状态。
(3)单质 C的结构式是_________ ,其化学性质稳定的原因是_____________________ 。
(4)C元素的简单气态氢化物中心原子的杂化方式为_________ ,分子构型为_________ ,与 H2S分子内共价键键角相比,较大的是_________ 。
(5)D元素的气态氢化物与 HF分子相比,沸点较大的是_________ ,请说明原因_____________________ 。
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | 与  同周期,其最高价氧化物的水化物呈两性 同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物是自来水生产过程中常用的消毒杀菌剂 |
(1)A的离子结构示意图是
(2)基态 A原子第一电离能
(3)单质 C的结构式是
(4)C元素的简单气态氢化物中心原子的杂化方式为
(5)D元素的气态氢化物与 HF分子相比,沸点较大的是
您最近一年使用:0次
名校
解题方法
4 . 前四周期元素W、X、Y、Z和M的原子序数依次增大,W、X同周期,W、Z同主族,基态W原子核外电子有7种运动状态且第一电离能比X高,基态Y和 M最高能层电子数相同且其他能层均为全满状态,M为人类最早使用的金属,下列说法错误的是
| A.离子半径:Z>Y>X |
| B.简单氢化物的沸点:X>W>Z |
| C.化合物Y2X2、YW3中,同时含有离子键和非极性键 |
| D.M的某种氧化物对应的水化物可溶于W简单氢化物的水溶液中 |
您最近一年使用:0次
2024-03-09更新
|
329次组卷
|
4卷引用:河南省中原名校2023-2024学年高三下学期3月联考理科综合化学试题
名校
解题方法
5 . 味精能增加食品的鲜味,是一种常用的增味剂,其化学名称为谷氨酸钠(结构如图所示),下列有关谷氨酸钠的说法正确的是

| A.所有原子均满足8电子结构 |
| B.所有碳原子均采用sp3杂化 |
| C.既可形成分子间氢键又可形成分子内氢键 |
| D.常温下,可溶于水是因为存在C—H极性共价键 |
您最近一年使用:0次
2024-03-02更新
|
176次组卷
|
2卷引用:河南省许平汝名校2023-2024学年高二下学期开学化学试题
名校
解题方法
6 . DNA的部分结构如图所示,其中嘌呤( )为平面结构。
)为平面结构。

下列说法正确的是
 )为平面结构。
)为平面结构。
下列说法正确的是
A.元素的电负性: |
B.基态原子的价层空轨道数: |
C.上图中碱基互补配对时存在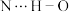 氢键 氢键 |
D.嘌呤中N原子的杂化轨道类型有 和 和 |
您最近一年使用:0次
名校
7 . 正硼酸( )是一种层状结构白色晶体,层内的
)是一种层状结构白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的是
分子通过氢键相连(如图)。下列有关说法正确的是
 )是一种层状结构白色晶体,层内的
)是一种层状结构白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的是
分子通过氢键相连(如图)。下列有关说法正确的是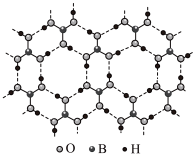
| A.正硼酸晶体属于共价晶体 | B. 分子的稳定性与氢键有关 分子的稳定性与氢键有关 |
C. 分子中B原子采用 分子中B原子采用 杂化 杂化 | D.含1mol 的晶体中有6mol氢键 的晶体中有6mol氢键 |
您最近一年使用:0次
2024-03-02更新
|
306次组卷
|
4卷引用:河南省驻马店市2023-2024学年高二下学期3月月考(大联考)化学试题
23-24高三下·四川雅安·开学考试
名校
8 . 山油柑碱(Acronycine)是一种广谱抗癌药,其某种合成路线如下,回答下列问题:_______ 。
(2)山油柑碱中含氧官能团有_______ (填名称),B的名称是_______ 。
(3)D→E的反应类型是_______ 。
(4)C→D的化学方程式为_______ 。
(5)在C的芳香族同分异构体中,同时符合下列条件的结构(不考虑立体异构)有_______ 种。①苯环上直接连接氨基(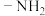 );②能发生银镜反应。其中核磁共振氢谱上有四组峰且峰的面积比
);②能发生银镜反应。其中核磁共振氢谱上有四组峰且峰的面积比 的结构简式为
的结构简式为_______ 。
(6)已知: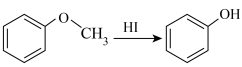 ,以间甲基苯酚为原料制备间羟基苯甲酸,设计合成路线
,以间甲基苯酚为原料制备间羟基苯甲酸,设计合成路线_______ (无机试剂和有机溶剂任选)。

(2)山油柑碱中含氧官能团有
(3)D→E的反应类型是
(4)C→D的化学方程式为
(5)在C的芳香族同分异构体中,同时符合下列条件的结构(不考虑立体异构)有
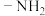 );②能发生银镜反应。其中核磁共振氢谱上有四组峰且峰的面积比
);②能发生银镜反应。其中核磁共振氢谱上有四组峰且峰的面积比 的结构简式为
的结构简式为(6)已知:
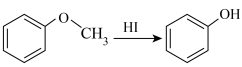 ,以间甲基苯酚为原料制备间羟基苯甲酸,设计合成路线
,以间甲基苯酚为原料制备间羟基苯甲酸,设计合成路线
您最近一年使用:0次
2024-03-01更新
|
197次组卷
|
4卷引用:T30-有机综合题
(已下线)T30-有机综合题四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学2024届四川省部分学校高三一模联考理科综合试题-高中化学(已下线)T36-有机推断题
名校
解题方法
9 . 离子液体因其不挥发性、无色、无臭、较好的化学稳定性被誉为二十一世纪的绿色化学溶剂,某离子液体(结构如下)在触觉传感器中应用广泛。X、Y、Z均为短周期主族元素,原子序数依次增大,Y是非金属性最强的元素。下列说法正确的是
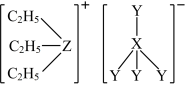
| A.原子半径:X>Y>Z |
| B.最高价氧化物的水化物的酸性:Y>Z>X |
| C.简单氢化物的沸点:Y>Z |
| D.该离子液体中各元素原子均满足8电子稳定结构 |
您最近一年使用:0次
2024-02-25更新
|
105次组卷
|
2卷引用:河南省漯河市2023-2024学年高三上学期期末质量监测化学试题
名校
10 . 下列有关物质结构与性质的说法错误的是
A. 所含元素中基态原子未成对电子数最多的是P 所含元素中基态原子未成对电子数最多的是P |
| B.HF在标准状况下为液态的重要原因是HF分子间存在氢键 |
| C.晶莹剔透的水晶中含有硅氧四面体结构 |
| D.石墨晶体的层状结构之间存在分子间作用力,因此具有导电性 |
您最近一年使用:0次



