1 . 同一短周期元素 、
、 、
、 、
、 的原子序数依次增大,其中
的原子序数依次增大,其中 被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是
被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是
 、
、 、
、 、
、 的原子序数依次增大,其中
的原子序数依次增大,其中 被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是
被认为目前形成化合物种类最多的元素,四种元素形成的某种化合物如图所示。下列说法错误的是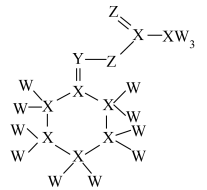
A.简单离子半径: |
B.元素的第一电离能: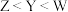 |
| C.分子中各原子最外层均满足8电子稳定结构 |
D.W的氢化物分子间形成了直线形氢键,故简单氢化物的沸点: |
您最近一年使用:0次
解题方法
2 . 结构决定性质。下列性质差异对应的解释错误的是
选项 | 性质差异 | 解释 |
A | 键角: | 电负性: |
B | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛可形成分子内氢键 |
C | pKa: | 极性: |
D | 熔点: | 晶体类型不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 同一主族元素形成的物质在结构和性质上往往具有一定的相似性。下列说法正确的是
| A.冰中1个H2O周围有4个紧邻分子,H2S晶体中1个H2S周围也有4个紧邻分子 |
| B.P和Cl可以形成PCl5分子,N和Cl也可以形成NCl5分子 |
C.Al(OH)3可与碱生成 ,B(OH)3也可与碱生成 ,B(OH)3也可与碱生成 |
| D.Cl2可与水生成HCl和HClO,F2也可与水生成HF和HFO |
您最近一年使用:0次
4 . 回答下列问题:
(1)符号“3px”没有给出的信息是_______。
(2)某元素基态原子4s轨道上有1个电子,则该元素基态原子价电子排布不可能是_______。
(3)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是_______。
(4)下列比较正确的是_______。
(5)下列实验事实不能用氢键来解释的是_______。
(6)由磷原子核形成的三种微粒:a. 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为_______ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为_______ 。
(7)比较H-O-H键角大小;H3O+_______ H2O(填“>”、“<”或“=”)。
(8)胍(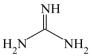 )分子中碳原子和氮原子共平面,胍中N杂化方式为
)分子中碳原子和氮原子共平面,胍中N杂化方式为_______ 。
(1)符号“3px”没有给出的信息是_______。
| A.能层 | B.能级 | C.电子云在空间的伸展方向 | D.电子的自旋方向 |
(2)某元素基态原子4s轨道上有1个电子,则该元素基态原子价电子排布不可能是_______。
| A.4s1 | B.3p64s1 | C.3d54s1 | D.3d104s1 |
(3)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是_______。
| A.HX | B.H2X | C.XH3 | D.XH4 |
(4)下列比较正确的是_______。
| A.酸性:H3PO4<H3AsO4 | B.熔点:MgO>CaO |
| C.离子半径:r(Al3+)>r(O2-) | D.键角:H2O>NH3 |
(5)下列实验事实不能用氢键来解释的是_______。
| A.CH4比SiH4稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
(6)由磷原子核形成的三种微粒:a.
 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为(7)比较H-O-H键角大小;H3O+
(8)胍(
 )分子中碳原子和氮原子共平面,胍中N杂化方式为
)分子中碳原子和氮原子共平面,胍中N杂化方式为
您最近一年使用:0次
名校
解题方法
5 . 聚吡咯作柔性电极材料,其单体为吡咯(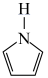 ),吡咯中所有原子共面,且分子中含有与苯类似的大π键(
),吡咯中所有原子共面,且分子中含有与苯类似的大π键(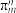 ,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数)。已知
,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数)。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.1mol吡咯中σ键数为 | B.吡咯中N原子的杂化轨道类型为 |
C.吡咯熔点远高于环戊二烯(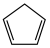 ) ) | D.吡咯中的大π键表示为 |
您最近一年使用:0次
名校
解题方法
6 .  是重要的半导体材料,
是重要的半导体材料, (镓)、P、
(镓)、P、 (砷)都是形成化合物半导体材料的重要元素.回答下列问题:
(砷)都是形成化合物半导体材料的重要元素.回答下列问题:
(1) 基态原子的电子占据了
基态原子的电子占据了_____________ 个能层,最高能级的电子排布式为_____________ ;
(2)元素周期表中,与P紧邻的4种元素中电负性最大的是_____________ (填元素符号)。 、P、S三种元素的第一电离能由大到小的顺序是
、P、S三种元素的第一电离能由大到小的顺序是_____________ ;
(3) 三者的沸点由高到低的顺序是
三者的沸点由高到低的顺序是__________________ ,原因是____________________________ ;
(4)白磷是由 分子形成的分子晶体,
分子形成的分子晶体, 分子呈正四面体结构,P原子位于正四面体的四个顶点.白磷易溶于
分子呈正四面体结构,P原子位于正四面体的四个顶点.白磷易溶于 ,难溶于水,原因是
,难溶于水,原因是________________________ ;
(5)采用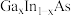 (镓铟砷)等材料,可提高太阳能电池的效率。
(镓铟砷)等材料,可提高太阳能电池的效率。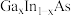 立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4个原子,则该晶胞中含有
立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4个原子,则该晶胞中含有_____________ 个砷原子;
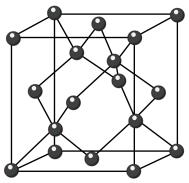
(6) 晶体的晶胞结构与金刚石相似(如图),设晶胞的边长为
晶体的晶胞结构与金刚石相似(如图),设晶胞的边长为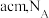 表示阿伏加德罗常数,则该晶体的密度为
表示阿伏加德罗常数,则该晶体的密度为_____________  。
。
 是重要的半导体材料,
是重要的半导体材料, (镓)、P、
(镓)、P、 (砷)都是形成化合物半导体材料的重要元素.回答下列问题:
(砷)都是形成化合物半导体材料的重要元素.回答下列问题:(1)
 基态原子的电子占据了
基态原子的电子占据了(2)元素周期表中,与P紧邻的4种元素中电负性最大的是
 、P、S三种元素的第一电离能由大到小的顺序是
、P、S三种元素的第一电离能由大到小的顺序是(3)
 三者的沸点由高到低的顺序是
三者的沸点由高到低的顺序是(4)白磷是由
 分子形成的分子晶体,
分子形成的分子晶体, 分子呈正四面体结构,P原子位于正四面体的四个顶点.白磷易溶于
分子呈正四面体结构,P原子位于正四面体的四个顶点.白磷易溶于 ,难溶于水,原因是
,难溶于水,原因是(5)采用
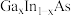 (镓铟砷)等材料,可提高太阳能电池的效率。
(镓铟砷)等材料,可提高太阳能电池的效率。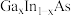 立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4个原子,则该晶胞中含有
立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4个原子,则该晶胞中含有(6)
 晶体的晶胞结构与金刚石相似(如图),设晶胞的边长为
晶体的晶胞结构与金刚石相似(如图),设晶胞的边长为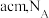 表示阿伏加德罗常数,则该晶体的密度为
表示阿伏加德罗常数,则该晶体的密度为 。
。
您最近一年使用:0次
2024-05-02更新
|
89次组卷
|
2卷引用:安徽省定远县第三中学2023-2024学年高二下学期4月月考化学试题
名校
7 . 一种能用于“点击反应”的新分子,结构如图所示,其中短周期主族元素W、X、Y、Z的原子序数依次增大,已知Y的原子序数是X的2倍,基态W原子价电子排布式为nsnnp2n-1。下列说法正确的是

| A.简单离子半径:Z>Y>X>W | B.Y的氧化物均为极性分子 |
| C.简单氢化物的沸点:X>Y | D.Z的所有含氧酸均为强酸 |
您最近一年使用:0次
名校
解题方法
8 . 关于氢键的下列说法中正确的是
| A.每个水分子内含有两个氢键 |
| B.冰、液态水、水蒸气中都存在氢键 |
| C.1个水分子最多可形成4个氢键 |
| D.HF的稳定性很强,是因为其分子间能形成氢键 |
您最近一年使用:0次
名校
解题方法
9 . 由四种短周期主族元素形成的某有机物甲的结构如图所示,甲分子中所有原子共平面,X、Y、Z、W的原子序数依次增大,Y、Z、W、X的原子半径依次减小。下列说法错误的是
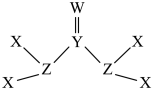
| A.通常状况下,由于甲分子间形成氢键使甲呈固态 |
B. 为直线形分子,其中2个Y原子均采取sp杂化 为直线形分子,其中2个Y原子均采取sp杂化 |
C.由于甲分子中所有原子共平面,所以甲分子中Z的杂化方式为 |
| D.电负性:Z<W,第一电离能:W>Z>Y |
您最近一年使用:0次
2024-04-11更新
|
202次组卷
|
2卷引用:安徽省合肥市第七中学2023-2024学年高二下学期第一次段考化学试卷
名校
解题方法
10 . 科教兴国,“可上九天揽月,可下五洋捉鳖”。下列说法正确的是
| A.“天舟六号”为中国空间站送去推进剂Xe气,Xe是第IA族元素 |
| B.火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO |
| C.我国科学家由嫦娥五号待回的月壤样品中,首次发现了天然玻璃纤维,该纤维中的主要氧化物SiO2属于分子晶体 |
| D.冰的密度比干冰的密度小,主要原因是冰分之间存在氢键 |
您最近一年使用:0次



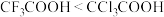
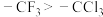
 (1040℃)
(1040℃) (178℃升华)
(178℃升华)

