名校
解题方法
1 . 某化学卷发水、烫发剂主要成分的结构如图所示,已知W、X、Y、Z、M均为短周期主族元素,且原子序数依次增大。下列说法正确的是
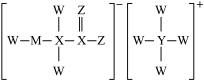
A.第一电离能大小比较: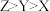 |
B.简单氢化物的沸点: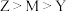 |
| C.X最高价氧化物对应的水化物能够促进水的电离 |
D.由W、X、Y、M四种元素组成的某种盐可与 发生显色反应 发生显色反应 |
您最近一年使用:0次
解题方法
2 . 硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)基态B原子中能量最高的电子所在的原子轨道的电子云在空间上有______ 个伸展方向,原子轨道呈______ 形。 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(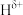 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(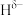 ),H、B、N电负性大小顺序是
),H、B、N电负性大小顺序是______ 。
(2)硼酸( )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。______ 。
②加热时,硼酸的溶解度增大,主要原因是______ 。
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的 而呈酸性。写出硼酸的电离方程式:
而呈酸性。写出硼酸的电离方程式:______ 。
(3)硼氢化钠( )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:______ 。
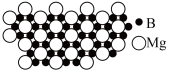
(4)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为______ 。
(1)基态B原子中能量最高的电子所在的原子轨道的电子云在空间上有
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(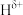 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(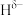 ),H、B、N电负性大小顺序是
),H、B、N电负性大小顺序是(2)硼酸(
 )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。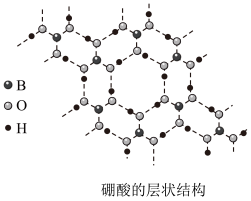
②加热时,硼酸的溶解度增大,主要原因是
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的
 而呈酸性。写出硼酸的电离方程式:
而呈酸性。写出硼酸的电离方程式:(3)硼氢化钠(
 )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:(4)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为
您最近一年使用:0次
3 . 一种可吸附甲醇的材料,其化学式为 ,部分晶体结构如下图所示,其中
,部分晶体结构如下图所示,其中 为平面结构。下列说法正确的是
为平面结构。下列说法正确的是
 ,部分晶体结构如下图所示,其中
,部分晶体结构如下图所示,其中 为平面结构。下列说法正确的是
为平面结构。下列说法正确的是
| A.基态原子的第一电离能:C<N<O |
B.该晶体中存在 氢键 氢键 |
| C.基态原子未成对电子数:B<C<O |
D.晶体中B、N和O原子轨道的杂化类型均为 |
您最近一年使用:0次
4 . 下列物质的性质可用氢键来解释的是
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.F2、Cl2、Br2、I2的熔、沸点依次升高 |
| C.CH3COOH、H—O—H、C2H5—OH中—OH上氢原子的活泼性依次减弱 |
| D.C2H5OH的沸点比CH3—O—CH3的沸点高 |
您最近一年使用:0次
5 . 铋及其化合物广泛应用于电子材料、医药等领域.一种以含铋烧渣(主要成分为 ,还含有少量
,还含有少量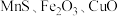 及
及 等)制取
等)制取 并回收锰的工艺流程如下:
并回收锰的工艺流程如下: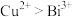 ;
;
② 易水解成
易水解成 沉淀;常温下,
沉淀;常温下, 存在的
存在的 范围约为
范围约为 ;回答下列问题:
;回答下列问题:
(1)基态锰原子的价电子排布式为____________ ;
(2)“水浸提锰”时,另加入少量稀硫酸可促进____________ (填化学式)溶解,进一步提高锰的浸取率;
(3)“浸出”时需要加入过量浓盐酸,其目的是____________ ;
(4)“滤渣2”的主要成分为Bi和____________ (填化学式);
(5)常温下,用铁氰化钾溶液检验“含 滤液”的现象为
滤液”的现象为____________ ;
(6)“脱氯”过程中发生主要反应的离子方程式为____________ ;
(7) 是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚(
是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚(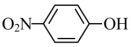 )等.对硝基苯酚的熔点高于邻硝基苯酚(
)等.对硝基苯酚的熔点高于邻硝基苯酚(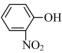 )的熔点,其原因是
)的熔点,其原因是____________________ ;
(8)我国科学家在新型二维半导体芯片材料——硒氧化铋的研究中取得突破性进展.硒氧化铋的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞参数为apm,apm,bpm;____________ (填标号); 周围紧邻的
周围紧邻的 共有
共有____________ 个;
③该晶体的密度为____________  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 ,还含有少量
,还含有少量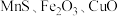 及
及 等)制取
等)制取 并回收锰的工艺流程如下:
并回收锰的工艺流程如下: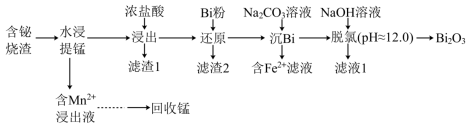
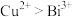 ;
;②
 易水解成
易水解成 沉淀;常温下,
沉淀;常温下, 存在的
存在的 范围约为
范围约为 ;回答下列问题:
;回答下列问题:(1)基态锰原子的价电子排布式为
(2)“水浸提锰”时,另加入少量稀硫酸可促进
(3)“浸出”时需要加入过量浓盐酸,其目的是
(4)“滤渣2”的主要成分为Bi和
(5)常温下,用铁氰化钾溶液检验“含
 滤液”的现象为
滤液”的现象为(6)“脱氯”过程中发生主要反应的离子方程式为
(7)
 是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚(
是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚( )等.对硝基苯酚的熔点高于邻硝基苯酚(
)等.对硝基苯酚的熔点高于邻硝基苯酚( )的熔点,其原因是
)的熔点,其原因是(8)我国科学家在新型二维半导体芯片材料——硒氧化铋的研究中取得突破性进展.硒氧化铋的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞参数为apm,apm,bpm;
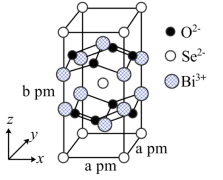
A.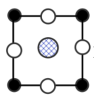 B.
B.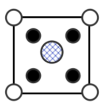 C.
C.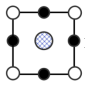 D.
D.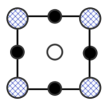
 周围紧邻的
周围紧邻的 共有
共有③该晶体的密度为
 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
6 . 下列关于物质的结构或性质的描述及解释都正确的是
| A.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强 |
B.键角: 是由于 是由于 中 中 上孤电子对数比 上孤电子对数比 分中 分中 上的少 上的少 |
C.已知: 元素和 元素和 元素的电负性差值大于 元素的电负性差值大于 元素和 元素和 元素的电负性差值,故: 元素的电负性差值,故: 分子的极性大于 分子的极性大于 |
D.稳定性: ,是由于水分子间存在氢键 ,是由于水分子间存在氢键 |
您最近一年使用:0次
名校
7 . 钛被称为继铁、铝之后的“第三金属”。一种制备金属钛的工艺流程如下所示:___________ 。
(2)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与CCl4相似。试预测CCl4的沸点___________ 136℃(填“>”“<”或“=”)并阐述推测理由___________ 。
(3)纳米TiO2是一种应用广泛的催化剂,其催化作用的一个实例如下所示:___________ 。
(4)硫酸氧钛晶体中阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示。该阳离子中Ti与O的原子数之比为___________ 。___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。

(2)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与CCl4相似。试预测CCl4的沸点
(3)纳米TiO2是一种应用广泛的催化剂,其催化作用的一个实例如下所示:

(4)硫酸氧钛晶体中阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示。该阳离子中Ti与O的原子数之比为


您最近一年使用:0次
2024-05-05更新
|
121次组卷
|
2卷引用:福建省福州市闽侯县第一中学2023-2024学年高二下学期3月月考化学试题
名校
8 . 下列有关物质结构的说法正确的是
| A.邻羟基苯甲醛的沸点高于对羟基苯甲醛的沸点 |
| B.第四周期元素中,基态原子的未成对电子数与钛相同的有Ni、Ge、Se |
C.基态铜原子( )的价层电子排布式: )的价层电子排布式: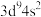 |
| D.比较Fe和Mn的第三电离能,可得I3(Fe)大于I3(Mn) |
您最近一年使用:0次
名校
解题方法
9 . 下列有关说法不正确 的是
| A.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释 |
B.乳酸( )分子中含有一个手性碳原子 )分子中含有一个手性碳原子 |
| C.水分子间存在氢键,故水很稳定,1000℃以上才会部分分解 |
| D.1个N2分子中的π键与1个CO2分子中的π键的数目之比为1:1 |
您最近一年使用:0次
名校
解题方法
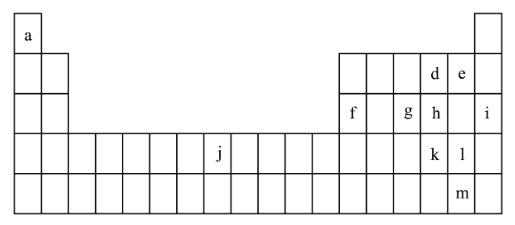
10 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:_______ (用元素符号填空)。
(2)上述元素形成的三种化合物熔点如下表:
请解释其熔点变化原因_______ (用对应微粒的化学式回答)。
(3)j的单质在锻压或捶打时,密堆积层的金属原子之间产生滑动,但金属键仍存在,因此j的单质具有良好的_______ 。
(4)用高能射线照射液态a2d时,一个a2d分子能释放出一个电子,同时产生一种阳离子,该阳离子的化学式_______ (填微粒符号);释放出来的电子可以被若干a2d分子形成的“网”捕获而形成a2d合电子,你认为a2d分子间能形成“网”的原因_______ 。
(5)k常用作光敏材料,基态k原子的外围电子排布式为____ ;kd3的空间构型是_____ 。
(2)上述元素形成的三种化合物熔点如下表:
| 化学式 | fe3 | fl3 | fm3 |
| 熔点/℃ | 1290 | 97.5 | 188 |
(3)j的单质在锻压或捶打时,密堆积层的金属原子之间产生滑动,但金属键仍存在,因此j的单质具有良好的
(4)用高能射线照射液态a2d时,一个a2d分子能释放出一个电子,同时产生一种阳离子,该阳离子的化学式
(5)k常用作光敏材料,基态k原子的外围电子排布式为
您最近一年使用:0次



