解题方法
1 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:正戊烷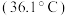 高于新戊烷 高于新戊烷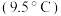 | 分子间作用力 |
| B | 熔点: | 晶体类型 |
| C | 酸性: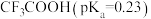 远强于 远强于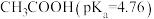 | 羟基极性 |
| D | 溶解度:甘油(丙三醇)与水互溶 | 分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 回答下列问题:
(1)乙二胺( )是一种有机化合物,乙二胺能与
)是一种有机化合物,乙二胺能与 、
、 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是___________ ,其中与乙二胺形成的化合物稳定性相对较高的是___________ (填“ ”或“
”或“ ”)。
”)。
(2)元素As与N同族。预测As的氢化物的键角比 的键角
的键角___________ (填“大”或“小”),其判断理由是___________ 。
(3)苯胺(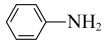 )与甲苯(
)与甲苯(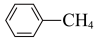 )的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(11.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(11.6℃),原因是___________ 。 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:___________ (用n代表P原子数)。
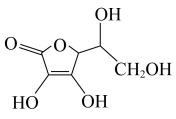
(4)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:___________ (填“难溶于水”或“易溶于水”)。
(1)乙二胺(
 )是一种有机化合物,乙二胺能与
)是一种有机化合物,乙二胺能与 、
、 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是 ”或“
”或“ ”)。
”)。(2)元素As与N同族。预测As的氢化物的键角比
 的键角
的键角(3)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(11.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(11.6℃),原因是 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
(4)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:
您最近一年使用:0次
3 . 烃及其衍生物是重要的化工原料,研究其性质具有得要意义。下列说法正确的是
A. 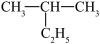 名称为2-乙基丙烷 名称为2-乙基丙烷 |
B.等质量的乙烯和聚乙烯完全燃烧生成 的物质的量相等 的物质的量相等 |
| C.沸点:乙醇>甲醚,CH3CH(CH3)CH3>CH3CH2CH2CH3 |
| D.1mol丙烯与氯气先发生加成反应,然后发生取代反应,最多消耗氯气6mol |
您最近一年使用:0次
4 . 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有________ ,其中能量较高的是________ 。(填标号)
A. B.
B. C.
C.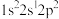 D.
D.
(2)基态Br原子的核外电子排布式为________ 。
(3) 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是________ ,中心离子的配位数为________ 。
(4)Kr是第四周期的稀有气体元素,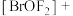 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为________ 。
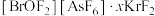 晶体中的微粒间作用力有
晶体中的微粒间作用力有________ (填标号)。
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在 形式,画出
形式,画出 的链状结构
的链状结构________ 。
(6)四氟乙烯 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为________ 和________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________ 。
(1)氟原子激发态的电子排布式有
A.
 B.
B. C.
C.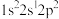 D.
D.
(2)基态Br原子的核外电子排布式为
(3)
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(4)Kr是第四周期的稀有气体元素,
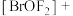 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为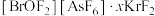 晶体中的微粒间作用力有
晶体中的微粒间作用力有a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在
 形式,画出
形式,画出 的链状结构
的链状结构(6)四氟乙烯
 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为
您最近一年使用:0次
解题方法
5 . 下列对一些实验事实的理论解释,正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 溴单质、碘单质在四氯化碳中的溶解度比在水中大 | 溴单质、碘单质和四氯化碳都为非极性分子 |
| B | 在常温常压下,1体积水可以溶解700体积氨气 | 氨是极性分子且有氢键影响 |
| C | 卤素单质从 到 到 ,在常温、常压下的聚集状态由气态、液态到固态 ,在常温、常压下的聚集状态由气态、液态到固态 | 范德华力逐渐减小 |
| D | HF的沸点高于HCl | H-F的键长比H-Cl的短 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 尿素 作为一种中性肥料,适用于各种土壤和植物。
作为一种中性肥料,适用于各种土壤和植物。
(1)十九世纪初,用氰酸银 与
与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。
,实现了由无机物到有机物的合成。
① 位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为
位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为______ 。
② 与
与 中的C原子杂化方式分别为
中的C原子杂化方式分别为______ 、______ 。
(2)二十世纪初,工业上以 和
和 为原料在一定温度和压强下合成
为原料在一定温度和压强下合成 :
: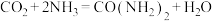 。
。
①上述物质中,属于非极性分子的是______ (填化学式)。
②键角比较:
______ (填“ ”或“
”或“ ”)
”) ,原因是
,原因是____________ 。
(3)尿素的结构和丙酮( )相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是
)相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是____________ 。
 作为一种中性肥料,适用于各种土壤和植物。
作为一种中性肥料,适用于各种土壤和植物。(1)十九世纪初,用氰酸银
 与
与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。
,实现了由无机物到有机物的合成。①
 位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为
位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为②
 与
与 中的C原子杂化方式分别为
中的C原子杂化方式分别为(2)二十世纪初,工业上以
 和
和 为原料在一定温度和压强下合成
为原料在一定温度和压强下合成 :
: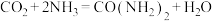 。
。①上述物质中,属于非极性分子的是
②键角比较:

 ”或“
”或“ ”)
”) ,原因是
,原因是(3)尿素的结构和丙酮(
 )相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是
)相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是
您最近一年使用:0次
解题方法
7 . 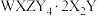 可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
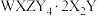 可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是A.第一电离能: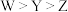 |
B.最简单氢化物的熔、沸点: |
| C.上述化合物的固体为分子晶体 |
| D.Z的最高价氧化物的水化物的阴离子空间结构为正四面体形 |
您最近一年使用:0次
8 . 现有几组物质的熔点(℃)数据:
(1)A组中硅晶体的熔点低于金刚石,原因是_______ 。
(2)C组中HF相对分子质量小于 但熔点却高于
但熔点却高于 ,是由于
,是由于_______ 。
(3)D组晶体中 、
、 、
、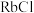 、
、 的熔点由高到低的顺序为
的熔点由高到低的顺序为_______ 。
(4) 晶体的晶胞如图所示,与NaCl的晶胞结构相似。若将
晶体的晶胞如图所示,与NaCl的晶胞结构相似。若将 由顶点转换成体心,则
由顶点转换成体心,则 的位置转换为
的位置转换为_______ 。 晶体在
晶体在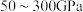 的高压下和
的高压下和 反应生成如图所示的晶胞结构,则该晶体的化学式为
反应生成如图所示的晶胞结构,则该晶体的化学式为_______ 。 的晶胞如图所示,密度为
的晶胞如图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为anm,则
的最近核间距为anm,则 的摩尔质量为
的摩尔质量为_______ 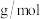 (列出代数式,设
(列出代数式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF: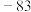 |  |
| 硅晶体:1410 | Na:98 |  : :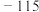 |  |
| 硼晶体:2300 | K:64 |  : :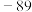 | 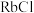 |
| 二氧化硅:1732 | Rb:39 | HI: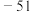 |  |
(1)A组中硅晶体的熔点低于金刚石,原因是
(2)C组中HF相对分子质量小于
 但熔点却高于
但熔点却高于 ,是由于
,是由于(3)D组晶体中
 、
、 、
、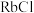 、
、 的熔点由高到低的顺序为
的熔点由高到低的顺序为(4)
 晶体的晶胞如图所示,与NaCl的晶胞结构相似。若将
晶体的晶胞如图所示,与NaCl的晶胞结构相似。若将 由顶点转换成体心,则
由顶点转换成体心,则 的位置转换为
的位置转换为
 晶体在
晶体在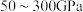 的高压下和
的高压下和 反应生成如图所示的晶胞结构,则该晶体的化学式为
反应生成如图所示的晶胞结构,则该晶体的化学式为
 的晶胞如图所示,密度为
的晶胞如图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为anm,则
的最近核间距为anm,则 的摩尔质量为
的摩尔质量为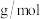 (列出代数式,设
(列出代数式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
9 . 下列现象与氢键有关的有几个
① 的沸点比
的沸点比 的高;
的高;
②乙醇能与水以任意比混溶,而甲醚(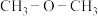 )难溶于水;
)难溶于水;
③邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低;
④水分子在高温下很稳定;
⑤冰的密度比液态水的密度小:
⑥ 易液化;
易液化;
⑦ 分子比
分子比 分子稳定;
分子稳定;
⑧在相同条件下, 的沸点比
的沸点比 的沸点高
的沸点高
①
 的沸点比
的沸点比 的高;
的高;②乙醇能与水以任意比混溶,而甲醚(
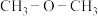 )难溶于水;
)难溶于水;③邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低;
④水分子在高温下很稳定;
⑤冰的密度比液态水的密度小:
⑥
 易液化;
易液化;⑦
 分子比
分子比 分子稳定;
分子稳定;⑧在相同条件下,
 的沸点比
的沸点比 的沸点高
的沸点高| A.6 | B.5 | C.4 | D.3 |
您最近一年使用:0次
10 . 下列与分子性质有关的说法正确的是
| A.氟代丙二酸(HOOC—CF2—COOH)酸性强于丙二酸(HOOC—CH2—COOH)是因为F原子吸引电子能力大于H原子,导致氟代丙二酸羧基中-OH的极性更大更易电离出H+ |
B.邻硝基苯酚(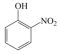 )的沸点高于对硝基苯酚( )的沸点高于对硝基苯酚(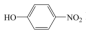 )是因为后者形成了分子间氢键 )是因为后者形成了分子间氢键 |
| C.C的电负性强于Si,所以CH4的熔沸点高于SiH4 |
| D.I2受热易升华,是因为分子内共价键键能较小所致 |
您最近一年使用:0次

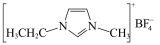 低于
低于


