解题方法
1 . 固态NH3晶体中含有的作用力有
| A.非极性键 | B.极性键 | C.配位键 | D.氢键 |
您最近一年使用:0次
名校
2 . 磷酸三甲酯常用作阻燃剂,可采用下列流程合成少量该物质:___________ 。反应⑤为加热条件下的分解反应,反应中还产生了三角锥形结构的气体,该气体的化学式为___________ 。
(2)关于上述流程图,下列说法正确的是___________。
(3)写出由反应⑥生成磷酸三甲酯的化学方程式___________ 。
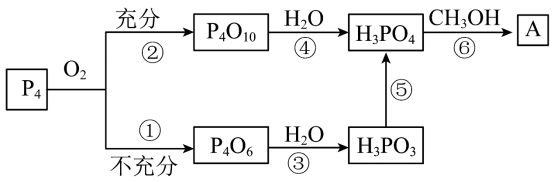
已知:磷酸和亚磷酸的结构: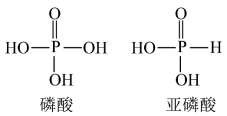
(2)关于上述流程图,下列说法正确的是___________。
| A.①~⑥反应过程中涉及到磷元素的三种不同价态 |
| B.CH3OH与H3PO4的投料比不同,A可能有不同的结构 |
| C.H3PO4溶液黏度较大,是由于溶液中存在氢键 |
| D.P4分子构型为正四面体形结构,键角为109°28′ |
您最近一年使用:0次
名校
解题方法
3 . 硼酸(H3BO3)晶体结构为层状,其二维平面结构如图:______ mol氢键。
(2)硼酸是一元弱酸,它本身不给出H+,但与水作用后能给出H+。用离子方程式说明硼酸水溶液呈酸性的原因为_______ 。

(2)硼酸是一元弱酸,它本身不给出H+,但与水作用后能给出H+。用离子方程式说明硼酸水溶液呈酸性的原因为
您最近一年使用:0次
名校
解题方法
4 . 硒(Se)是第34号元素,含硒化合物在材料、药物领域具有广泛应用。
(1)基态Se原子的价电子排布式为_______ 。
(2)H2Se是一种有恶臭的气体,与H2O相比
①沸点:H2Se______ H2O。
②热稳定性:H2Se______ H2O。
A.> B.< C.无法确定
(1)基态Se原子的价电子排布式为
(2)H2Se是一种有恶臭的气体,与H2O相比
①沸点:H2Se
②热稳定性:H2Se
A.> B.< C.无法确定
您最近一年使用:0次
名校
解题方法
5 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。
(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
(2)第三周期元素的原子中,未成对电子不可能有_______。
(3)基态F原子的轨道表示式为_______ ,四氟乙烯的电子式为_______ 。
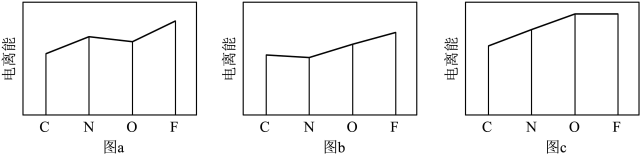
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填字母),第三电离能的变化图是_______ (填字母)。
(5) 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(6)比较甲醚和乙醇的沸点高低,并说明理由_______ 。
 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
| A.原子与原子之间 | B.分子与分子之间 | C.离子与离子之间 | D.离子与电子之间 |
(2)第三周期元素的原子中,未成对电子不可能有_______。
| A.4个 | B.3个 | C.2个 | D.1个 |
(3)基态F原子的轨道表示式为
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)
 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为(6)比较甲醚和乙醇的沸点高低,并说明理由
您最近一年使用:0次
名校
6 . 科学家正在研究温室气体 和
和 的转化和利用。在
的转化和利用。在 基催化剂作用下,
基催化剂作用下, 和
和 反应可获得合成气
反应可获得合成气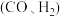 。
。
(1)基态 原子的电子排布式可简要表示为
原子的电子排布式可简要表示为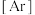
_____ 。
(2) 能与
能与 形成正四面体形的配位分子
形成正四面体形的配位分子 ,该分子属于
,该分子属于_____ 。
A.极性分子 B.非极性分子, 中含有
中含有_____  键。
键。
(3)已知 的燃烧热为
的燃烧热为 的燃烧热为
的燃烧热为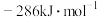 。用
。用 和
和 反应所得的合成气的热值(单位:
反应所得的合成气的热值(单位: )为多少?
)为多少?_____ (写出计算过程,体积按标准状况计算, )。
)。
一定条件下, 和
和 都能与
都能与 形成笼状结构的水合物晶体(如图),相关参数如表所示。
形成笼状结构的水合物晶体(如图),相关参数如表所示。

已知可燃冰形成过程可以表示为: 。
。
(4)“可燃冰”中分子间存在的作用有_____ 。
(5)目前已探明的可燃冰都分布在深海海底或永久冻土层深处,结合平衡原理解释这一现象_____ 。
(6)为开采深海海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知上图中笼状结构的空腔直径为
的设想。已知上图中笼状结构的空腔直径为 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是_____ 。
 的晶胞呈立方体结构(如图),图中每一个小球代表一个
的晶胞呈立方体结构(如图),图中每一个小球代表一个 分子。
分子。

(7)甲烷晶体中,离一个甲烷分子最近的甲烷分子有_____。
(8)已知甲烷晶体密度为 ,晶胞的棱长为
,晶胞的棱长为 。则阿伏加德罗常数可以用含
。则阿伏加德罗常数可以用含 、a的代数式表示为
、a的代数式表示为
_____  。
。
 和
和 的转化和利用。在
的转化和利用。在 基催化剂作用下,
基催化剂作用下, 和
和 反应可获得合成气
反应可获得合成气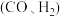 。
。(1)基态
 原子的电子排布式可简要表示为
原子的电子排布式可简要表示为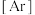
(2)
 能与
能与 形成正四面体形的配位分子
形成正四面体形的配位分子 ,该分子属于
,该分子属于A.极性分子 B.非极性分子,
 中含有
中含有 键。
键。(3)已知
 的燃烧热为
的燃烧热为 的燃烧热为
的燃烧热为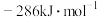 。用
。用 和
和 反应所得的合成气的热值(单位:
反应所得的合成气的热值(单位: )为多少?
)为多少? )。
)。一定条件下,
 和
和 都能与
都能与 形成笼状结构的水合物晶体(如图),相关参数如表所示。
形成笼状结构的水合物晶体(如图),相关参数如表所示。
分子直径/ | 分子与 的结合能 的结合能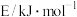 | |
 | 0.436 | 16.40 |
 | 0.512 | 29.91 |
 。
。(4)“可燃冰”中分子间存在的作用有
(5)目前已探明的可燃冰都分布在深海海底或永久冻土层深处,结合平衡原理解释这一现象
(6)为开采深海海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知上图中笼状结构的空腔直径为
的设想。已知上图中笼状结构的空腔直径为 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是 的晶胞呈立方体结构(如图),图中每一个小球代表一个
的晶胞呈立方体结构(如图),图中每一个小球代表一个 分子。
分子。
(7)甲烷晶体中,离一个甲烷分子最近的甲烷分子有_____。
| A.4个 | B.6个 | C.8个 | D.12个 |
(8)已知甲烷晶体密度为
 ,晶胞的棱长为
,晶胞的棱长为 。则阿伏加德罗常数可以用含
。则阿伏加德罗常数可以用含 、a的代数式表示为
、a的代数式表示为
 。
。
您最近一年使用:0次
名校
解题方法
7 . 甲胺是重要的化工原料,被广泛应用于国民经济各个领域,是农药、医药、橡胶等领域内的重要的基本化工原料。
(1)甲胺(CH3NH2)是一种弱碱,可与盐酸反应生成盐酸盐(用CH3NH3Cl表示)。下列叙述正确的是___________。
(2)与甲胺类似,氨基酸也能与酸反应,请结合官能团性质解释甘氨酸(H2NCH2COOH)的熔点高于分子量相近的丙酸(CH3CH2COOH)和丁胺(CH3CH2CH2NH2)的原因:___________ 。
(1)甲胺(CH3NH2)是一种弱碱,可与盐酸反应生成盐酸盐(用CH3NH3Cl表示)。下列叙述正确的是___________。
A.CH3NH3Cl在水中的电离方程式为:CH3NH3Cl CH3NH CH3NH +Cl- +Cl- |
| B.0.01 mol/L CH3NH2水溶液的 pH=12 |
| C.0.1 mol/L CH3NH2水溶液加水稀释,pH降低 |
D.CH3NH3Cl水溶液中:c(Cl-)>c(H+)>c(CH3NH )>c(OH-) )>c(OH-) |
您最近一年使用:0次
名校
8 . 我国长征系列运载火箭采用偏二甲肼(C2H8N2)和 作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是
作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是
 作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是
作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是A.基态N的价电子排布图为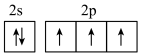 |
| B.N、O的电负性较大,其单质通常比较活泼 |
| C.偏二甲肼分子间存在氢键,沸点较高 |
| D.二氧化碳为非极性分子,水分子和偏二甲肼为极性分子 |
您最近一年使用:0次
2024-01-07更新
|
252次组卷
|
3卷引用:上海市宜川中学2023-2024学年高三上学期10月月考化学试卷
9 . 关于H2O2分子和H2O分子的下列描述合理的是
| A.分子中均只含极性键 | B.O原子的杂化类型不同 |
| C.分子均是极性分子 | D.沸点是由范德华力决定的 |
您最近一年使用:0次
10 . 键能是衡量共价键稳定性的参数之一,CH3OH有_______ 种键能数据,CH3OH可以与水以任意比例互溶的原因可能是_______ 。
您最近一年使用:0次



