名校
解题方法
1 . 下列晶体熔点性质比较,错误的是
A. | B.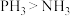 | C.金刚石>晶体硅 | D.氧化镁>氯化钠 |
您最近一年使用:0次
名校
解题方法
2 . 化学与生产生活密切相关,下列说法错误的是
| A.二氧化硅是制造水泥、玻璃和光导纤维的原料 |
| B.离子液体有良好的导电性,可用作电化学研究的电解质 |
| C.天然气水合物是一种潜在的能源,可燃冰是甲烷水合物,甲烷和水之间存在氢键 |
D.以 为基础,用 为基础,用 取代部分 取代部分 ,用 ,用 取代部分 取代部分 获得的陶瓷,可用于制作LED发光材料 获得的陶瓷,可用于制作LED发光材料 |
您最近一年使用:0次
名校
解题方法
3 . 硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是___________ 。
(2)硫单质的一种结构为 ,S原子的杂化方式为
,S原子的杂化方式为___________ 。
(3)① 、②
、② 、③
、③ 键角由大到小的顺序是
键角由大到小的顺序是___________ 。(用序号回答即可)
(4)熔点:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(5)分析并比较A: 与B:
与B: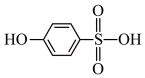 的沸点高低:
的沸点高低:___________ (用A、B表示),原因是___________ 。
(6)ZnS晶胞如图所示: 填在了
填在了 形成的
形成的___________ 空隙中。
②已知晶胞密度为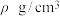 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为___________ cm。
(1)基态硫原子的价层电子排布图是
(2)硫单质的一种结构为
 ,S原子的杂化方式为
,S原子的杂化方式为(3)①
 、②
、② 、③
、③ 键角由大到小的顺序是
键角由大到小的顺序是(4)熔点:

 (填“>”或“<”)。
(填“>”或“<”)。(5)分析并比较A:
 与B:
与B: 的沸点高低:
的沸点高低:(6)ZnS晶胞如图所示:

 填在了
填在了 形成的
形成的②已知晶胞密度为
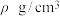 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
| A.HF、HCl、HBr、HI的熔沸点、还原性都依次升高(增强) |
| B.通常测定氟化氢的相对分子质量大于理论值,因分子间存在氢键 |
C. 、 、 、 、 分子中所有原子都满足最外层为8电子结构的是 分子中所有原子都满足最外层为8电子结构的是 、 、 |
| D.乙醇比甲醇更易溶于水 |
您最近一年使用:0次
名校
解题方法
5 . 下列有关氢键的说法正确的是
| A.HF溶液中存在三种类型的氢键 | B.  的沸点比 的沸点比 的低 的低 |
| C.H2O的稳定性高,是因为水分子间存在氢键 | D.1mol冰中含有2mol氢键 |
您最近一年使用:0次
6 . 已知几种共价键的键能如下:
下列说法错误的是
| 化学键 | H—N | N≡N | Cl—Cl | H—Cl |
键能/ | 391 | 946 | 243 | 431 |
| A.键能:N≡N>N=N>N—N |
B.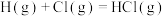 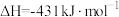 |
C.H—N键能小于H—Cl键能,所以 的沸点高于HCl 的沸点高于HCl |
D.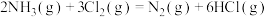 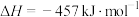 |
您最近一年使用:0次
名校
7 . 硫氰化钾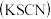 不仅用作化学检测试剂,还可用于农药、医药、电镀等。
不仅用作化学检测试剂,还可用于农药、医药、电镀等。 可通过以下反应得到:
可通过以下反应得到: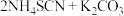

 。回答下列问题:
。回答下列问题:
(2)写出
 的结构式
的结构式(3)
 存在的化学键类型是
存在的化学键类型是 填字母,下同
填字母,下同 。
。 只含有离子键
只含有离子键  只含有共价键
只含有共价键  既含有离子键又含有共价键
既含有离子键又含有共价键(4)上述反应涉及的多种元素或者物质中:
 实验室制备
实验室制备 的化学方程式
的化学方程式 属于第二周期且非金属性由弱到强的顺序为
属于第二周期且非金属性由弱到强的顺序为 比其同主族其它元素的氢化物沸点高的原因为
比其同主族其它元素的氢化物沸点高的原因为(5)下列事实能说明非金属性
 强于
强于 的是
的是 常温下
常温下 化学性质稳定
化学性质稳定 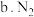 的沸点低于红磷的沸点
的沸点低于红磷的沸点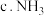 受热分解的温度高于
受热分解的温度高于
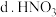 的酸性强于
的酸性强于
您最近一年使用:0次
8 . 氮、氧、磷、砷及其化合物在工农业生产等方面有着重要应用。请按要求回答下列问题。
(1)电负性P_______ As(填“>”或“<”或“=”)。
(2)尿素(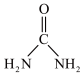 )中碳原子杂化类型
)中碳原子杂化类型_______ ; 离子的立体构型名称(即空间构型)为
离子的立体构型名称(即空间构型)为_______ 。
(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是_______ 。
(4)我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。已知砷化镓的熔点为1238℃,GaAs的晶胞结构如图所示。_______ ,As与Ga之间存在的化学键有_______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
②1号镓原子的坐标为_______ 。晶胞密度为dg∙cm-3,摩尔质量为Mg∙mol-1 ,阿伏加德罗常数的值用NA表示,则晶胞中最近的As和Ga原子核间距为_______ nm(列式表示)。
(1)电负性P
(2)尿素(
 )中碳原子杂化类型
)中碳原子杂化类型 离子的立体构型名称(即空间构型)为
离子的立体构型名称(即空间构型)为(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是
(4)我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。已知砷化镓的熔点为1238℃,GaAs的晶胞结构如图所示。
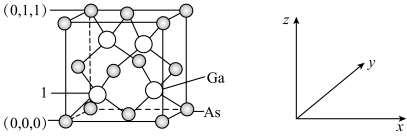
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
②1号镓原子的坐标为
您最近一年使用:0次
名校
9 . 下列对有关事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 氟化氢的沸点比溴化氢的沸点高 | 氟化氢分子间形成氢键 |
| B | 在CS2中的溶解度:CCl4>H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
| C | 用质谱仪检测乙酸时,谱图出现了质荷比为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
| D | 稳定性:[Cu(H2O)4]2+<[Cu(NH3)4]2+ | N的电负性小于O的电负性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下列各组物质性质的比较,结论正确的是
| A.热稳定性:HF>H2O>NH3 | B.溶液酸性:CF3COOH < CCl3COOH |
| C.分子的极性:BCl3 > NCl3 | D.在水中的溶解度:CH3CH2Br > CH3CH2OH |
您最近一年使用:0次



