1 . Wolff-Kishner-黄鸣龙还原反应机理如下( 均代表烃基),下列有关说法不正确的是
均代表烃基),下列有关说法不正确的是
 均代表烃基),下列有关说法不正确的是
均代表烃基),下列有关说法不正确的是
| A.肼的沸点高于氨气,原因是分子间氢键数目更多,且相对分子质量更大 |
| B.过程①发生加成反应,过程②发生消去反应 |
C.增大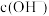 ,可以使过程③反应速率增大,促进平衡正向移动 ,可以使过程③反应速率增大,促进平衡正向移动 |
D.应用该机理, 可以在碱性条件下转变为 可以在碱性条件下转变为 |
您最近一年使用:0次
2 . 研究发现有一种高效的消毒漂白剂TCCA(如图所示)。W、X、Y、Z是分属两个不同短周期且原子序数递增的主族元素,Y原子核外最外层电子数是内层电子数的3倍。下列叙述正确的是

| A.X、Y与氢元素共同组成的化合物只含共价键 |
| B.氧化物的水化物酸性:Z>X>W |
| C.氢化物的沸点满足:Y>W |
| D.分子中所有原子均满足8电子稳定结构 |
您最近一年使用:0次
解题方法
3 . 近年来,光催化剂的研究是材料领域的热点方向。如图一种 配合物复合光催化剂,可将
配合物复合光催化剂,可将 转化为
转化为 。下列说法错误的是
。下列说法错误的是

 配合物复合光催化剂,可将
配合物复合光催化剂,可将 转化为
转化为 。下列说法错误的是
。下列说法错误的是
A.该配合物中 的配位数是6,中心离子为 的配位数是6,中心离子为 |
B. 配合物中第二周期元素的电负性由大到小的顺序为 配合物中第二周期元素的电负性由大到小的顺序为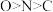 |
C.已知吡啶(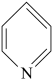 )中所有原子共平面,则吡啶中存在 )中所有原子共平面,则吡啶中存在 大π键 大π键 |
D. 的沸点比 的沸点比 高,主要原因是 高,主要原因是 分子间存在范德华力和氢键,而 分子间存在范德华力和氢键,而 分子间只有范德华力 分子间只有范德华力 |
您最近一年使用:0次
4 . 一种高分子材料G在生产、生活中用途广泛,其结构如图所示。合成G的两种单体为甲、乙,且甲的相对分子质量大于乙。下列叙述正确的是

| A.G只有1种官能团 | B.甲的沸点高于乙 |
| C.乙熔化时断裂共价键 | D.乙连续氧化不能生成甲 |
您最近一年使用:0次
5 . 水是最常见的物质之一,也是生命的源泉。请回答:
(1)氧原子的价层电子轨道表示式为___________ 。 的VSEPR空间结构名称是
的VSEPR空间结构名称是___________ 。
(2)水是最重要的溶剂,对溶液的性质有重要影响。
①下列说法正确的是___________ 。
A.水电离生成 和
和 ,
, 的键角比
的键角比 中的小
中的小
B. 溶于水形成
溶于水形成 ,
, 中O的杂化方式不变
中O的杂化方式不变
C.氨基酸一般都能溶于水和乙醇,主要是因为与水分子间能形成氢键
D.乙胺 和乙酰胺
和乙酰胺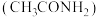 溶于水可显碱性,且乙胺碱性更强
溶于水可显碱性,且乙胺碱性更强
②丙酮可发生自身羟醛缩合,研究表明该反应机理为,碱性条件下丙酮失去1个 形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性
形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性 的理由
的理由___________ 。
(3)晶莹剔透的雪花呈六角形,与其微观结构有关。如下左图为冰晶体的晶胞结构图(底面为含 角的菱形,底面边长a pm,高c pm),右图为晶体结构图(为保证结构清晰,两图均只画出氧原子)。每个氧原子的配位数(周围的氢原子数)为
角的菱形,底面边长a pm,高c pm),右图为晶体结构图(为保证结构清晰,两图均只画出氧原子)。每个氧原子的配位数(周围的氢原子数)为___________ 。距离最近的两个氧原子间距离为___________ pm(用含a或c的代数式表示)。冰晶体中氧原子相连可形成六元环状结构,冰晶体中的六元环构型为___________ 。(填“椅式”、“船式”或“椅式和船式”)

(1)氧原子的价层电子轨道表示式为
 的VSEPR空间结构名称是
的VSEPR空间结构名称是(2)水是最重要的溶剂,对溶液的性质有重要影响。
①下列说法正确的是
A.水电离生成
 和
和 ,
, 的键角比
的键角比 中的小
中的小B.
 溶于水形成
溶于水形成 ,
, 中O的杂化方式不变
中O的杂化方式不变C.氨基酸一般都能溶于水和乙醇,主要是因为与水分子间能形成氢键
D.乙胺
 和乙酰胺
和乙酰胺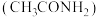 溶于水可显碱性,且乙胺碱性更强
溶于水可显碱性,且乙胺碱性更强②丙酮可发生自身羟醛缩合,研究表明该反应机理为,碱性条件下丙酮失去1个
 形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性
形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性 的理由
的理由(3)晶莹剔透的雪花呈六角形,与其微观结构有关。如下左图为冰晶体的晶胞结构图(底面为含
 角的菱形,底面边长a pm,高c pm),右图为晶体结构图(为保证结构清晰,两图均只画出氧原子)。每个氧原子的配位数(周围的氢原子数)为
角的菱形,底面边长a pm,高c pm),右图为晶体结构图(为保证结构清晰,两图均只画出氧原子)。每个氧原子的配位数(周围的氢原子数)为
您最近一年使用:0次
解题方法
6 . W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,且四种元素的原子质子数之和为48。下列说法错误的是
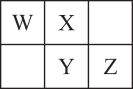

A.相同浓度最高价含氧酸溶液的 : : |
B.元素的最高化合价: |
C.简单氢化物的沸点: |
D.单核离子的半径: |
您最近一年使用:0次
名校
解题方法
7 . 元素周期表是许多科学家共同努力的结晶。下图是元素周期表的一部分。
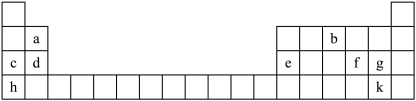
请回答下列问题:
(1)a元素的名称是_______ ,在实验室中c的单质通常保存在_______ 中。
(2)f、g、k三种元素的非金属性由强到弱的顺序是_______ (用元素符号表示)。
(3)e的最高价氧化物与h的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4)b的简单氢化物沸点高于同主族相邻周期元素的简单氢化物,其原因是_______ 。

请回答下列问题:
(1)a元素的名称是
(2)f、g、k三种元素的非金属性由强到弱的顺序是
(3)e的最高价氧化物与h的最高价氧化物对应的水化物反应的离子方程式为
(4)b的简单氢化物沸点高于同主族相邻周期元素的简单氢化物,其原因是
您最近一年使用:0次
2022-10-10更新
|
462次组卷
|
2卷引用:皖豫名校联盟2022-2023学年高三毕业班第一次联考化学试题
解题方法
8 . 氟是特种塑料、橡胶和冷冻剂(氟氯烷)中的关键元素。回答下列问题:
(1)基态F原子核外电子的空间运动状态有_______ 种。
(2)同周期元素N、O、F的第一电离能由大到小的顺序为_______ ,N、O、F 常见的氢化物NH3、H2O、HF的稳定性由强到弱的顺序为_______ 。
(3)氟气与水的反应复杂,主要生成HF和O2,副反应生成少量的H2O2、OF2等。OF2分子的空间构型为_______ ;HF与水能以任意比例互溶,原因是_______ 。 在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合(HF)2形式存在,使HF分子缔合的作用力是_______
(4)同主族元素Cl、Br、I的单质均可与水反应生成次卤酸,则ClO-中氯原子的杂化方式为_______ 。
(5)XeF2晶体属四方晶系,晶胞结构如图所示,晶胞棱边夹角均为90.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。图中原子A的分数坐标为(0,0,0) ,原子B的分数坐标为( ,
, ,
, )。已知Xe- F键长为r pm,则原子C的分数坐标为
)。已知Xe- F键长为r pm,则原子C的分数坐标为_______ ;设NA为阿伏加德罗常数的值,XeF2的密度为_______ (列计算式)g·cm-3。

(1)基态F原子核外电子的空间运动状态有
(2)同周期元素N、O、F的第一电离能由大到小的顺序为
(3)氟气与水的反应复杂,主要生成HF和O2,副反应生成少量的H2O2、OF2等。OF2分子的空间构型为
(4)同主族元素Cl、Br、I的单质均可与水反应生成次卤酸,则ClO-中氯原子的杂化方式为
(5)XeF2晶体属四方晶系,晶胞结构如图所示,晶胞棱边夹角均为90.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。图中原子A的分数坐标为(0,0,0) ,原子B的分数坐标为(
 ,
, ,
, )。已知Xe- F键长为r pm,则原子C的分数坐标为
)。已知Xe- F键长为r pm,则原子C的分数坐标为
您最近一年使用:0次
9-10高二下·河北·阶段练习
名校
解题方法
9 . 图为冰晶体的结构模型,大球代表O,小球代表H。下列有关说法正确的是

| A.冰晶体中每个水分子与另外四个水分子形成四面体结构 |
| B.冰晶体具有空间网状结构,是共价晶体 |
C.水分子间通过 键形成冰晶体 键形成冰晶体 |
| D.冰融化后,水分子之间的空隙增大 |
您最近一年使用:0次
2022-08-29更新
|
998次组卷
|
25卷引用:09—10学年衡中高二下学期第二次调研考试化学试卷
(已下线)09—10学年衡中高二下学期第二次调研考试化学试卷2015-2016学年山东省淄博市高青一中高二4月月考化学试卷云南省玉溪市新平三中2019-2020学年高二上学期12月份月考化学试题课时2 分子晶体——A学习区 夯实基础(鲁科版选修3)(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体 第1课时 分子晶体(鲁科版2019)选择性必修2 第3章 不同聚集状态的物质与性质 第2节 几种简单的晶体结构模型(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体鲁科版2019选择性必修2第3章 不同聚集状态的物质与性质 第2节 几种简单的晶体结构模型 第4课时 分子晶体晶体结构的复杂性(已下线)3.2.2 共价晶体与分子晶体及晶体结构的复杂性-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题05 物质结构和元素周期律-备战2022年高考化学学霸纠错(全国通用)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第43练 分子晶体与共价晶体-2023年高考化学一轮复习小题多维练(全国通用)专题3 微粒间作用力与物质性质 第四单元 分子间作用力分子晶体 第2课时 分子晶体第二节 分子晶体与共价晶体 第1课时 分子晶体(已下线)3.2.1 分子晶体-同步学习必备知识第三章 晶体结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)浙江省丽水市2022-2023学年高二下学期普通高中期末教学质量检测化学试题3.4.2分子晶体 课后3.2.1 分子晶体-课堂例题(已下线)2010年云南省玉溪一中高二下学期期末考试化学试题甘肃省静宁县第一中学2020-2021学年高二上学期期末考试化学(实验班)试题(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)福建省泉州市泉港区第五中学等校2021-2022学年高二下学期期末联考化学试题福建省泉州市泉港区第五中学等校2021-2022学年高二下学期期末联考化学试题
10 . W、X、Y、Z、M为原子序数依次增大的短周期主族元素,W为宇宙中含量最多的元素,X的内层电子数为最外层的一半,Z与M最外层电子数相同,且M的原子序数等于Y与Z的原子序数之和。下列说法正确的是
| A.原子半径:X>Y>Z>M |
| B.W与Y能形成含有非极性键的化合物 |
| C.Z和M的最简单氢化物的沸点:Z<M |
| D.氧化物对应的水化物的酸性:X<M |
您最近一年使用:0次



