名校
解题方法
1 . 我国某科研团队制得一种超分子功能材料,反应如下:
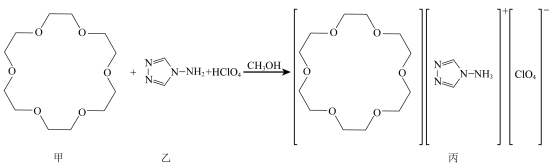
A. 分子中3个非羟基氧吸电子,使 分子中3个非羟基氧吸电子,使 键极性增大,易电离出 键极性增大,易电离出 |
| B.乙质子化后形成的阳离子嵌入甲的环内,通过氢键结合形成超分子 |
| C.丙含有的H、C、N、O和Cl五种元素中,O的电负性和第一电离能均最大 |
| D.若将乙更换为其类似物,则可根据其阳离子大小选择空腔适合的甲的类似物 |
您最近一年使用:0次
2 . X、Y、Z为原子序数依次增大的三种短周期主族元素。元素X基态原子的电子只有1种自旋取向,Y的最外层电子数是其内层的3倍,元素Z基态原子的3p轨道上有4个电子,W位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.下列说法正确的是
| A.简单氢化物的沸点:Y<Z | B.简单离子半径大小:W>Y>Z>X |
| C.电负性大小:Y>Z>X>W | D. 的空间构型为平面三角形 的空间构型为平面三角形 |
您最近一年使用:0次
3 . 德国科学家发现新配方:他使用了远古地球上存在的 、
、 、
、 、
、 、
、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
 、
、 、
、 、
、 、
、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是A.基态 价电子排布为 价电子排布为 | B. 、 、 、 、 分子间均存在氢键 分子间均存在氢键 |
C. 、 、 、HCN中均存在σ键和π键 、HCN中均存在σ键和π键 | D.沸点: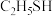 (乙硫醇) (乙硫醇) |
您最近一年使用:0次
2024-05-03更新
|
114次组卷
|
2卷引用:云南省曲靖市第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
4 . 下列说法正确的是
| A.I2的升华破坏了共价键 |
| B.氢键是一种特殊的共价键 |
| C.Na2O2中的阴阳离子个数比为1:2 |
| D.卤素单质的熔点从F2到I2逐渐升高,则碱金属单质的熔点从Li到Cs也逐渐升高 |
您最近一年使用:0次
名校
5 . 黑火药的主要成分为木炭(C)、硫黄(S)和火硝(KNO3).请回答下列问题。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为___________ 形。
(2)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为___________ 。
(3)C、N、O、K四种元素的第一电离能由大到小的顺序为___________ 。
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为___________ ;
②H2Se的中心原子杂化类型是:___________ , SeO32-的立体构型是___________ ;
③比较H2S与H2O沸点高低,并说明原因:___________ 。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为
(2)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为(3)C、N、O、K四种元素的第一电离能由大到小的顺序为
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为
②H2Se的中心原子杂化类型是:
③比较H2S与H2O沸点高低,并说明原因:
您最近一年使用:0次
名校
6 . 下列解释不正确的是
| 选项 | 物质的结构或性质或者实验目的 | 解释 |
| A | 键角: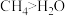 | CH4中C原子与H2O中O原子杂化不同 |
| B | CH4、SiH4、GeH4熔点逐渐升高 | 相对分子质量逐渐增大 |
| C | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
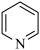
| D | 水中溶解性;苯<吡啶( | 吡啶能与水形成分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . N、P、As为第VA族元素,该族元素及其化合物在生产、生活中有广泛应用。回答下列问题:
(1)基态As原子核外有______ 个未成对电子,N、P、As电负性由大到小的顺序为______ 。
(2)已知:4AsH3 As4+6H2↑,AsH3的空间结构为
As4+6H2↑,AsH3的空间结构为______ ,已知As4为正四面体结构,则1molAs4中含______ molσ键。
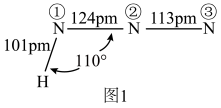
(3)氨、肼(N2H4)和叠氮酸(HN3)都是氮元素的重要氢化物,肼的相对分子质量与乙烷(C2H6)接近,但沸点远高于乙烷的原因是______ 。叠氮酸的结构如图1所示,分子中②号N原子的杂化方式为_______ 。_______ ,该晶体的密度为______ g cm3。
cm3。
(1)基态As原子核外有
(2)已知:4AsH3
 As4+6H2↑,AsH3的空间结构为
As4+6H2↑,AsH3的空间结构为(3)氨、肼(N2H4)和叠氮酸(HN3)都是氮元素的重要氢化物,肼的相对分子质量与乙烷(C2H6)接近,但沸点远高于乙烷的原因是
 cm3。
cm3。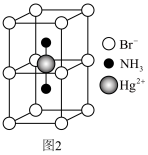
您最近一年使用:0次
2024-03-20更新
|
166次组卷
|
2卷引用:云南省文山州广南县第十中学校2023-2024学年高二下学期3月考试化学试题
8 . 下列有关说法正确的是
A.元素的电负性: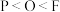 |
B.因为二氧化硅的相对分子质量比二氧化碳大,所以沸点: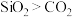 |
C. 、 、 、 、 三种离子晶体的熔点: 三种离子晶体的熔点: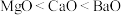 |
D.稳定性: ,是因为水分子间存在氢键的缘故 ,是因为水分子间存在氢键的缘故 |
您最近一年使用:0次
名校
9 . ⅣA、ⅤA、ⅥA、ⅦA四个主族元素的氢化物的沸点变化趋势如下图所示,分析图中的递变规律,下列结论中正确的是

| A.CH4分子间的氢键较弱,故其沸点较低 |
| B.图中的横坐标的数值表示的是中心原子的主族序数 |
| C.第ⅣA族元素氢化物的稳定性随相对分子质量的递增逐渐增强 |
| D.H2O、HF、NH3三种物质的沸点比同主族的其他氢化物高 |
您最近一年使用:0次
2024-03-03更新
|
280次组卷
|
3卷引用:云南省文山州广南县第十中学校2023-2024学年高二下学期3月考试化学试题
解题方法
10 . 现有短周期主族元素X、Y、Z、R、T,R原子最外层电子数是电子层数的2倍;Y与Z能形成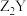 、
、 型离子化合物,Y与T同主族,五种元素的原子半径与原子序数的关系如图,下列说法正确的是
型离子化合物,Y与T同主族,五种元素的原子半径与原子序数的关系如图,下列说法正确的是
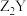 、
、 型离子化合物,Y与T同主族,五种元素的原子半径与原子序数的关系如图,下列说法正确的是
型离子化合物,Y与T同主族,五种元素的原子半径与原子序数的关系如图,下列说法正确的是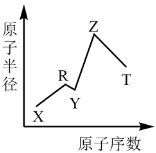
| A.原子半径和离子半径均满足:Y<Z |
| B.简单的气态氢化物的沸点和稳定性排序均为:Y>T |
| C.最高价氧化物对应的水化物的酸性:T<R |
| D.由X、R、Y三种元素组成的化合物水溶液一定显酸性 |
您最近一年使用:0次

 )
)

