名校
解题方法
1 .  及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:
(1)基态铁原子的核外电子排布式为:______ , 比
比 更稳定的原因是:
更稳定的原因是:______ 。
(2) 中铁元素的配位数是
中铁元素的配位数是______ ,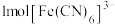 中含有的
中含有的 键的数目为
键的数目为______ , 中C原子的杂化方式为
中C原子的杂化方式为______ 。
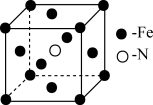
(3)铁和氨在 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:______ 。
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)______ 。

 及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:(1)基态铁原子的核外电子排布式为:
 比
比 更稳定的原因是:
更稳定的原因是:(2)
 中铁元素的配位数是
中铁元素的配位数是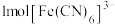 中含有的
中含有的 键的数目为
键的数目为 中C原子的杂化方式为
中C原子的杂化方式为(3)铁和氨在
 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出
 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)
您最近一年使用:0次
2 . 某工业废渣的主要成分为NiO、CuO、 、ZnO,一种综合回收利用的工艺流程如图所示:
、ZnO,一种综合回收利用的工艺流程如图所示:

回答下列问题:
(1)写出浸渣主要成分的一种用途:_______ 。
(2)浸取液含有的配离子有 、
、 、
、 ,
, 的中心离子为
的中心离子为_______ ,配位数为_______ ; 能作配体的原因是
能作配体的原因是_______ 。
(3)“还原”得到Cu时发生反应的氧化剂和还原剂的物质的量之比为_______ ;该反应温度不宜过高,原因是_______ 。
(4)“沉锌镍”后得到的滤液中可循环利用的物质有_______ (填化学式)。
(5)“脱锌”时反应的化学方程式为_______ 。
(6)NiO为绿色固体,常用作搪瓷的着色剂,其晶胞结构如图所示:

①测定晶体结构最常用的方法是_______ (填选项字母)。
A.核磁共振氢谱 B.红外光谱 C.X射线衍射实验 D.称重法
②若晶胞中 之间的最短距离为a nm,阿伏加德罗常数的值为
之间的最短距离为a nm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
 、ZnO,一种综合回收利用的工艺流程如图所示:
、ZnO,一种综合回收利用的工艺流程如图所示:
回答下列问题:
(1)写出浸渣主要成分的一种用途:
(2)浸取液含有的配离子有
 、
、 、
、 ,
, 的中心离子为
的中心离子为 能作配体的原因是
能作配体的原因是(3)“还原”得到Cu时发生反应的氧化剂和还原剂的物质的量之比为
(4)“沉锌镍”后得到的滤液中可循环利用的物质有
(5)“脱锌”时反应的化学方程式为
(6)NiO为绿色固体,常用作搪瓷的着色剂,其晶胞结构如图所示:

①测定晶体结构最常用的方法是
A.核磁共振氢谱 B.红外光谱 C.X射线衍射实验 D.称重法
②若晶胞中
 之间的最短距离为a nm,阿伏加德罗常数的值为
之间的最短距离为a nm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为 (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
您最近一年使用:0次
解题方法
3 . 科幻电影《阿凡达》中外星人流的是蓝色的血液,其实血液的颜色主要是由血蛋白中含有的金属元素决定的,如含铁元素的为常见红色血液、含铜元素的为蓝色血液、含钒元素的为绿色血液等,铜、铁、钒在科学研究和工农业生产中有许多用途。回答下列问题:
(1)基态V的核外电子排布式为_______ 。
(2) 溶液常用作农业杀菌剂,溶液中存在
溶液常用作农业杀菌剂,溶液中存在 。该离子中存在的化学键有
。该离子中存在的化学键有_______ (填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
(3) 与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的
与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的 键和π键的个数比为
键和π键的个数比为_______ ,其中C原子的杂化轨道类型为_______ 。

(4)铜的氧化物、氮化物都广泛应用于光信息存储和高速集成电路领域。
①Cu、O、N的电负性由大到小的顺序为_______ 。
②已知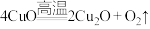 ,从铜离子的价层电子结构角度分析,高温下能转化生成
,从铜离子的价层电子结构角度分析,高温下能转化生成 的主要原因是
的主要原因是_______ 。
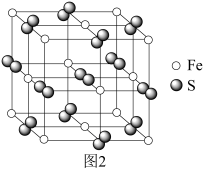
(5)铁与硫能形成多种化合物,某种化合物的晶胞结构如图2所示。该化合物的化学式是_______ ;若该晶胞边长为 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  。
。
(1)基态V的核外电子排布式为
(2)
 溶液常用作农业杀菌剂,溶液中存在
溶液常用作农业杀菌剂,溶液中存在 。该离子中存在的化学键有
。该离子中存在的化学键有A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
(3)
 与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的
与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的 键和π键的个数比为
键和π键的个数比为
(4)铜的氧化物、氮化物都广泛应用于光信息存储和高速集成电路领域。
①Cu、O、N的电负性由大到小的顺序为
②已知
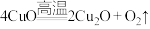 ,从铜离子的价层电子结构角度分析,高温下能转化生成
,从铜离子的价层电子结构角度分析,高温下能转化生成 的主要原因是
的主要原因是(5)铁与硫能形成多种化合物,某种化合物的晶胞结构如图2所示。该化合物的化学式是
 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
4 . 铌是汽车和飞机制造业特别重要的材料,具有良好的耐腐蚀、冷热加工等性能,以高钛渣(含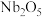 、
、 、
、 、CaO)为原料制取单质的流程如图甲所示:
、CaO)为原料制取单质的流程如图甲所示:


已知:①MIBK为甲基异丁基酮;②钽铌液中含有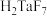 、
、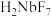 均为弱酸;③
均为弱酸;③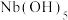 难溶于水。
难溶于水。
(1)酸溶时, 发生的反应的离子方程式为
发生的反应的离子方程式为_______ 。
(2)酸溶时,HF的浓度对铌、钽的浸出率的影响如图丙所示,则HF的最佳浓度为_______  。
。
(3)沉铌时,发生的反应的化学方程式为_______ 。
(4)电解制备铌的原理如图乙所示,阴极发生的电极反应为_______ 。
(5)铌(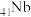 )和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
)和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:

①铌元素位于周期表中的位置是_______ 。
②图中Nb原子与Ni原子的最短距离为_______ nm。
③Nb、Ni互化物晶体的密度为_______ 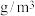 (列出计算式)。
(列出计算式)。
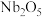 、
、 、
、 、CaO)为原料制取单质的流程如图甲所示:
、CaO)为原料制取单质的流程如图甲所示:

已知:①MIBK为甲基异丁基酮;②钽铌液中含有
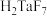 、
、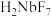 均为弱酸;③
均为弱酸;③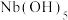 难溶于水。
难溶于水。(1)酸溶时,
 发生的反应的离子方程式为
发生的反应的离子方程式为(2)酸溶时,HF的浓度对铌、钽的浸出率的影响如图丙所示,则HF的最佳浓度为
 。
。(3)沉铌时,发生的反应的化学方程式为
(4)电解制备铌的原理如图乙所示,阴极发生的电极反应为
(5)铌(
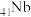 )和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
)和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
①铌元素位于周期表中的位置是
②图中Nb原子与Ni原子的最短距离为
③Nb、Ni互化物晶体的密度为
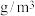 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解题方法
5 . 钛是一种稀有金属,具有密度小、强度高、耐腐蚀等特点,钛和钛的化合物在航天、化工、建筑、日常生活中都有着广泛的用途。已知:阿伏加德罗常数的值为NA。
(1)基态钛原子价电子排布式为_______ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的还有_______ 种。
(2)钛的一种常见化合物是[Ti(H2O)6]Cl3,1mol该物质中含有σ键的数目为_______ ,配体H2O的VSEPR模型名称是_______ ,其沸点高于H2S,原因是_______ 。
(3)TO2与光气(COCl2)、氯化亚砜(SOCl2)等反应可以制得TiCl4,用于制造虹彩剂、烟雾、颜料等。
①氯化亚砜中心原子的杂化方式为_______ 杂化;
②光气是_______ 分子(填“极性”或“非极性”)。
(4)铁与钛同周期,某离子型铁氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为_______ 。已知该晶体的晶胞参数为a pm,阿伏加德罗常数的值为NA,则该晶体的密度d=_______  (用含a和NA的代数式表示)。
(用含a和NA的代数式表示)。

(1)基态钛原子价电子排布式为
(2)钛的一种常见化合物是[Ti(H2O)6]Cl3,1mol该物质中含有σ键的数目为
(3)TO2与光气(COCl2)、氯化亚砜(SOCl2)等反应可以制得TiCl4,用于制造虹彩剂、烟雾、颜料等。
①氯化亚砜中心原子的杂化方式为
②光气是
(4)铁与钛同周期,某离子型铁氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为
 (用含a和NA的代数式表示)。
(用含a和NA的代数式表示)。
您最近一年使用:0次
名校
解题方法
6 . 硼元素从发现之初就有着重要用途,古埃及制造玻璃使用硼砂作溶剂,古代炼丹家也使用过硼砂。晶态硼的熔沸点高、硬度大。工业上可用碱法制备单质硼,制备流程如下:

(1)B在元素周期表中的位置是_______ 。 是有机化学中的常用试剂,其电子式为
是有机化学中的常用试剂,其电子式为_______ 。
(2)滤渣1是_______ (填化学式),通入 的目的是
的目的是_______ 。
(3)以 和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:
和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:_______ 。
(4) 是潜在的储氢材料,为白色晶体,稳定无毒。
是潜在的储氢材料,为白色晶体,稳定无毒。
① 在催化剂作用下与水反应释放氢气,另一产物的阴离子
在催化剂作用下与水反应释放氢气,另一产物的阴离子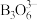 具有环状结构,写出
具有环状结构,写出 与水反应的化学方程式:
与水反应的化学方程式:_______ 。
②熔化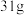
 可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:
可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:_______ 。
(5)氮化硼(BN)有多种晶形。它可以和碳一样形成与石墨相似的平面六边形的层状结构,如题图1,层中 共价键的键长比
共价键的键长比 单键的键长短,其原因是
单键的键长短,其原因是_______ 。

(6)已知立方氮化硼晶胞(图2)边长为apm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为_______  。
。


(1)B在元素周期表中的位置是
 是有机化学中的常用试剂,其电子式为
是有机化学中的常用试剂,其电子式为(2)滤渣1是
 的目的是
的目的是(3)以
 和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:
和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:(4)
 是潜在的储氢材料,为白色晶体,稳定无毒。
是潜在的储氢材料,为白色晶体,稳定无毒。①
 在催化剂作用下与水反应释放氢气,另一产物的阴离子
在催化剂作用下与水反应释放氢气,另一产物的阴离子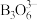 具有环状结构,写出
具有环状结构,写出 与水反应的化学方程式:
与水反应的化学方程式:②熔化
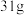
 可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:
可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:(5)氮化硼(BN)有多种晶形。它可以和碳一样形成与石墨相似的平面六边形的层状结构,如题图1,层中
 共价键的键长比
共价键的键长比 单键的键长短,其原因是
单键的键长短,其原因是
(6)已知立方氮化硼晶胞(图2)边长为apm,阿伏加德罗常数的值为
 ,则晶体的密度为
,则晶体的密度为 。
。
您最近一年使用:0次
2022-12-03更新
|
262次组卷
|
2卷引用:重庆市南开中学校2022-2023学年高三上学期第四次月考化学试题
解题方法
7 . 锰、铬、钴、铁的单质及其化合物在科研和生产中有着重要用途。回答下列问题:
(1)基态锰原子的价电子排布式为_______ 。
(2) 和
和 均为离子化合物,
均为离子化合物, 的熔点高于
的熔点高于 熔点的原因为
熔点的原因为_______ 。
(3)化学式为 的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,
的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中, 的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量
的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量 溶液,所得
溶液,所得 沉淀的物质的量之比为3∶2∶1。
沉淀的物质的量之比为3∶2∶1。
①呈暗绿色的配合物,其内界的离子符号为_______ 。
② 分子的
分子的 模型为
模型为_______ 。
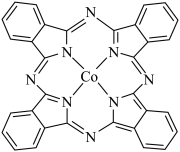
(4)如图为酞菁钴分子的平面结构,下列说法正确的是_______(填标号)。
(5)如图是一种由Y(与 同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。
同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。
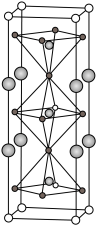
①该晶体的化学式为_______ 。
②其中Y的配位数为_______ 。
③在氧气气氛中该晶体可被部分氧化,氧原子进入晶格而使晶体呈现深紫色。新进入的氧原子在晶胞中的位置是_______ 。
(1)基态锰原子的价电子排布式为
(2)
 和
和 均为离子化合物,
均为离子化合物, 的熔点高于
的熔点高于 熔点的原因为
熔点的原因为(3)化学式为
 的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,
的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中, 的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量
的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量 溶液,所得
溶液,所得 沉淀的物质的量之比为3∶2∶1。
沉淀的物质的量之比为3∶2∶1。①呈暗绿色的配合物,其内界的离子符号为
②
 分子的
分子的 模型为
模型为(4)如图为酞菁钴分子的平面结构,下列说法正确的是_______(填标号)。

A.电负性: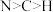 | B.4个N原子均与 形成配位键 形成配位键 |
C.分子中N的杂化轨道类型均为 | D.第一电离能: |
 同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。
同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。
①该晶体的化学式为
②其中Y的配位数为
③在氧气气氛中该晶体可被部分氧化,氧原子进入晶格而使晶体呈现深紫色。新进入的氧原子在晶胞中的位置是
您最近一年使用:0次
名校
解题方法
8 . 硼是第ⅢA族唯一的非金属元素,是农作物生长必需的微量营养元素。硼的单质及化合物都有重要用途。回答下列问题:
(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别是___________ 、___________ (填标号)。
A. B.
B. 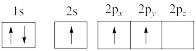
C. D.
D.
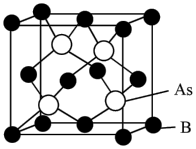
(2)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图所示),若其中有两个原子为 ,其余为
,其余为 ,则该结构单元有
,则该结构单元有___________ 种不同的结构类型。

(3)氨硼烷( )含氢量高热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高热稳定性好,是一种具有潜力的固体储氢材料。
①在第二周期中,第一电离能介于B和N之间的有___________ 种元素。
②原子个数和价电子数目均相等的微粒互称为等电子体。则与 电子数也相等的等电子体分子是
电子数也相等的等电子体分子是___________ (写分子式)。
(4)硼酸是一元弱酸,但 本身不能电离,只能通过结合来自水中的
本身不能电离,只能通过结合来自水中的 而释放出
而释放出 ,则在水溶液中
,则在水溶液中 的电离方程式为
的电离方程式为___________ 。
(5)硼与第ⅤA族元素组成的化合物氮化硼(BN)、磷化硼(BP)、砷化硼(BAs)的晶体结构与单晶硅相似,其中氮化硼(BN)和磷化硼(BP)是受到高度关注的耐磨涂料,砷化硼(BAs)是一种超高热导率半导体材料。
①氮化硼晶体的熔点要比磷化硼晶体高,其原因是___________ 。
②砷化硼(BAs)的晶胞结构如下图所示,已知阿伏加德罗常数的值为 ,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ=
,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ=___________  (列出含a、
(列出含a、 的计算式即可)。
的计算式即可)。
(6)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点,B点原子的分数坐标分别为(0,0,0)、(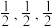 ),则C点原子的分数坐标为
),则C点原子的分数坐标为___________ 晶胞中C、D间距离
___________  。
。

(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别是
A.
 B.
B. 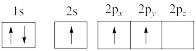
C.
 D.
D.
(2)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图所示),若其中有两个原子为
 ,其余为
,其余为 ,则该结构单元有
,则该结构单元有
(3)氨硼烷(
 )含氢量高热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高热稳定性好,是一种具有潜力的固体储氢材料。①在第二周期中,第一电离能介于B和N之间的有
②原子个数和价电子数目均相等的微粒互称为等电子体。则与
 电子数也相等的等电子体分子是
电子数也相等的等电子体分子是(4)硼酸是一元弱酸,但
 本身不能电离,只能通过结合来自水中的
本身不能电离,只能通过结合来自水中的 而释放出
而释放出 ,则在水溶液中
,则在水溶液中 的电离方程式为
的电离方程式为(5)硼与第ⅤA族元素组成的化合物氮化硼(BN)、磷化硼(BP)、砷化硼(BAs)的晶体结构与单晶硅相似,其中氮化硼(BN)和磷化硼(BP)是受到高度关注的耐磨涂料,砷化硼(BAs)是一种超高热导率半导体材料。
①氮化硼晶体的熔点要比磷化硼晶体高,其原因是
②砷化硼(BAs)的晶胞结构如下图所示,已知阿伏加德罗常数的值为
 ,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ=
,若晶胞中B原子到As原子最近距离为a pm,则该晶体的密度ρ= (列出含a、
(列出含a、 的计算式即可)。
的计算式即可)。
(6)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
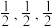 ),则C点原子的分数坐标为
),则C点原子的分数坐标为
 。
。
您最近一年使用:0次
名校
解题方法
9 . 氮及其化合物在工、农业生产中用途广泛。
(1)基态氮原子的核外电子排布式为_______ ;与N同周期的主族元素中,电负性大于N的有 _______ 种。
(2)NaN3在强烈撞击的情况下快速分解并产生大量氮气,可用于汽车安全气囊的制造。写出一种与N 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_______ ,N 的空间构型为
的空间构型为 _______ 。
(3)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是_______ 。
(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

①分子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),已知N
),已知N 为平面结构且含有大π键,则N
为平面结构且含有大π键,则N 中的大π键应表示为
中的大π键应表示为 _______ 。
②图中虚线代表氢键,其表示式为(NH )N﹣H•••Cl、
)N﹣H•••Cl、_______ 、_______ 。
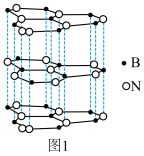
(5)氮化硼(BN)和碳一样可以形成像石墨那样的平面六角形的层状结构,如图1所示,其中B原子的杂化方式为_______ 。该氮化硼晶体具有良好的润滑性,其原因是 _______ 。
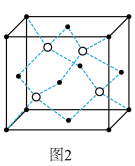
(6)一定条件下,层型BN可转变为立方氮化硼,其晶胞结构如图2所示。一个晶胞中所含B原子的数目为_______ ;已知晶体的密度为dg•cm﹣3,NA为阿伏加德罗常数的值,则晶胞边长为 _______ pm(用含d、NA的代数式表示)。
(1)基态氮原子的核外电子排布式为
(2)NaN3在强烈撞击的情况下快速分解并产生大量氮气,可用于汽车安全气囊的制造。写出一种与N
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式: 的空间构型为
的空间构型为 (3)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是
(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

①分子中的大π键可用符号Π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),已知N
),已知N 为平面结构且含有大π键,则N
为平面结构且含有大π键,则N 中的大π键应表示为
中的大π键应表示为 ②图中虚线代表氢键,其表示式为(NH
 )N﹣H•••Cl、
)N﹣H•••Cl、(5)氮化硼(BN)和碳一样可以形成像石墨那样的平面六角形的层状结构,如图1所示,其中B原子的杂化方式为

(6)一定条件下,层型BN可转变为立方氮化硼,其晶胞结构如图2所示。一个晶胞中所含B原子的数目为

您最近一年使用:0次
10 . 碳族化合物在研究和生产中有许多重要用途,请回答下列问题:
(1)已知 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为_______ 。
(2)基态锗原子(Ge)价层电子的轨道表示式为_______ 。
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因_______ 。
(4)氮化硅( )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N_______ Si—N—Si(填“>”“<”“=”)。
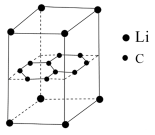
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为_______  (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
(1)已知
 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为(2)基态锗原子(Ge)价层电子的轨道表示式为
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因
(4)氮化硅(
 )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为
 (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
您最近一年使用:0次



