1 . 钒、钨、锌在工业上用途广泛。
(1)基态钒(V)元素在周期表中的位置为_______ ,其最高化合价为_______ ,与其同周期且未成对电子数相同的元素符号为_______ ;
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
则X的配离子为_______ ,Y的配体为_______ 。
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为_______ 色。

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到_______ 个钨原子。
②计算晶胞的空间利用率_______ (写出表达式,不计算具体数值)。
(1)基态钒(V)元素在周期表中的位置为
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
| 原溶液 | X溶液 | X溶液 | Y溶液 | Y溶液 |
| 所加试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则X的配离子为
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到
②计算晶胞的空间利用率
您最近一年使用:0次
2 . I.次磷酸( )是一种精细化工产品。
)是一种精细化工产品。
(1) 溶液中的含磷微粒只有
溶液中的含磷微粒只有 和
和 ,则该溶液呈
,则该溶液呈_______ 性(填“酸”“碱”或“中”)。
(2)25℃时, 溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入
溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入 溶液中水的体积
溶液中水的体积_______ (填“大于”“小于”或“等于”)加入盐酸中水的体积。
II.
(3)硅元素可形成多种晶体。
①硅与氯、溴结合能形成 、
、 ,沸点较高的是
,沸点较高的是_______ 。
②晶体Si和晶体SiC结构相似,熔点较低的是_______ 。
(4)某化合物具有超导性,其晶胞结构如图所示,则该化合物的化学式为_______ ,1个Mg与_______ 个Ni等距离且最近。

III.为了达到碳中和,研发二氧化碳、烃类等物质的利用技术已成为科研热点。
(5)



则

_______ (用 、
、 表示)。
表示)。
(6)已知反应:
 。将1molCO和2mol
。将1molCO和2mol 充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
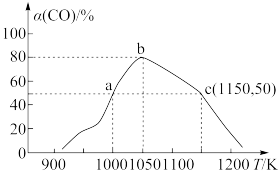
①试求温度为1000K条件下,反应开始至2min时,
_______ 。
②已知c点时容器内的压强为p,则在1150K温度下该反应的压强平衡常数 为
为_______ ( 是用各气体物质的分压替代浓度来计算的平衡常数)。
是用各气体物质的分压替代浓度来计算的平衡常数)。
 )是一种精细化工产品。
)是一种精细化工产品。(1)
 溶液中的含磷微粒只有
溶液中的含磷微粒只有 和
和 ,则该溶液呈
,则该溶液呈(2)25℃时,
 溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入
溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入 溶液中水的体积
溶液中水的体积II.
(3)硅元素可形成多种晶体。
①硅与氯、溴结合能形成
 、
、 ,沸点较高的是
,沸点较高的是②晶体Si和晶体SiC结构相似,熔点较低的是
(4)某化合物具有超导性,其晶胞结构如图所示,则该化合物的化学式为

III.为了达到碳中和,研发二氧化碳、烃类等物质的利用技术已成为科研热点。
(5)




则


 、
、 表示)。
表示)。(6)已知反应:

 。将1molCO和2mol
。将1molCO和2mol 充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
①试求温度为1000K条件下,反应开始至2min时,

②已知c点时容器内的压强为p,则在1150K温度下该反应的压强平衡常数
 为
为 是用各气体物质的分压替代浓度来计算的平衡常数)。
是用各气体物质的分压替代浓度来计算的平衡常数)。
您最近一年使用:0次
名校
3 . 下列有关物质性质与应用的对应关系正确的是
| 选项 | 性质 | 实际应用 |
| A | 小苏打不稳定,受热分解生成CO2 | 用于泡沫灭火器 |
| B | 聚乙炔是无限延伸的线状结构 | 用于导电材料 |
| C | Al(OH)3受热分解,生成高熔点物质和水 | 用作塑料的阻燃剂 |
| D | 石墨是混合型晶体,含大π键 | 用作润滑剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-22更新
|
1373次组卷
|
7卷引用:山东省济南市2022届高三3月高考模拟考试(一模)化学试题
山东省济南市2022届高三3月高考模拟考试(一模)化学试题(已下线)秘籍02 化学与STSE-备战2022年高考化学抢分秘籍(全国通用)湖北省随州市曾都区第一中学2022届高三下学期第二次学业水平选择性模拟考试化学试题(已下线)专项06 元素及其化合物-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)专题05 元素及其化合物-三年(2020-2022)高考真题分项汇编河北省五个一联盟2022-2023学年高三上学期12月联考化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)
4 . ZnGeP2是非线性晶体材料,在激光技术方面有广泛的用途。回答下列问题:
(1)基态Ge原子的价电子排布式为_______ 。
(2)O、P、K、Zn按电负性由大到小的顺序排列为______ 。
(3)H2O、PH3、KH按熔点由高到低的顺序排列为______ ,熔点差异的原因是_______ 。
(4)以Zn为顶点的ZnGeP2晶胞结构如图所示。
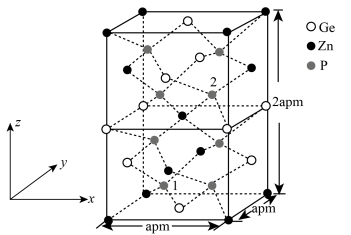
①Zn原子的配位数为________ 。
②以Ge为顶点的晶胞中,Zn原子位于______ (填写正确的字母)。
A.面心 B.棱心 C.面心和棱心
③已知晶胞中1号原子的分数坐标为( ,
, ,
, ),则2号原子的分数坐标为
),则2号原子的分数坐标为______ 。
④该晶体的密度为______ g•cm-3。
(1)基态Ge原子的价电子排布式为
(2)O、P、K、Zn按电负性由大到小的顺序排列为
(3)H2O、PH3、KH按熔点由高到低的顺序排列为
(4)以Zn为顶点的ZnGeP2晶胞结构如图所示。

①Zn原子的配位数为
②以Ge为顶点的晶胞中,Zn原子位于
A.面心 B.棱心 C.面心和棱心
③已知晶胞中1号原子的分数坐标为(
 ,
, ,
, ),则2号原子的分数坐标为
),则2号原子的分数坐标为④该晶体的密度为
您最近一年使用:0次
名校
解题方法
5 . ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_____ ;

原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为_____ ;
Se原子序数为_____ ,其核外M层电子的排布式为_____ ;
 离子的立体构型为
离子的立体构型为_____ ;
ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为_____ g·cm-3(列式并计算)。
(2)
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为
Se原子序数为
 离子的立体构型为
离子的立体构型为ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为
(2)

您最近一年使用:0次
名校
解题方法
6 . 物质的结构决定性质,依据性质在我们日常生活中才会有形形色色的用途。
I.磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷的化合物在药物生产和农药制造等方面用途非常广泛。请回答下列有关问题:
(1)画出基态P原子的核外电子排布图_____ 。
(2)NH3比PH3易液化的原因是_____ 。
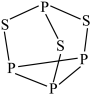
(3)P4S3可用于制造火柴,其结构如图所示。
①P4S3中硫原子的杂化轨道类型为_____ 。
②电负性:磷_____ 硫(填“>”或“<”);第一电离能磷大于硫的原因是_____ 。
(4)NH4BF4是合成氮化硼纳米管的原料之一,1molNH4BF4中含有_____ mol配位键。
Ⅱ.
(5)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为acm,则r(N3-)为_____ cm。该氮化钛的密度为_____ g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。

I.磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷的化合物在药物生产和农药制造等方面用途非常广泛。请回答下列有关问题:

(1)画出基态P原子的核外电子排布图
(2)NH3比PH3易液化的原因是
(3)P4S3可用于制造火柴,其结构如图所示。
①P4S3中硫原子的杂化轨道类型为
②电负性:磷
(4)NH4BF4是合成氮化硼纳米管的原料之一,1molNH4BF4中含有
Ⅱ.
(5)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为acm,则r(N3-)为

您最近一年使用:0次
名校
7 . 铬、铁、钴、铜等金属及其化合物在工业上有重要用途。请回答:
(1)基态铬原子的价电子排布图为 (填序号)。
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl +2CrO2Cl2+3COCl2↑。
①上述描述中涉及的非金属元素电负性由大到小的顺序是__________ (填序号)。
A.C>Cl>O B.C<Cl<O C.O>Cl>C D.C<O<Cl
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于_____ 晶体。
③配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O 的溶液中滴加2mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配合物的化学式应该写为__________ (填序号)。
A.[Cr(H2O)4Cl] Cl2·2H2O B.[Cr(H2O)4Cl2] Cl·2H2O
C.[Cr(H2O)4Cl2] Cl D.[Cr(H2O)3Cl3]·H2O
(3)Co3+与NO 形成的配合物与K+生成黄色沉淀可以检验溶液中的K+。
形成的配合物与K+生成黄色沉淀可以检验溶液中的K+。
①配体 的立体构型为
的立体构型为__________ (填序号)。
A. 三角锥形 B. 平面三角形 C.直线形 D.V形
② 的中心原子的杂化类型为
的中心原子的杂化类型为__________ (填序号)。
A. sp B. sp2 C.sp3 D.dsp2
③N原子中有_______ 种能量不同的电子。
(4)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示。

化学式为_____ 。该晶胞中只由铁原子构成的晶胞堆积模型为__________ 。若两个最近的Fe原子间的距离为a nm,则该晶体的密度是______________ (填序号)g/cm3(设阿伏加德罗常数的值为NA)。
A. B.
B. ×1030 C.
×1030 C. ×
× ×1027 D.
×1027 D.  ×1021
×1021
(5)如上述晶胞将N原子放在顶点,则Fe原子会在晶胞中出现的位置是棱心和__________ 。
(1)基态铬原子的价电子排布图为 (填序号)。
A. | B. |
C.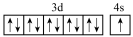 | D. |
①上述描述中涉及的非金属元素电负性由大到小的顺序是
A.C>Cl>O B.C<Cl<O C.O>Cl>C D.C<O<Cl
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于
③配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O 的溶液中滴加2mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配合物的化学式应该写为
A.[Cr(H2O)4Cl] Cl2·2H2O B.[Cr(H2O)4Cl2] Cl·2H2O
C.[Cr(H2O)4Cl2] Cl D.[Cr(H2O)3Cl3]·H2O
(3)Co3+与NO
 形成的配合物与K+生成黄色沉淀可以检验溶液中的K+。
形成的配合物与K+生成黄色沉淀可以检验溶液中的K+。①配体
 的立体构型为
的立体构型为A. 三角锥形 B. 平面三角形 C.直线形 D.V形
②
 的中心原子的杂化类型为
的中心原子的杂化类型为A. sp B. sp2 C.sp3 D.dsp2
③N原子中有
(4)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示。

化学式为
A.
 B.
B. ×1030 C.
×1030 C. ×
× ×1027 D.
×1027 D.  ×1021
×1021(5)如上述晶胞将N原子放在顶点,则Fe原子会在晶胞中出现的位置是棱心和
您最近一年使用:0次
解题方法
8 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.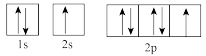 d.
d.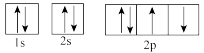
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
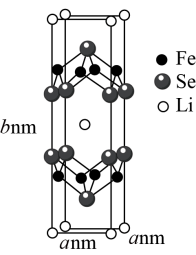
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热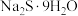 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
9 . 硼及其化合物在新材料、工农业生产等方面用途、广泛。
(1)写出基态B原子的轨道表达式___________ 。
(2)已知:硼酸的电离方程式可表示为H3BO3+H2O⇌[B(OH)4]-+H+。
①根据以上信息,下列说法正确的是_________ 。(填序号)
a.硼酸是一元酸
b.硼酸在电离的过程中,B原子的杂化类型发生了变化
c.硼酸与过量NaOH反应,能观察到白色沉淀逐渐消失
②从化学键的角度表述由H3BO3,形成[B(OH)4]-的过程__________ 。
(3)B与N可以形成不同类型的晶体,如六方氮化硼、立方氮化硼等,其结构如图。
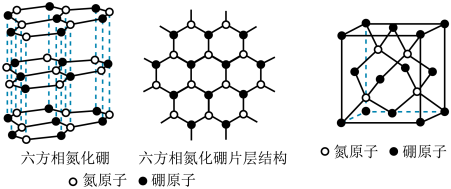
①六方氮化硼的晶体结构类似石墨,每一个B或N的杂化类型是__________ 。
②立方氮化硼因其硬度高、耐磨性好,在机械加工行业广泛用作切削工具。立方氮化硼可在高温高压的条件下由六方氮化硼转化而成。如图,立方氮化硼的晶体类型为___________ ,立方氮化硼的密度为dg⋅cm-3,阿伏加德罗常数为NA,B与N的相对原子质量分别为m和n,则立方晶胞边长a=______________ cm。

(1)写出基态B原子的轨道表达式
(2)已知:硼酸的电离方程式可表示为H3BO3+H2O⇌[B(OH)4]-+H+。
①根据以上信息,下列说法正确的是
a.硼酸是一元酸
b.硼酸在电离的过程中,B原子的杂化类型发生了变化
c.硼酸与过量NaOH反应,能观察到白色沉淀逐渐消失
②从化学键的角度表述由H3BO3,形成[B(OH)4]-的过程
(3)B与N可以形成不同类型的晶体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,每一个B或N的杂化类型是
②立方氮化硼因其硬度高、耐磨性好,在机械加工行业广泛用作切削工具。立方氮化硼可在高温高压的条件下由六方氮化硼转化而成。如图,立方氮化硼的晶体类型为
您最近一年使用:0次
解题方法
10 . 硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1) 的立体构型是
的立体构型是___________
(2) 为一元酸,与足量NaOH溶液反应得到
为一元酸,与足量NaOH溶液反应得到 ,
, 和
和 中B的杂化轨道类型分别为
中B的杂化轨道类型分别为___________ 、___________ 。
(3) 被认为是有机化学上的“万能还原剂”,
被认为是有机化学上的“万能还原剂”, 的电子式为
的电子式为___________ ,其中三种元素的电负性由大到小的顺序是___________ 。
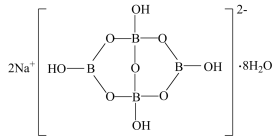
(4)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作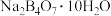 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图1所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
,其结构如图1所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是___________ (填选项字母)。
A.离子键 B.共价键 C.金属键
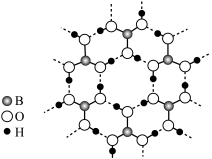
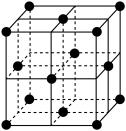
(5)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为 ,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中的位置如图2所示,其堆积方式为
,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中的位置如图2所示,其堆积方式为___________ , 占据阴离子组成的所有最小正四面体中心,该化合物的化学式为
占据阴离子组成的所有最小正四面体中心,该化合物的化学式为___________ (用最简整数比表示)。假设晶胞边长为a pm,用 代表阿伏加德罗常数的值,则该晶胞的密度为
代表阿伏加德罗常数的值,则该晶胞的密度为___________  (用含a,
(用含a, 的代数式表示)
的代数式表示)
(1)
 的立体构型是
的立体构型是(2)
 为一元酸,与足量NaOH溶液反应得到
为一元酸,与足量NaOH溶液反应得到 ,
, 和
和 中B的杂化轨道类型分别为
中B的杂化轨道类型分别为(3)
 被认为是有机化学上的“万能还原剂”,
被认为是有机化学上的“万能还原剂”, 的电子式为
的电子式为(4)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作
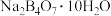 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图1所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
,其结构如图1所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是A.离子键 B.共价键 C.金属键

(5)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为
 ,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中的位置如图2所示,其堆积方式为
,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中的位置如图2所示,其堆积方式为 占据阴离子组成的所有最小正四面体中心,该化合物的化学式为
占据阴离子组成的所有最小正四面体中心,该化合物的化学式为 代表阿伏加德罗常数的值,则该晶胞的密度为
代表阿伏加德罗常数的值,则该晶胞的密度为 (用含a,
(用含a, 的代数式表示)
的代数式表示)
您最近一年使用:0次



