1 . 东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________ ,3d能级上的未成对的电子数为______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______ ,提供孤电子对的成键原子是_____ 。
③氨的沸点_____ (“高于”或“低于”)膦(PH3),原因是______ ;氨是_____ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ 。
(3)单质铜及镍都是由______ 键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1958kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______ 。
(4)某镍白铜合金的立方晶胞结构如图所示。
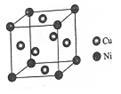
①晶胞中铜原子与镍原子的数量比为_____ 。
②若合金的密度为dg/cm3,晶胞参数a=________ nm。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
③氨的沸点
(3)单质铜及镍都是由
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为
②若合金的密度为dg/cm3,晶胞参数a=
您最近一年使用:0次
2016-12-09更新
|
8588次组卷
|
25卷引用:宁夏青铜峡市高级中学2022届高三上学期开学考试化学试题
宁夏青铜峡市高级中学2022届高三上学期开学考试化学试题宁夏育才中学2016-2017学年高二下学期期末考试化学试题【全国百强校】宁夏回族自治区吴忠中学2019届高三上学期第三次月考(期中)化学试题【全国百强校】宁夏回族自治区吴忠中学2019届高三下学期第一次模拟考试理科综合化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高二下学期期中考试化学试题宁夏银川市宁夏大学附属中学2021届高三上学期第一次月考化学试题宁夏银川市开元学校2021届高三上学期第三次月考考试化学试题2016年全国普通高等学校招生统一考试化学(新课标2卷精编版)2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷辽宁省辽阳市集美学校2017-2018学年高二3月月考化学试题云南省河口县第一中学2019届高三上学期期中考试理科综合化学试题2016年全国普通高等学校招生统一考试化学(全国2卷参考版)步步为赢 高二化学暑假作业:作业十四 物质结构与性质(选修3)四川省宜宾市第四中学2018-2019学年高二下学期期中考试化学试题山东省滨州市惠民县第二中学2018-2019学年高二5月份月考化学试题新疆阿勒泰地区第二高级中学2018-2019学年高二下学期期末(A卷)化学试题黑龙江省鸡西市鸡东县第二中学2020届高三上学期期中考试化学试题山西省忻州市第一中学2019-2020学年高二下学期期中考试化学试题2020届成都市第七中学高中毕业班四月份教学质量监测卷理科综合化学部分四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题四川省宜宾市叙州区第一中学校2020届高三下学期第四学月考试理综化学试题吉林省汪清县第六中学2019-2020学年高二6月月考化学试题黑龙江省大庆市第四中学2020届高三下学期第四次检测理综化学试题甘肃省嘉峪关市第一中学2021届高三下学期七模考试理综化学试题云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题
名校
解题方法
2 . 2019年诺贝尔化学奖授予三位开发锂离子电池的科学家。TiS2、LiCoO2和LiMnO2等都是他们研究锂离子电池的载体。回答下列问题:
(1)基态Co原子的价层电子排布图为_______ ,Co2+、Co3+能与NH3、H2O、SCN-等形成配合物,上述配位体中的第二周期元素电负性从小到大顺序是_______ 。
(2)已知第三电离能数据:I3(Mn)=3246kJ•mol-1,I3(Fe)=2957kJ•mol-1,锰的第三电离能大于铁的第三电离能,其主要原因是_______ 。
(3)据报道,在MnO2的催化下,甲醛可被氧化成CO2,在处理含HCHO的废水或空气方面有广泛应用。HCHO中键角_______ CO2中键角(填“大于”“小于”或“等于”)。
(4)工业上,采用电解熔融氯化锂制备锂,钠还原TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为605℃、-24℃,它们的熔点相差很大,其主要原因是_______ 。
(5)二氧化钛晶胞如图1所示,钛原子配位数为_______ 。氮化钛的晶胞如图2所示,图3是氮化钛的晶胞截面图(相邻原子两两相切)。已知:NA表示阿伏加德罗常数,氮化钛晶体密度为dg•cm-3.氮化钛晶胞中N原子半径为_______ pm。

(1)基态Co原子的价层电子排布图为
(2)已知第三电离能数据:I3(Mn)=3246kJ•mol-1,I3(Fe)=2957kJ•mol-1,锰的第三电离能大于铁的第三电离能,其主要原因是
(3)据报道,在MnO2的催化下,甲醛可被氧化成CO2,在处理含HCHO的废水或空气方面有广泛应用。HCHO中键角
(4)工业上,采用电解熔融氯化锂制备锂,钠还原TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为605℃、-24℃,它们的熔点相差很大,其主要原因是
(5)二氧化钛晶胞如图1所示,钛原子配位数为

您最近一年使用:0次
2021-09-06更新
|
236次组卷
|
2卷引用:宁夏吴忠中学2023-2024学年高三上学期开学第一次月考化学试题
3 . Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子中,电子填充的能量最高的能级符号为___________ 。
(2)铁的晶体有三种堆积方式,其中两种的堆积方式如下,下列说法正确的是( )
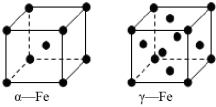
A.空间利用率α-Fe大于γ-Fe
B.α-Fe、γ-Fe晶胞中铁原子个数比为1:2
C.金属铁的导电性是由于通电时自由电子作定向移动
D.α-Fe延展时,可以转变为γ-Fe
(3)在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(4)铁氰化钾K3[Fe(CN)6]溶液是检验Fe2+常用的试剂。1 mol [Fe(CN)6]3-含σ键的数目为___________ 。
(5)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是___________ 。配体N 中心原子的杂化类型为
中心原子的杂化类型为___________ 。CoO的熔点是1 935 ℃,CoS的熔点是1 135 ℃,试分析CoO的熔点较高的原因___________ 。
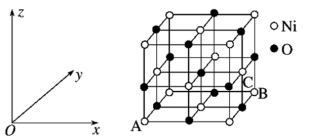
(6)NiO的晶胞结构如图所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为___________ 。
(1)基态Fe原子中,电子填充的能量最高的能级符号为
(2)铁的晶体有三种堆积方式,其中两种的堆积方式如下,下列说法正确的是

A.空间利用率α-Fe大于γ-Fe
B.α-Fe、γ-Fe晶胞中铁原子个数比为1:2
C.金属铁的导电性是由于通电时自由电子作定向移动
D.α-Fe延展时,可以转变为γ-Fe
(3)在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(4)铁氰化钾K3[Fe(CN)6]溶液是检验Fe2+常用的试剂。1 mol [Fe(CN)6]3-含σ键的数目为
(5)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
 中心原子的杂化类型为
中心原子的杂化类型为(6)NiO的晶胞结构如图所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为

您最近一年使用:0次
2021-03-04更新
|
222次组卷
|
2卷引用:宁夏银川一中2021届高三下学期返校测试理综化学试题
名校
4 . 富马酸亚铁是治疗贫血药物的一种。能有效避免添加无机铁对维生素等活性物质的破坏。请根据下列信息回答对应的问题:
(1)在“富马酸亚铁”中,亚铁离子的核外电子排布式为_______ ,其未成对电子数数量为_______
(2)富马酸的结构如图所示,结合其结构特点,下列几种溶剂中,可以溶解富马酸的有_______(填写字母选项)

(3)富马酸结构中,碳原子的杂化类型是_______ ,其中元素的电负性由大到小排序为_______ 。
(4)如图是富马酸的一种同分异构体:马来酸,其结构如图所示,查阅资料发现,富马酸的熔点在300oC,而马来酸熔点仅140oC,请用文字说明其熔点差异巨大原因:_______ 。

(5)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103oC,则Fe(CO)5中含有的化学键类型包括_______ 。Fe(CO)5的熔沸点_______ Ni(CO)4(填“高于”或“低于”)
A.极性共价键 B.离子键 C.配位键 D.金属键
(6)除了常规的药物补铁,老人家推崇“铁锅炒菜”补铁,这种补铁效果十分有限,主要原因是铁锅表面会覆盖一层四氧化三铁,或者氧化铁,不适合人体的直接吸收,反倒是锅底会存在少量的石墨与氧化亚铁,理想氧化亚铁晶体的晶胞如图所示:

已知:氧化亚铁晶体的密度为ρ g/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,Fe2+的个数为_______ ,与O2-紧邻且等距离的O2-数目为_______ ;Fe2+与O2-最短核间距为_______ pm。
(1)在“富马酸亚铁”中,亚铁离子的核外电子排布式为
(2)富马酸的结构如图所示,结合其结构特点,下列几种溶剂中,可以溶解富马酸的有_______(填写字母选项)

| A.水 | B.乙醚 | C.乙醇 | D.苯 |
(4)如图是富马酸的一种同分异构体:马来酸,其结构如图所示,查阅资料发现,富马酸的熔点在300oC,而马来酸熔点仅140oC,请用文字说明其熔点差异巨大原因:

(5)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103oC,则Fe(CO)5中含有的化学键类型包括
A.极性共价键 B.离子键 C.配位键 D.金属键
(6)除了常规的药物补铁,老人家推崇“铁锅炒菜”补铁,这种补铁效果十分有限,主要原因是铁锅表面会覆盖一层四氧化三铁,或者氧化铁,不适合人体的直接吸收,反倒是锅底会存在少量的石墨与氧化亚铁,理想氧化亚铁晶体的晶胞如图所示:

已知:氧化亚铁晶体的密度为ρ g/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,Fe2+的个数为
您最近一年使用:0次
2021-11-02更新
|
187次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期开学检测化学试题
名校
解题方法
5 . 第四周期的铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(l)基态铬原子的价电子排布式为___________ 。
(2)CrO2C12和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2C12的反应为:
K2Cr2O7+3CCl4=2KCl+2CrO2C12+3COCl2↑
① 上述反应式中非金属元素电负性由大到小的顺序是_______ (用元素符号表示)。
② 常温下CrO2C12是一种易溶于CCl4的液体,则固态CrO2C12属于______ 晶体。
③ COCl2分子中所有原子均满足8电子结构,则COCl2分子中σ键和π键的个数比为____ 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的半径分别为6.9×10-2nm 和7.8×10-2nm,则熔点:NiO______ (填“< ”、“= ”或“>” ) FeO。
(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O] ,其结构如图所示。下列说法不正确的是_____ (填字母序号)。

A.该复合物中只含有离子键和配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.CO与N2的价电子总数相同,其结构为C≡O
(5)Ca与F形成的晶体M的最小单元“晶胞”如下图所示,则M的化学式为______________ ;如果M晶体的密度为d g·cm-3,阿伏伽德罗常数为NA,则晶体中两个距离最近的F中心间的距离为_____ cm。

(l)基态铬原子的价电子排布式为
(2)CrO2C12和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2C12的反应为:
K2Cr2O7+3CCl4=2KCl+2CrO2C12+3COCl2↑
① 上述反应式中非金属元素电负性由大到小的顺序是
② 常温下CrO2C12是一种易溶于CCl4的液体,则固态CrO2C12属于
③ COCl2分子中所有原子均满足8电子结构,则COCl2分子中σ键和π键的个数比为
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的半径分别为6.9×10-2nm 和7.8×10-2nm,则熔点:NiO
(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O] ,其结构如图所示。下列说法不正确的是

A.该复合物中只含有离子键和配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.CO与N2的价电子总数相同,其结构为C≡O
(5)Ca与F形成的晶体M的最小单元“晶胞”如下图所示,则M的化学式为

您最近一年使用:0次
2017-08-15更新
|
475次组卷
|
2卷引用:宁夏吴忠市青铜峡市高级中学2021届高三上学期开学考试化学试题



