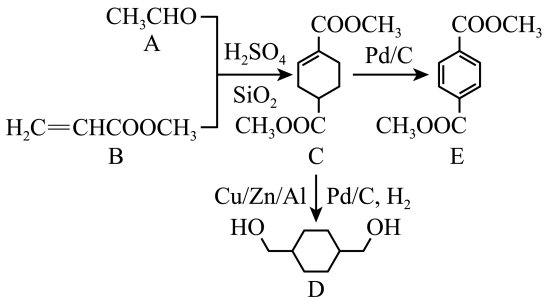
1 . 我国科学家利用生物质合成共聚酯的单体,合成时涉及多种元素,回答下列问题:
(1)基态Cu+的电子排布式为_____ 。
(2)Cu、Zn、Al的第一电离能由大到小的顺序为_____ (填元素符号,下同)。
(3)H2C=CHCOOCH3中所含元素的电负性由小到大的顺序为_____ ,该有机物中,碳原子的杂化类型是_____ 。
(4)区别晶体SiO2和非晶体SiO2的方法是_____ 。
(5)有机物C和D的相对分子质量相差较小,但是D的沸点明显高于C的,其主要原因是_____ 。
(6)我国科学家开发钙钯络合氢化物(CaPdH2)来实现乙炔高选择性合成乙烯。CaPdH2由Ca2+和[PdH2]2-(富电子)构成。CaPdH2中存在的化学键有_____ (填标号)。
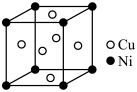
(7)白铜是我国使用最早的合金之一,白铜晶胞结构如图所示。已知晶体密度为dg·cm-3,设NA为阿伏加德罗常数的值。Cu和Ni之间的最短距离为_____ (只列计算式)nm。

(1)基态Cu+的电子排布式为
(2)Cu、Zn、Al的第一电离能由大到小的顺序为
(3)H2C=CHCOOCH3中所含元素的电负性由小到大的顺序为
(4)区别晶体SiO2和非晶体SiO2的方法是
(5)有机物C和D的相对分子质量相差较小,但是D的沸点明显高于C的,其主要原因是
(6)我国科学家开发钙钯络合氢化物(CaPdH2)来实现乙炔高选择性合成乙烯。CaPdH2由Ca2+和[PdH2]2-(富电子)构成。CaPdH2中存在的化学键有
| A.离子键 | B.配位键 | C.非极性键 | D.金属键 |

您最近一年使用:0次
2022-02-20更新
|
1020次组卷
|
6卷引用:贵州省遵义市2021-2022学年高三下学期开学考试理科综合化学试题
2 . 钒和铬都是重要的战略金属,利用钒、铬废渣(主要成分为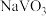 和
和 ,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。
,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。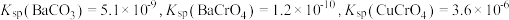 。
。
回答下列问题:
(1)基态铬原子价电子轨道表示式为_______ 。
(2)钒、铬废渣“水浸”前,先要进行粉碎处理,为提高浸取效率,还可采取的措施有_______ (任写一点)。
(3)“沉钒”的含钒产物为钒酸钙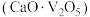 ,该过程中发生反应的化学方程式是
,该过程中发生反应的化学方程式是_______ 。
(4)“沉铬”时,铬转化为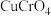 沉淀,“转化”过程中发生反应的离子方程式为
沉淀,“转化”过程中发生反应的离子方程式为_______ 。
(5)向“沉钒后液”中加入足量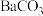 ,可将其中的铬转化为
,可将其中的铬转化为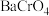 沉淀,铬的理论转化率为
沉淀,铬的理论转化率为_______ (保留三位有效数字) 。
。
(6)复合材料氧铬酸钙的立方晶胞如下图所示。_______ 。
②已知该晶体的密度为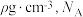 为阿伏加德罗常数的值,则相邻
为阿伏加德罗常数的值,则相邻 与
与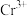 之间的最短距离为
之间的最短距离为_______ 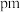 (列出计算式即可)。
(列出计算式即可)。
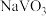 和
和 ,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。
,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。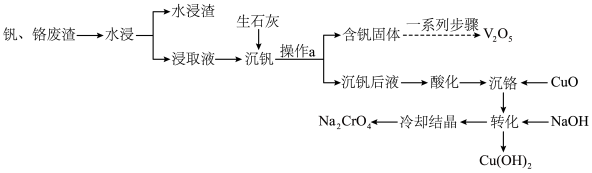
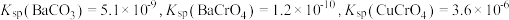 。
。回答下列问题:
(1)基态铬原子价电子轨道表示式为
(2)钒、铬废渣“水浸”前,先要进行粉碎处理,为提高浸取效率,还可采取的措施有
(3)“沉钒”的含钒产物为钒酸钙
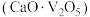 ,该过程中发生反应的化学方程式是
,该过程中发生反应的化学方程式是(4)“沉铬”时,铬转化为
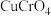 沉淀,“转化”过程中发生反应的离子方程式为
沉淀,“转化”过程中发生反应的离子方程式为(5)向“沉钒后液”中加入足量
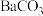 ,可将其中的铬转化为
,可将其中的铬转化为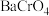 沉淀,铬的理论转化率为
沉淀,铬的理论转化率为 。
。(6)复合材料氧铬酸钙的立方晶胞如下图所示。
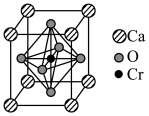
②已知该晶体的密度为
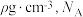 为阿伏加德罗常数的值,则相邻
为阿伏加德罗常数的值,则相邻 与
与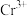 之间的最短距离为
之间的最短距离为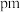 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
2024-02-27更新
|
599次组卷
|
3卷引用:贵州省黔东南苗族侗族自治州黔东南州九校联考2023-2024学年高三下学期开学化学试题
贵州省黔东南苗族侗族自治州黔东南州九校联考2023-2024学年高三下学期开学化学试题广东省湛江市2024届高三下学期第二次模拟测试化学试题(已下线)大题01 化工流程综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
3 . 科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为a pm,阿伏加德罗常数的值为NA,下列说法正确的是
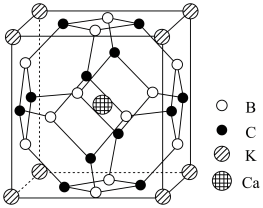

A.晶体中与 最近且距离相等的 最近且距离相等的 有12个 有12个 |
B.晶体化学式为 |
| C.该晶胞对应的晶体类型为分子晶体 |
D.晶体的密度为 |
您最近一年使用:0次
2023-08-14更新
|
167次组卷
|
2卷引用:贵州省六校联盟2024届高三开学实用性联考(一)化学试题
解题方法
4 . 请回答下列问题。
(1)基态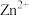 的核外电子排布式为
的核外电子排布式为______ ,钾、钠元素中第一电离能较大的是______ 。
(2)在醋酸溶液中 可与四苯硼化钠作用生成四苯硼化钾
可与四苯硼化钠作用生成四苯硼化钾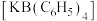 白色沉淀。四苯硼化钾的熔点是300℃,则其晶体类型是
白色沉淀。四苯硼化钾的熔点是300℃,则其晶体类型是______ 晶体。若将“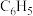 ”(苯基)视为一个整体,则阴离子
”(苯基)视为一个整体,则阴离子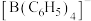 的空间构型是
的空间构型是______ ,在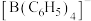 中不存在的化学键是
中不存在的化学键是______ (填字母)。
A.配位键 B.非极性键 C.π键 D.离子键
(3)已知物质间的转化关系如图甲所示,其中a、c均大于0。

①基态钠原子的第一电离能为______ 
②相同条件下, 的晶格能
的晶格能______ (填“>”“<”或“=”)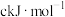 ,原因为
,原因为______ 。
(4) 的立方晶胞结构如图乙所示。若紧邻的两个
的立方晶胞结构如图乙所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为
之间的距离为dpm,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 ,则A原子的分数坐标为
,则A原子的分数坐标为______ ;Na的摩尔质量可表示为______  (用含有d、ρ、
(用含有d、ρ、 的代数式表示)。
的代数式表示)。
(1)基态
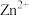 的核外电子排布式为
的核外电子排布式为(2)在醋酸溶液中
 可与四苯硼化钠作用生成四苯硼化钾
可与四苯硼化钠作用生成四苯硼化钾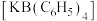 白色沉淀。四苯硼化钾的熔点是300℃,则其晶体类型是
白色沉淀。四苯硼化钾的熔点是300℃,则其晶体类型是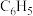 ”(苯基)视为一个整体,则阴离子
”(苯基)视为一个整体,则阴离子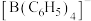 的空间构型是
的空间构型是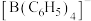 中不存在的化学键是
中不存在的化学键是A.配位键 B.非极性键 C.π键 D.离子键
(3)已知物质间的转化关系如图甲所示,其中a、c均大于0。

①基态钠原子的第一电离能为

②相同条件下,
 的晶格能
的晶格能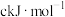 ,原因为
,原因为(4)
 的立方晶胞结构如图乙所示。若紧邻的两个
的立方晶胞结构如图乙所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为
之间的距离为dpm,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 ,则A原子的分数坐标为
,则A原子的分数坐标为 (用含有d、ρ、
(用含有d、ρ、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
5 . 某些含硫有机物可用于医药领域,如化合物I和II是重金属元素汞的解保剂。回答以下问题:

(1)已知汞位于第六周期,与锌同族,则基态汞原子的价电子排布式为_______ 。
(2)化合物I中S原子的杂化方式为_______ ,其中H、C、O三元素的电负性由小到大的顺序是_______ 。
(3)下列有关说法正确的是_______ 。
a.II中C—C—C键角是180° b.II中存在离子键与共价键
c.III中硫氧键的键能均相等 d.III中的δ键与π键之比为4∶1
(4)化合物I的结构与甘油( )相似,但是甘油在水中的溶解度更大,其原因可能是
)相似,但是甘油在水中的溶解度更大,其原因可能是_______ 。
(5)理论计算预测,由汞(Hg)、锗(Ge),锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体(晶胞如图a所示)可视为Ge晶体(晶胞如图b所示)中部分Ge原子被Hg和Sb取代后形成。

①锗晶体类型为_______ ,Ge与C同族,但Ge不能像C原子那样原子之间可以形成双键或叁键,从原子结构角度解释原因_______ 。
②X的最简式为_______ ;X的晶体中与Hg距离最近的Sb的数目为_______ 。
③设必为阿伏加德罗常数的值、X的最简式的摩尔质量为 ,用
,用 和M时的代数式表示出X晶体的密度为
和M时的代数式表示出X晶体的密度为_______  (列出计算式即可)。
(列出计算式即可)。

(1)已知汞位于第六周期,与锌同族,则基态汞原子的价电子排布式为
(2)化合物I中S原子的杂化方式为
(3)下列有关说法正确的是
a.II中C—C—C键角是180° b.II中存在离子键与共价键
c.III中硫氧键的键能均相等 d.III中的δ键与π键之比为4∶1
(4)化合物I的结构与甘油(
 )相似,但是甘油在水中的溶解度更大,其原因可能是
)相似,但是甘油在水中的溶解度更大,其原因可能是(5)理论计算预测,由汞(Hg)、锗(Ge),锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体(晶胞如图a所示)可视为Ge晶体(晶胞如图b所示)中部分Ge原子被Hg和Sb取代后形成。

①锗晶体类型为
②X的最简式为
③设必为阿伏加德罗常数的值、X的最简式的摩尔质量为
 ,用
,用 和M时的代数式表示出X晶体的密度为
和M时的代数式表示出X晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解题方法
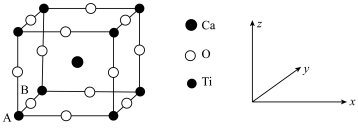
6 . 钛酸钙是一种具有优异介电特性、温度特性、机械特性以及光学特性的基础无机介电材料,钛酸钙晶胞结构如图所示。已知A的原子坐标为 ,
, 的原子坐标为
的原子坐标为 ,钛酸钙晶胞的棱长为
,钛酸钙晶胞的棱长为 。下列说法不正确的是
。下列说法不正确的是
 ,
, 的原子坐标为
的原子坐标为 ,钛酸钙晶胞的棱长为
,钛酸钙晶胞的棱长为 。下列说法不正确的是
。下列说法不正确的是
A.阳离子的半径: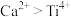 | B.钛酸钙晶体中与 距离最近的 距离最近的 有8个 有8个 |
C.B的原子坐标为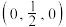 | D.钛酸钙晶体的密度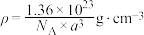 |
您最近一年使用:0次
解题方法
7 . 铬、铜、锌、硒、镉、锡等金属及其化合物具有广泛的用途,在现代工业中备受青睐。回答下列问题:
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为_______ ,铬原子价电子排布式为_______ 。
(2) 可用于去头皮屑,常温下为白色晶体,熔点340~350℃,则
可用于去头皮屑,常温下为白色晶体,熔点340~350℃,则 的晶体类型为
的晶体类型为_______ , 的分子构型为
的分子构型为_______ , 分子中
分子中 的杂化类型是
的杂化类型是_______ ,与 互为等电子体的阴离子
互为等电子体的阴离子_______ (写出一种即可)。
(3)我国科学家最新研制成功的一种纳米半导体材料可以高效实现光化学转换,该种材料主要成分为硫化镉和硫化锌。 与
与 位于同一副族,且在
位于同一副族,且在 的下一周期。已知
的下一周期。已知 熔点为2830℃;
熔点为2830℃; 熔点为1750℃,
熔点为1750℃, 熔点更高的原因为
熔点更高的原因为_______ 。
(4)黄铜常被用于制造阀门,它是 与
与 的合金,铜和锌的第二电离能大小关系为:
的合金,铜和锌的第二电离能大小关系为: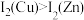 ,原因是
,原因是_______ 。
(5)磷锡青铜是有名的弹性材料,广泛用于仪器仪表中的耐磨零件和抗磁元件等。磷锡青铜晶胞结构如图所示。 代表阿伏加德罗常数的值,铜、磷原子最近距离为
代表阿伏加德罗常数的值,铜、磷原子最近距离为 。
。
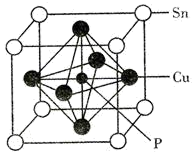
①磷锡青铜的化学式为_______ 。
②磷锡青铜晶体密度为_______  (列出计算式即可)。
(列出计算式即可)。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态
 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为(2)
 可用于去头皮屑,常温下为白色晶体,熔点340~350℃,则
可用于去头皮屑,常温下为白色晶体,熔点340~350℃,则 的晶体类型为
的晶体类型为 的分子构型为
的分子构型为 分子中
分子中 的杂化类型是
的杂化类型是 互为等电子体的阴离子
互为等电子体的阴离子(3)我国科学家最新研制成功的一种纳米半导体材料可以高效实现光化学转换,该种材料主要成分为硫化镉和硫化锌。
 与
与 位于同一副族,且在
位于同一副族,且在 的下一周期。已知
的下一周期。已知 熔点为2830℃;
熔点为2830℃; 熔点为1750℃,
熔点为1750℃, 熔点更高的原因为
熔点更高的原因为(4)黄铜常被用于制造阀门,它是
 与
与 的合金,铜和锌的第二电离能大小关系为:
的合金,铜和锌的第二电离能大小关系为: ,原因是
,原因是(5)磷锡青铜是有名的弹性材料,广泛用于仪器仪表中的耐磨零件和抗磁元件等。磷锡青铜晶胞结构如图所示。
 代表阿伏加德罗常数的值,铜、磷原子最近距离为
代表阿伏加德罗常数的值,铜、磷原子最近距离为 。
。
①磷锡青铜的化学式为
②磷锡青铜晶体密度为
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
名校
解题方法
8 . 如图为几种晶体或晶胞的示意图:
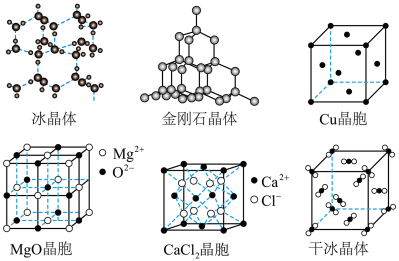
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是____ 。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:___ 。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能___ (填“大于”或“小于”)MgO晶体,原因是____ 。
(4)每个Cu晶胞中实际占有___ 个Cu原子,CaCl2晶体中Ca2+的配位数为__ 。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_____ 。

请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能
(4)每个Cu晶胞中实际占有
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是
您最近一年使用:0次
2019-09-06更新
|
255次组卷
|
20卷引用:贵州省独山县高级中学2020届高三上学期开学考试理综化学试题
贵州省独山县高级中学2020届高三上学期开学考试理综化学试题云南省广南县第三中学2020届高三上学期开学考试化学试题云南省金平县一中2020届高三上学期开学考试化学试题2018版化学(苏教版)高考总复习专题十一课时跟踪训练--微粒间作用力与物质性质云南省景东一中2017-2018学年高二下学期6月份考试化学试题云南省广南一中2019届高三上学期10月月考化学试题甘肃省武威第十八中学2018-2019学年高二下学期期中考试化学试题云南省丘北县第二中学2018-2019学年高二下学期6月份考试化学试题云南省屏边县第一中学2019-2020学年高二上学期12月月考化学试题云南省凤庆县第一中学2019-2020学年高二12月月考化学试题云南省耿马县民族中学2019-2020学年高二12月月考化学试题云南省永平县第二中学2019-2020学年高二上学期期末考试化学试题云南省陇川县第一中学2019-2020学年高二上学期期末考试化学试题云南省梁河县第一中学2019-2020学年高二上学期期末考试化学试题云南省剑川县第一中学2019-2020学年高二上学期期末考试化学试题云南省麻栗坡民族中学2019-2020学年高二上学期期末考试化学试题云南省金平县第一中学2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高二下学期期中考试化学试题云南省施甸县第三中学2019-2020学年高二12月月考化学试题山东省菏泽第一中学2021-2022学年高二下学期第一次月考化学试题
解题方法
9 . Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1)基态Cu原子的外围电子排布式为__ ,其最高能级的电子云为__ 形。
(2)SO 的空间构型为
的空间构型为___ (用文字描述);Cu2+与OH-反应能生成[Cu(OH)4]2-,Cu2+与之间OH-的化学键类型为___ ,[Cu(OH)4]2-中配位数为__ 。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为__ ,手性碳原子的数量为___ 个,由其结构推测,抗坏血酸__ 溶于水(填“难”或“易”),请解释原因__ 。

(4)Cu2O的晶胞如图2所示,则Cu原子的配位数为__ 。若NA为阿伏加德罗常数,晶体密度为ρg•cm-3,求Cu2O的晶胞边长a=__ cm。
(1)基态Cu原子的外围电子排布式为
(2)SO
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为

(4)Cu2O的晶胞如图2所示,则Cu原子的配位数为
您最近一年使用:0次
10 . 第四周期的钛、镍、铜、锌等金属元素及其化合物在工业生产和科学研究中具有重要作用。回答下列问题:
(1)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。基态Zn2+的电子排布式为__ 。葡萄糖酸根[CH2OH(CHOH)4COO-]中手性碳原子(连有四个不同的原子或基团的碳)的个数为___ 。
(2)一些中医典籍中记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。在ZnCO3中,阴离子的空间构型为____ 。
(3)镍元素可形成多种配合物。若配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=___ ;一定条件下,丁二酮肟( )与Ni2+反应生成鲜红色沉淀物的结构如图所示,该沉淀物中所含非金属元素的电负性由小到大的顺序为
)与Ni2+反应生成鲜红色沉淀物的结构如图所示,该沉淀物中所含非金属元素的电负性由小到大的顺序为___ ,碳原子的杂化类型为__ ,该结构中存在的化学键有___ (填字母选项)。

a.离子键 b.共价键 c.金属键 d.配位键
(4)工业上可用TiCl4(常温下呈液态)与Mg高温下反应制备钛单质。同时生成MgCl2,解释TiCl4熔点比MgCl2低很多的原因__ 。
(5)某镍白铜合金的立方晶胞结构如图所示,该晶胞的化学式为__ ,若晶胞参数为anm,则晶胞密度为___ g/cm3。

(1)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。基态Zn2+的电子排布式为
(2)一些中医典籍中记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。在ZnCO3中,阴离子的空间构型为
(3)镍元素可形成多种配合物。若配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
 )与Ni2+反应生成鲜红色沉淀物的结构如图所示,该沉淀物中所含非金属元素的电负性由小到大的顺序为
)与Ni2+反应生成鲜红色沉淀物的结构如图所示,该沉淀物中所含非金属元素的电负性由小到大的顺序为
a.离子键 b.共价键 c.金属键 d.配位键
(4)工业上可用TiCl4(常温下呈液态)与Mg高温下反应制备钛单质。同时生成MgCl2,解释TiCl4熔点比MgCl2低很多的原因
(5)某镍白铜合金的立方晶胞结构如图所示,该晶胞的化学式为

您最近一年使用:0次



