名校
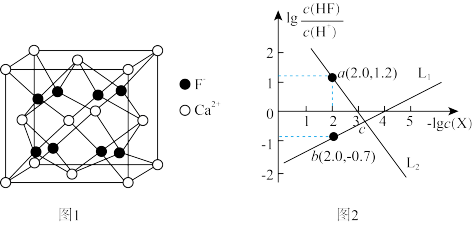
1 .  是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为a pm,
是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为a pm, 表示阿伏加德罗常数的值),难溶于水、可溶于酸。常温下,用盐酸调节
表示阿伏加德罗常数的值),难溶于水、可溶于酸。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中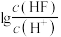 与
与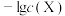 (X为
(X为 或
或 )的关系如图2所示。下列说法错误的是。
)的关系如图2所示。下列说法错误的是。
 是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为a pm,
是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为a pm, 表示阿伏加德罗常数的值),难溶于水、可溶于酸。常温下,用盐酸调节
表示阿伏加德罗常数的值),难溶于水、可溶于酸。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中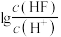 与
与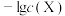 (X为
(X为 或
或 )的关系如图2所示。下列说法错误的是。
)的关系如图2所示。下列说法错误的是。
A.每个氟化钙晶胞中含有 的数目为4个 的数目为4个 |
B.氟化钙的晶体密度为 |
C. 表示 表示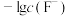 与 与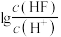 的变化曲线 的变化曲线 |
D.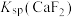 的数量级为 的数量级为 |
您最近一年使用:0次
2022-12-16更新
|
939次组卷
|
8卷引用:重庆市南开中学校2022-2023学年高二下学期开学考试化学试题
名校
解题方法
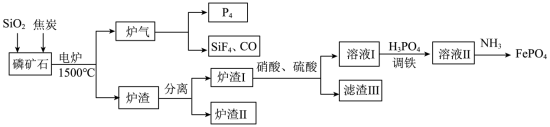
2 . “刀片电池”通过结构创新,大大提升了磷酸铁锂电池的能量密度。以下是以磷矿石(主要成分Ca5(PO4)3F,还有Fe2O3、CaCO3等杂质)为原料生产白磷(P4)同时制得刀片电池正极材料FePO4的工艺流程:
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
(1)白磷(P4)不溶于水但易溶于二硫化碳,说明P4是___________ (填“极性分子”或“非极性分子”)。
(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中FeP溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:___________ 。
(3)炉渣Ⅱ的主要成分是___________ 。
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是___________ 。若此条件下Fe3+恰好完全转化为FePO4沉淀(当溶液中某离子浓度≤1×10−5mol/L时,可视为该离子沉淀完全),过滤,现往滤液中加入2mol/L的MgCl2溶液(设溶液体积增加1倍),此时溶液中___________ Mg3(PO4)2沉淀生成(填“有”或“无”或“无法确定”)【已知FePO4、Mg3(PO4)2的Ksp分别为1.3×10−22、1.0×10−24】
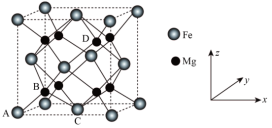
(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示: ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为___________ 。此晶胞中Fe的配位数是___________ 。
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
(1)白磷(P4)不溶于水但易溶于二硫化碳,说明P4是
(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中FeP溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:
(3)炉渣Ⅱ的主要成分是
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是
(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示:
 ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为
您最近一年使用:0次
2024-02-03更新
|
740次组卷
|
3卷引用:重庆市荣昌中学校2023-2024学年高三下学期开学考试化学试题
名校
3 . 晶体 为拓扑绝缘体材料,其结构可视为金刚石晶体中的C原子被
为拓扑绝缘体材料,其结构可视为金刚石晶体中的C原子被 和
和 取代后形成。其晶胞如图所示(已知:
取代后形成。其晶胞如图所示(已知: ),下列说法错误的
),下列说法错误的
 为拓扑绝缘体材料,其结构可视为金刚石晶体中的C原子被
为拓扑绝缘体材料,其结构可视为金刚石晶体中的C原子被 和
和 取代后形成。其晶胞如图所示(已知:
取代后形成。其晶胞如图所示(已知: ),下列说法错误的
),下列说法错误的
A.最近的两个 原子的距离 原子的距离 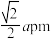 |
B.该晶胞中 原子的配位数为4 原子的配位数为4 |
C.若 原子的坐标为 原子的坐标为  ,则 ,则 原子的坐标为 原子的坐标为 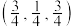 |
D.该晶胞的密度为  ( ( 为阿伏加德罗常数) 为阿伏加德罗常数) |
您最近一年使用:0次
4 . 已知,图甲为金属钠的晶胞,晶胞边长为a pm,图乙为金属钠的晶胞截面,图丙为Li2S晶胞截面(已知Li2S的晶体结构与CaF2相似)。假设晶胞边长为d pm,则下列关于Li2S晶胞的描述错误的是
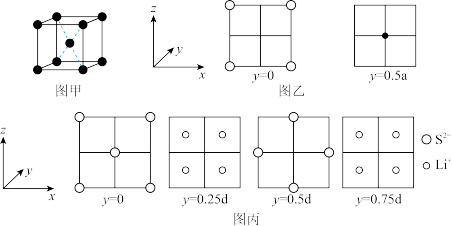

| A.每个晶胞中含有的S2-数目为4 |
| B.与Li+距离最近且相等的S2-有4个 |
| C.与Li+距离最近且相等的Li+有12个 |
D.该晶胞中两个距离最近的Li+和S2-的核间距的计算表达式为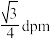 |
您最近一年使用:0次
2022-09-05更新
|
456次组卷
|
5卷引用:重庆市育才中学校2023届高三上学期开学测试化学试题
重庆市育才中学校2023届高三上学期开学测试化学试题重庆市育才中学校2023届高三上学期开学测试化学试题重庆市育才中学2022-2023学年高三上学期开学考试化学试题(已下线)易错点17 晶体结构与性质-备战2023年高考化学考试易错题江西省景德镇一中2022-2023学年高二下学期期中考试(19班)化学试题
真题
名校
5 . [化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
2016-12-09更新
|
5125次组卷
|
12卷引用:重庆市垫江县2018届高三上学期模底考试理综化学试题
重庆市垫江县2018届高三上学期模底考试理综化学试题四川省宜宾市第四中学2021届高三上学期开学考试理综化学试题2015年全国普通高等学校招生统一考试化学(新课标I卷)2016届广东省深圳第二外国语学校高三上学期第二次教学质检化学试卷2016届黑龙江省哈尔滨一中高三上学期12月月考化学试卷宁夏石嘴山市第三中学2018届高三9月月考化学试题百所名校联考-物质结构与性质云南省曲靖市第一中学2020届高三化学仿真模拟考试理科综合化学试题云南省曲靖一中2020届高考化学仿真试卷河北省石家庄市第二中学2020届高中毕业班四月份教学质量监测卷理科综合化学部分安徽省马鞍山市2020届高考第二次模拟理综化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题
名校
解题方法
6 . 镓(Ga)、锗(Ge)、硅(Si)、硒(Se)的单质及某些化合物如砷化镓、磷化镓等都是常用的半导体材料,应用于航空航天测控、光纤通讯等领域。回答下列问题:
(1)硒常用作光敏材料,基态硒原子的核外电子排布式为_______ ;与硒同周期的p区元素中第一电离能大于硒的元素有_______ 种; 的空间构型是
的空间构型是_______ 。
(2)水晶的主要成分是二氧化硅,在水晶中硅原子的配位数是_______ 。硅与氢结合能形成一系列的二元化合物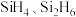 等,与氯、溴结合能形成
等,与氯、溴结合能形成 ,上述四种物质沸点由高到低顺序为
,上述四种物质沸点由高到低顺序为_______ ,丁硅烯 中
中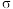 键与
键与 键个数之比为
键个数之比为_______ 。
(3)GaN、GaP、GaAs都是原子晶体,熔点如表所示,分析其熔点变化的原因_______ 。
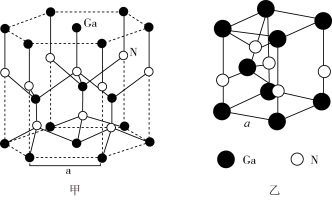
(4)GaN晶胞结构如图甲所示。已知六棱柱底边边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为
。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为 ,GaN晶体的密度为
,GaN晶体的密度为_______  (用
(用 表示)。
表示)。
(1)硒常用作光敏材料,基态硒原子的核外电子排布式为
 的空间构型是
的空间构型是(2)水晶的主要成分是二氧化硅,在水晶中硅原子的配位数是
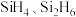 等,与氯、溴结合能形成
等,与氯、溴结合能形成 ,上述四种物质沸点由高到低顺序为
,上述四种物质沸点由高到低顺序为 中
中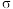 键与
键与 键个数之比为
键个数之比为(3)GaN、GaP、GaAs都是原子晶体,熔点如表所示,分析其熔点变化的原因
| GaN | GaP | GaAs | |
| 熔点 | 1700℃ | 1480℃ | 1238℃ |
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为
。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为 ,GaN晶体的密度为
,GaN晶体的密度为 (用
(用 表示)。
表示)。
您最近一年使用:0次
2021-03-08更新
|
904次组卷
|
4卷引用:重庆市育才中学2021届高三下学期入学考试化学试题
名校
解题方法
7 . Ⅰ、由CO2、甲醇为原料合成绿色化学品碳酸二甲酯(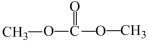 )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
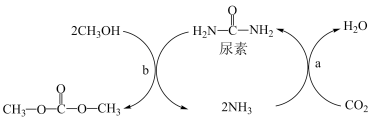
(1)下列说法不正确的是___________ (填字母)。
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.NH3极易溶解在水中,只因氨分子与水分子间形成了氢键
C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅱ、硫元素在化合物中常表现出多种化合价,它的许多化合物在研究和生产中有许多重要用途。回答下列问题:
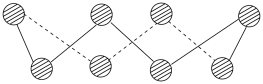
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是___________ 。
(3) 的电子式是
的电子式是___________ ,依据 理论推测
理论推测 的空间构型为
的空间构型为___________ ,常温下 是气体而
是气体而 是液体的原因是
是液体的原因是___________ 。
(4) 的键角
的键角___________  的键角(填“大于”或“小于”),理由是
的键角(填“大于”或“小于”),理由是___________ 。
(5) 在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方
在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方 晶体结构如图所示。
晶体结构如图所示。
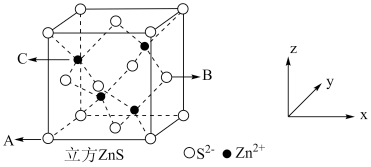
①已知A、B点的原子坐标分别为 和
和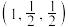 ,则C点的原子坐标为
,则C点的原子坐标为___________ ;
②若晶胞棱长为 ,密度为
,密度为___________  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
(1)下列说法不正确的是
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.NH3极易溶解在水中,只因氨分子与水分子间形成了氢键
C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅱ、硫元素在化合物中常表现出多种化合价,它的许多化合物在研究和生产中有许多重要用途。回答下列问题:
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是

(3)
 的电子式是
的电子式是 理论推测
理论推测 的空间构型为
的空间构型为 是气体而
是气体而 是液体的原因是
是液体的原因是(4)
 的键角
的键角 的键角(填“大于”或“小于”),理由是
的键角(填“大于”或“小于”),理由是(5)
 在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方
在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方 晶体结构如图所示。
晶体结构如图所示。
①已知A、B点的原子坐标分别为
 和
和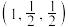 ,则C点的原子坐标为
,则C点的原子坐标为②若晶胞棱长为
 ,密度为
,密度为 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
2022-09-05更新
|
351次组卷
|
6卷引用:重庆市育才中学校2023届高三上学期开学测试化学试题
8 . 镓(熔点为29.8℃,沸点2403 ℃)是新型半导体的基础材料,随着其系列化合物砷化镓、氮化镓等在光电子和高速集成电路等高精尖领域的广泛应用,高纯镓的地位日益凸显。从粉煤灰(主要成分为 Al2O3、Ga2O3、SiO2、MgO等)中提取镓并回收铝,可变废为宝并减少污染,其中一种提取工艺如图:____________________________________ 。
(2)“焙烧”的目的主要是通过Al2O3与 Na2CO3反应破坏粉煤灰晶相中的稳定结构,活化反应物以提高后续浸出效率,写出该反应的化学方程式:___________________________________ ,滤渣的主要成分为 MgO、______________ (填化学式)。
(3)“调pH 沉镓”的原理为_________________________________________________ (用离子方程式表示),已知常温下 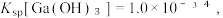 设浸出后溶液中含镓微粒的初始浓度为
设浸出后溶液中含镓微粒的初始浓度为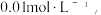 通常认为溶液中离子浓度小于
通常认为溶液中离子浓度小于 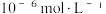 为沉淀完全。则此时应控制溶液pH不低于
为沉淀完全。则此时应控制溶液pH不低于______________________________ (保留一位小数)。
(4)“电解精炼”原理如图1所示。____________________ (用a、M表示)。
②析出纯镓的电极方程式为_______________________________________ 。
③该电解池不能采用盐酸代替 NaOH 溶液的理由是_______________________________________ 。
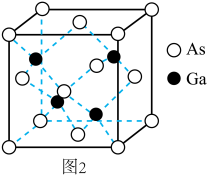
(5)以纯镓为原料可制得砷化镓,其晶体结构(图2)与金刚石类似,已知晶胞参数为a cm,阿伏加德罗常数值为NA,则砷化镓的晶体密度为_________________________ g/cm3(列出计算式)。
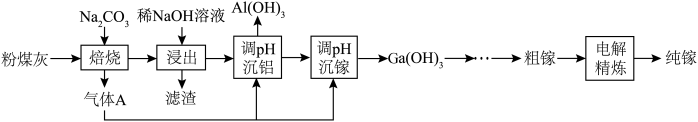
(2)“焙烧”的目的主要是通过Al2O3与 Na2CO3反应破坏粉煤灰晶相中的稳定结构,活化反应物以提高后续浸出效率,写出该反应的化学方程式:
(3)“调pH 沉镓”的原理为
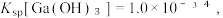 设浸出后溶液中含镓微粒的初始浓度为
设浸出后溶液中含镓微粒的初始浓度为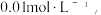 通常认为溶液中离子浓度小于
通常认为溶液中离子浓度小于 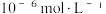 为沉淀完全。则此时应控制溶液pH不低于
为沉淀完全。则此时应控制溶液pH不低于(4)“电解精炼”原理如图1所示。

②析出纯镓的电极方程式为
③该电解池不能采用盐酸代替 NaOH 溶液的理由是
(5)以纯镓为原料可制得砷化镓,其晶体结构(图2)与金刚石类似,已知晶胞参数为a cm,阿伏加德罗常数值为NA,则砷化镓的晶体密度为
您最近一年使用:0次
9 . 六方ZnS的晶胞结构如图甲所示(高为cnm),其晶胞的上表面如图乙所示,已知 、
、 半径分别为
半径分别为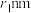 、
、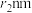 ,且
,且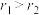 ,下列说法错误的是
,下列说法错误的是
 、
、 半径分别为
半径分别为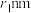 、
、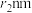 ,且
,且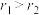 ,下列说法错误的是
,下列说法错误的是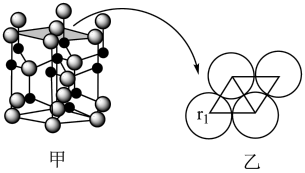
| A.ZnS的熔点低于ZnO |
B.晶胞的空间利用率为 |
C.该晶体中 占据了 占据了 构成的正四面体空隙 构成的正四面体空隙 |
D.在晶体中离 最近且等距的 最近且等距的 有12个 有12个 |
您最近一年使用:0次
名校
解题方法
10 . CO在化学链(如气相烃类)燃烧和催化CO氧化过程中均展现出良好的性能,同时具有成本低廉的优势,有望成为贵金属催化剂的替代品。中国科学院工程热物理研究所的科研人员初步揭示了CO在CuO表面的催化机理,并深入研究了CO在铜基氧化物表面的反应机制,并提出了对应的反应动力学模型。
(1)基态铜原子的价电子排布式为_______ ,其核外电子占据的原子轨道有_______ 种伸展方向。
(2)N与C、O同周期,H、C、N三种元素的电负性从小到大的顺序为_______ ;C、N、O第一电离能从大到小的顺序为_______ 。
(3)CO分子中σ键与π键的数目之比为_______ 。
(4)已知 的熔点高于
的熔点高于 的熔点,其原因是
的熔点,其原因是_______ 。
(5)铜的某氧化物的晶胞如图所示,该晶胞中Cu原子与O原子之间的最近距离为a pm,阿伏加德罗常数的值为NA,则该晶胞的密度为_______  (填含a、NA的代数式)。
(填含a、NA的代数式)。

(1)基态铜原子的价电子排布式为
(2)N与C、O同周期,H、C、N三种元素的电负性从小到大的顺序为
(3)CO分子中σ键与π键的数目之比为
(4)已知
 的熔点高于
的熔点高于 的熔点,其原因是
的熔点,其原因是(5)铜的某氧化物的晶胞如图所示,该晶胞中Cu原子与O原子之间的最近距离为a pm,阿伏加德罗常数的值为NA,则该晶胞的密度为
 (填含a、NA的代数式)。
(填含a、NA的代数式)。
您最近一年使用:0次
2022-09-11更新
|
232次组卷
|
2卷引用:重庆八中2022-2023学年高三上学期入学考试化学试题



