1 .
(1)I.下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
II.黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
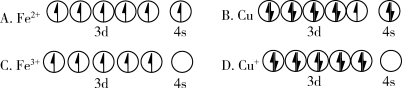
(2)CuFeS2中存在的化学键类型是________________ 。下列基态原子或离子的价层电子排布图正确的_____________ 。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是______ ,中心原子杂化类型为__________ ,属于_______ (填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是____________________ 。
(4)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为_____ ,共价键的类型有_________ 。
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为__________ ,S2-的配位数为____________ 。
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏伽德罗常数的值,CuFeS2晶体的密度是________ g•cm-3(列出计算式)。
(1)I.下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
II.黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(2)CuFeS2中存在的化学键类型是

(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水低的主要原因是
(4)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏伽德罗常数的值,CuFeS2晶体的密度是
您最近一年使用:0次
2018-11-28更新
|
3021次组卷
|
3卷引用:新疆第二师八一中学2022-2023学年高三上学期开学考试化学试题
名校
2 . 镓的化合物
(1)半导体工业中通过刻蚀制造微纳结构,GaN是重要的半导体材料,通常采用含氯气体在放电条件下进行刻蚀。写出利用Ar-Cl2混合气体放电刻蚀GaN的化学方程式_____ 。
(2)金属镓熔点很低但沸点很高其中存在二聚体Ga.1990年,科学家将液态Ga和l2在甲苯中超声处理,得到了组成为Gal的物质。该物质中含有多种不同氧化态的Ga,具有两种可能的结构,分子式分别为Ga4I4(A)和Ga6I6(B),二者对应的阴离子分别为C和D,两种阴离子均由Ga和I构成且其中所有原子的价层均满足8电子。写出示出A和B组成特点的结构笱式并标出Ga的氧化态_____ ,画出C和D的结构_____ 。
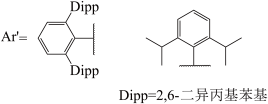
(3)GaI常用于合成低价Ga的化合物。将GaI与Ar’Li(Ar’基如图所示,解答中直接采用简写Ar’)在-78℃的甲苯溶液中反应,得到晶体E,E中含有2个Ga原子:E在乙醚溶液中与金属钠反应得到晶体F,X射线晶体学表明,F中的Ga-Ga键长比E中短0.028nm。关于F中Ga-Ga的键级历史上曾有过争议,其中一种观点认为,F中的Ca价层满足8电子。基于该观点,画出E和F的结构式_____ 。
(1)半导体工业中通过刻蚀制造微纳结构,GaN是重要的半导体材料,通常采用含氯气体在放电条件下进行刻蚀。写出利用Ar-Cl2混合气体放电刻蚀GaN的化学方程式
(2)金属镓熔点很低但沸点很高其中存在二聚体Ga.1990年,科学家将液态Ga和l2在甲苯中超声处理,得到了组成为Gal的物质。该物质中含有多种不同氧化态的Ga,具有两种可能的结构,分子式分别为Ga4I4(A)和Ga6I6(B),二者对应的阴离子分别为C和D,两种阴离子均由Ga和I构成且其中所有原子的价层均满足8电子。写出示出A和B组成特点的结构笱式并标出Ga的氧化态

(3)GaI常用于合成低价Ga的化合物。将GaI与Ar’Li(Ar’基如图所示,解答中直接采用简写Ar’)在-78℃的甲苯溶液中反应,得到晶体E,E中含有2个Ga原子:E在乙醚溶液中与金属钠反应得到晶体F,X射线晶体学表明,F中的Ga-Ga键长比E中短0.028nm。关于F中Ga-Ga的键级历史上曾有过争议,其中一种观点认为,F中的Ca价层满足8电子。基于该观点,画出E和F的结构式
您最近一年使用:0次
2023-09-07更新
|
308次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高三下学期开学化学试题
解题方法
3 . 一种新型硫酸盐功能电解液由2mol·L-1Na2SO4和0.3mol·L-1MgSO4混合组成,电化学测试表明该电解液构建的Na2Ni[Fe(CN)6]、NaTi2(PO4)3/C电池可以稳定循环500次以上。
请回答下列问题:
(1)MgSO4中三种原子的半径由大到小的顺序是___________ (用元素符号表示),其中电负性最大的元素是___________ (填名称)。
(2)第一电离能N>O的原因是___________ 。
(3)Na2Ni[Fe(CN)6]中,基态Fe2+核外电子的空间运动状态有___________ 种,[Fe(CN)6]4-中σ键和π键的数目之比为___________ 。
(4)NaTi2(PO4)3中, 中磷原子的杂化类型是
中磷原子的杂化类型是___________ 。
(5)N、O两种元素形成的简单氢化物的熔点:NH3___________ H2O(填“>”“<”或“=”),其原因是___________ 。
(6)NiaMgbFec的立方晶胞结构如图所示。已知晶胞的边长为npm,设NA为阿伏加德罗常数的值。

①a:b:c=___________ 。
②该晶体密度是___________ g·cm-3(用含n、NA的代数式表示)。
请回答下列问题:
(1)MgSO4中三种原子的半径由大到小的顺序是
(2)第一电离能N>O的原因是
(3)Na2Ni[Fe(CN)6]中,基态Fe2+核外电子的空间运动状态有
(4)NaTi2(PO4)3中,
 中磷原子的杂化类型是
中磷原子的杂化类型是(5)N、O两种元素形成的简单氢化物的熔点:NH3
(6)NiaMgbFec的立方晶胞结构如图所示。已知晶胞的边长为npm,设NA为阿伏加德罗常数的值。

①a:b:c=
②该晶体密度是
您最近一年使用:0次
2023-04-26更新
|
279次组卷
|
3卷引用:新疆疏附县第一中学2023-2024学年高三上学期开学摸底测试化学试题
新疆疏附县第一中学2023-2024学年高三上学期开学摸底测试化学试题河南省名校大联考2023届高三下学期三模考试理综化学试题(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)
名校
解题方法
4 . 过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)Cr 是第___________ 周期第___________ 族元素。
(2)基态 Cr 原子的核外电子有___________ 种空间运动状态,有___________ 个未成对电子。
(3)Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为___________ 。
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是___________ ,H2O 的键角小于 NH3,原因是___________ 。
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是___________ 原子。若 NA 表示阿伏加德罗常数的值,则该晶体的密度为___________ g∙cm−3(用含 a、c 和 NA 的代数式表示)。晶胞中长、宽为a nm,高为c nm。
(1)Cr 是第
(2)基态 Cr 原子的核外电子有
(3)Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是

您最近一年使用:0次
2022-01-07更新
|
352次组卷
|
3卷引用:新疆喀什第二中学2021-2022学年高三下学期开学考试化学试题
名校
5 . [化学——选修3:物质结构与性质]
周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a是组成物质种类最多的元素,c是地壳中含量最多的元素,d与a同族,e2+离子3d轨道中有9个电子。回答下列问题:
(1)e原子的价层电子排布图为____________
(2)晶体d、晶体da晶体ac2的熔点由高到低的顺序为____________ (用化学用语表示,下同),a、b、c三种元素的第一电离能由大到小的顺序为________________________ 。
(3)元素b、c形成两种常见阴离子bc2-和bc3-,其中bc2-离子的中心原子杂化轨道类型为____________ ,bc3-离子的空间构型为____________ 。
(4)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。请写出得到深蓝色透明溶液的离子方程式________________________ ,析出深蓝色晶体时加入乙醇的作用是________________________ 。
(5)e单质的晶胞结构如图所示,e原子半径为rpm,e晶体密度的计算式为____________ g·cm3。(用含NA、r的表达式表示)

周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a是组成物质种类最多的元素,c是地壳中含量最多的元素,d与a同族,e2+离子3d轨道中有9个电子。回答下列问题:
(1)e原子的价层电子排布图为
(2)晶体d、晶体da晶体ac2的熔点由高到低的顺序为
(3)元素b、c形成两种常见阴离子bc2-和bc3-,其中bc2-离子的中心原子杂化轨道类型为
(4)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。请写出得到深蓝色透明溶液的离子方程式
(5)e单质的晶胞结构如图所示,e原子半径为rpm,e晶体密度的计算式为

您最近一年使用:0次
2020-09-09更新
|
426次组卷
|
3卷引用:新疆昌吉市第九中学2021届高三上学期开学考试化学试题
6 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物( )。回答下列问题:
)。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_____ 。橄榄石中,各元素电负性大小顺序为_____ ,铁的化合价为_____ 。
(2)已知一些物质的熔点数据如下表:
 与
与 均为第三周期元素,分析同族元素的氯化物
均为第三周期元素,分析同族元素的氯化物 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因_____ 。 的空间结构为
的空间结构为_____ ,其中 的轨道杂化形式为
的轨道杂化形式为_____ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有_____ 个 。该物质化学式为
。该物质化学式为_____ 。

 )。回答下列问题:
)。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)已知一些物质的熔点数据如下表:
| 物质 |  |  |  |  |
| 熔点/℃ | 800.7 |  | 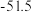 |  |
 与
与 均为第三周期元素,分析同族元素的氯化物
均为第三周期元素,分析同族元素的氯化物 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因 的空间结构为
的空间结构为 的轨道杂化形式为
的轨道杂化形式为(3)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有
 。该物质化学式为
。该物质化学式为
您最近一年使用:0次
名校
解题方法
7 . 钾和碘的相关化合物在化工医药材料等领域有广泛的应用。回答下列问题:
(1)IO3-离子的立体构型的名称为____ ,中心原子的杂化方式为____ 。
(2)HIO4的酸性强于HIO3,其原因为____ 。
(3)KIO3晶体是一种性能良好的非线性光学材料,晶胞如图。晶胞的棱长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,K与I间的最短距离为____ nm,与K紧邻的O的个数为____ 。

(1)IO3-离子的立体构型的名称为
(2)HIO4的酸性强于HIO3,其原因为
(3)KIO3晶体是一种性能良好的非线性光学材料,晶胞如图。晶胞的棱长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,K与I间的最短距离为

您最近一年使用:0次
2020-04-04更新
|
128次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高三下学期开学化学试题
名校
解题方法
8 . 卤族元素的单质和化合物在生产生活中有重要的用途。
(1)溴原子的价电子排布图为__________ 。
(2)在一定浓度的 HF 溶液中,氟化氢是以缔合形式(HF)2 存在的。使氟化氢分子缔合的作用力是____________ 。
(3)根据下表数据,分析熔点和硬度变化的原因:________________ 。
(4)HIO3 的酸性_____ (填“>”或“<”)HIO4,原因是_________________ 。
(5)晶胞有两个基本要素:①坐标参数:表示晶胞内部各微粒的相对位置。下图是 CaF2 的晶胞,其中原子坐标参数 A 为(0,0,0);B 为(1/2, 1/2,0);C 为(1,1,1)。则 D 微粒的坐标参数为____ 。

②晶胞参数(即晶胞边长):描述晶胞的大小和形状。已知 CaF2 晶体的密度为 c g•cm3,则晶胞中 Ca2+与离它最近的 F之间的距离为______ nm(设 NA 为阿伏加德罗常数的值,用含 c、NA 的式子表示)。
(1)溴原子的价电子排布图为
(2)在一定浓度的 HF 溶液中,氟化氢是以缔合形式(HF)2 存在的。使氟化氢分子缔合的作用力是
(3)根据下表数据,分析熔点和硬度变化的原因:
| NaF | NaCl | MgO | CaO | |
熔点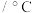 | 993 | 801 | 2852 | 2614 |
| 摩氏硬度 | 3.2 | 2.5 | 6.5 | 4.5 |
(5)晶胞有两个基本要素:①坐标参数:表示晶胞内部各微粒的相对位置。下图是 CaF2 的晶胞,其中原子坐标参数 A 为(0,0,0);B 为(1/2, 1/2,0);C 为(1,1,1)。则 D 微粒的坐标参数为

②晶胞参数(即晶胞边长):描述晶胞的大小和形状。已知 CaF2 晶体的密度为 c g•cm3,则晶胞中 Ca2+与离它最近的 F之间的距离为
您最近一年使用:0次
名校
解题方法
9 . 某绿色农药结构简式如图,回答下列问题。

(1)基态硒原子价电子排布式为__________ ,该农药组成元素中,第一电离能较大的前三种元素是________ (按由大到小顾序排列)。
(2)分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为_________ ;CSe2首次是由H2Se 和CCl4 反应制取的,试比较上述三种分子的键角_____________ (按由大到小顺序排列)。
(3)H2SeO3 分子的中心原子杂化类型是____________ ,试比较H2SeO3、H2SeO4 和H2SO4三种酸的酸性强弱(按由强到弱顺序排列)_______________ 。
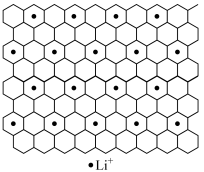
(4)石墨是碳元素的一种同素异形体,石墨晶体可看作ABABA...堆积方式。碱金属离子可填充在石墨层问形成石墨夹层化合物,同时堆积方式从ABABAB...变为AAAA...。下图为石墨夹层化合物W 的投影图,试写出W 的学式_____ ,微粒之间存在的化学键有______ 。

(1)基态硒原子价电子排布式为
(2)分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为
(3)H2SeO3 分子的中心原子杂化类型是
(4)石墨是碳元素的一种同素异形体,石墨晶体可看作ABABA...堆积方式。碱金属离子可填充在石墨层问形成石墨夹层化合物,同时堆积方式从ABABAB...变为AAAA...。下图为石墨夹层化合物W 的投影图,试写出W 的学式

您最近一年使用:0次



