1 . 我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为___________ ;单晶硅的晶体类型为___________ 。SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为___________ 。SiCl4可发生水解反应,机理如下:
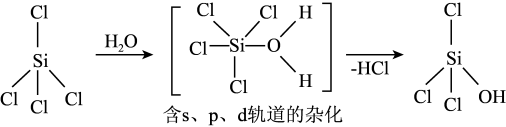
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为___________ (填标号)。
(2)CO2分子中存在___________ 个 键和
键和___________ 个 键。
键。
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是___________ ,晶胞参数为a pm、a pm、c pm,该晶体密度为___________ g·cm-3(写出表达式)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnxZr1-xOy,则y=___________ (用x表达)。

(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)CO2分子中存在
 键和
键和 键。
键。(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是

您最近一年使用:0次
2021-06-11更新
|
21210次组卷
|
26卷引用:陕西省渭南市蒲城县尧山中学2023-2024学年高三下学期开学收心考试理综试题-高中化学
陕西省渭南市蒲城县尧山中学2023-2024学年高三下学期开学收心考试理综试题-高中化学陕西省宝鸡市渭滨区2022届高考模拟(一)化学试题2021年高考全国甲卷化学真题北京首都师范大学附属中学2021-2022学年高三上学期10月月考化学试题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国甲卷化学试题变式题黑龙江省哈尔滨市第三中学校2021-2022学年高三上学期第四次验收考试理科综合化学试题2020年全国卷Ⅰ理综化学高考真题变式题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)(已下线)微专题50 分子的立体结构的判断-备战2023年高考化学一轮复习考点微专题江西省重点校联盟2022-2023学年高三上学期10月联考化学试题天津市咸水沽第一中学2022-2023学年高三上学期线上期末考试化学试题天津市静海区第一中学2020-2021学年高三下学期第三次模拟考试化学试题(已下线)第五章 物质结构与性质 元素周期律 第32讲 物质结构与性质综合题研究(已下线)第四部分 物质结构与性质 综合提能训练(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)上海市实验学校2023-2024学年高三上学期第一次月考化学试题
名校
解题方法
2 . 全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有_______ 种,若其电子排布式表示为[ Ne]3s2 违背了
违背了_______ 。
(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3_______ SiCl4(填“>”或“<”),与SiCl4互为等电子体的离子为_______ (任写1种即可)。已知电负性:H>Si,则SiHCl3充分水解的化学方程式为_______ 。
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是_______ (填字母标号)。
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度_______ (填“高”或“低”),解释原因_______ 。
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则r(Ti3+)为_______ D,该氮化钛的密度_______ g· cm-3(列出计算式即可)。

(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有
 违背了
违背了(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则r(Ti3+)为

您最近一年使用:0次
2022-04-14更新
|
1939次组卷
|
11卷引用:陕西师范大学附属中学、渭北中学等2022-2023学年高三上学期期初检测化学联考试题
陕西师范大学附属中学、渭北中学等2022-2023学年高三上学期期初检测化学联考试题陕西师范大学附属中学、渭北中学等2023届高三上学期期初检测联考化学试题山西省临汾市2022届高考考前适应性训练考试(二)理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷01(全国甲卷)广东省茂名市普通高中毕业班2022届高三下学期模拟考试化学试题北京市第二中学2022届高三下学期五月模拟考试化学试题广东省广州市第六中学2022届高三第三次模拟考试化学试题广西南宁市第二中学2021-2022学年高三下学期收网题理综化学试题(已下线)第21练 新高考模式综合练(广东卷)-2022年【暑假分层作业】高二化学(2023届一轮复习通用)新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
3 . 如图所示是晶体结构中的一部分,图中 、
、 、
、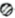 分别表示原子X、Y、Z。其对应的化学式
分别表示原子X、Y、Z。其对应的化学式
A.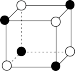 XY XY | B.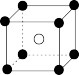 X2Y X2Y |
C.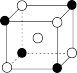 X3Y X3Y | D.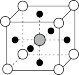 XY3Z XY3Z |
您最近一年使用:0次
2022-05-01更新
|
608次组卷
|
8卷引用:陕西省咸阳市实验中学2022-2023学年高二上学期开学质量检测化学试题
名校
解题方法
4 . 观察下列模型并结合信息,判断有关说法错误的是
| 晶体硼的结构单元 (有12个  原子) 原子) |  分子 分子 |  分子 分子 |  | |
| 结构模型 示意图 | 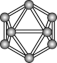 |  | 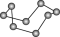 |  |
| A.固态硫S8中S原子为sp2杂化 |
| B.SF6中心原子的价层电子对数为6,其中S-F键的键长、键能均相等 |
| C.晶体硼的结构单元中含有30个B-B键,含20个正三角形 |
| D.HCN的结构式为H-C≡N |
您最近一年使用:0次
名校
解题方法
5 . 我国科学家在FeS2表面自组装单原子层Cu5纳米团簇构筑双催化剂实现H2O2到·OH的稳定持续活化。FeS2的晶胞结构如图所示。已知:晶胞参数为a pm。下列说法错误的是


| A.每个晶胞中含有4个Fe2+ |
| B.H2O2和FeS2中都含有非极性键 |
C. 和 和 之间的最短距离为 之间的最短距离为 a pm a pm |
D.Fe2+位于 形成的正八面体空隙中 形成的正八面体空隙中 |
您最近一年使用:0次
2022-06-04更新
|
227次组卷
|
4卷引用:陕西省咸阳市实验中学2022-2023学年高二上学期开学质量检测化学试题
名校
解题方法
6 . 铀氮化合物是核燃料循环系统中的重要材料。已知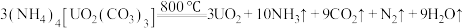 。回答下列问题:
。回答下列问题:
(1)基态氮原子价电子轨道表示式为______ 。
(2)反应中断裂的化学键有______ (填字母)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(3) 的空间构型为
的空间构型为______ 。
(4)反应所得的气态产物中属于非极性分子的是______ (填化学式,下同):氢化物中更易与 形成配离子的是
形成配离子的是______ 。向 溶液中滴加少量氨水,反应现象为
溶液中滴加少量氨水,反应现象为______ 。
(5)基态U原子的价电子排布式为 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是______ (填字母)。
a. b.
b.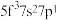 c.
c.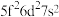 d.
d.
(6)某种铀氮化物的晶胞如图。已知晶胞密度为 ,U原子半径为
,U原子半径为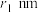 ,N原子半径为
,N原子半径为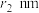 ,设
,设 为阿伏加德罗常数的值,则该晶胞的空间利用率为
为阿伏加德罗常数的值,则该晶胞的空间利用率为______ (用含d、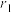 、
、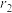 、
、 的式子表示)。
的式子表示)。

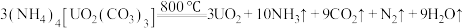 。回答下列问题:
。回答下列问题:(1)基态氮原子价电子轨道表示式为
(2)反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(3)
 的空间构型为
的空间构型为(4)反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,反应现象为
溶液中滴加少量氨水,反应现象为(5)基态U原子的价电子排布式为
 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是a.
 b.
b.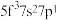 c.
c.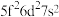 d.
d.
(6)某种铀氮化物的晶胞如图。已知晶胞密度为
 ,U原子半径为
,U原子半径为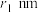 ,N原子半径为
,N原子半径为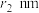 ,设
,设 为阿伏加德罗常数的值,则该晶胞的空间利用率为
为阿伏加德罗常数的值,则该晶胞的空间利用率为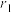 、
、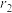 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
7 . 西北工业大学一课题组借用足球烯核心成功实现了高效且选择性可精准定制的离子跨膜输运(如图所示)。

已知:图中有机物称为“冠醚”,命名规则是“原子个数-冠醚-氧原子个数”,如 的名称为12-冠醚-4。
的名称为12-冠醚-4。
请回答下列问题:
(1)基态 最外层电子云轮廓图为
最外层电子云轮廓图为________ ,基态钠原子核外电子排布式为_________ 。
(2)运输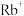 的冠醚名称是
的冠醚名称是___________ 。冠醚与碱金属离子之间存在微弱的配位键,配位原子是氧,不是碳,其原因是___________ 。
(3)几种冠醚与识别的碱金属离子如表所示:
①18-冠醚-6不能识别和运输 和
和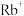 的原因是
的原因是___________ 。
②冠醚不能识别和运输阴离子的主要原因是___________ 。
(4)足球烯如图1所示。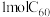 含
含___________  键。
键。

(5)锂晶胞为最密六方堆积,如图2所示。图2中底边长为 ,高为
,高为 为阿伏加德罗常数的值。锂晶体的密度为
为阿伏加德罗常数的值。锂晶体的密度为___________  。
。


已知:图中有机物称为“冠醚”,命名规则是“原子个数-冠醚-氧原子个数”,如
 的名称为12-冠醚-4。
的名称为12-冠醚-4。请回答下列问题:
(1)基态
 最外层电子云轮廓图为
最外层电子云轮廓图为(2)运输
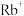 的冠醚名称是
的冠醚名称是(3)几种冠醚与识别的碱金属离子如表所示:
| 冠醚 | 冠醚空腔直径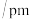 | 适合的粒子(直径 |
| 12-冠醚-4 |  |  |
| 15-冠醚-5 | 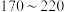 | 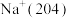 |
| 18-冠醚-6 | 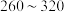 |  |
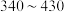 |  | |
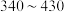 | 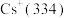 |
 和
和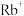 的原因是
的原因是②冠醚不能识别和运输阴离子的主要原因是
(4)足球烯如图1所示。
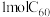 含
含 键。
键。
(5)锂晶胞为最密六方堆积,如图2所示。图2中底边长为
 ,高为
,高为 为阿伏加德罗常数的值。锂晶体的密度为
为阿伏加德罗常数的值。锂晶体的密度为 。
。
您最近一年使用:0次
名校
8 . 材料科学发展日新月异。

(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子 层上的未成对电子数为
层上的未成对电子数为_____ 。
(2)硫酸镍溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是_____ 。
②在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为_____ ,提供孤电子对的成键原子是_____ 。
(3)将 应用于超导体、材料科学等领域的探索正在不断地深入。
应用于超导体、材料科学等领域的探索正在不断地深入。 的结构如图1,
的结构如图1,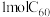 分子中
分子中 键的数目为
键的数目为_____ 。 能在二硫化碳中溶解而不溶于水的原因是
能在二硫化碳中溶解而不溶于水的原因是_____ 。
(4)某金属 与
与 可制备一种超导材料,晶胞如图2所示,
可制备一种超导材料,晶胞如图2所示, 原子位于晶胞的棱上与内部。该材料的化学式为
原子位于晶胞的棱上与内部。该材料的化学式为_____ 。
(5)石墨的晶体结构如图3(甲)所示,碳原子的杂化方式为_____ ,图3(乙)虚线勾勒出的是其晶胞,则石墨晶胞含碳原子个数为_____ 个。
(6)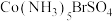 可形成两种配合物,已知
可形成两种配合物,已知 的配位数是6,为确定
的配位数是6,为确定 的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加
的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀;在第二种配合物溶液中加入
溶液时,产生白色沉淀;在第二种配合物溶液中加入 溶液时,无明显现象。第二种配合物的化学式为
溶液时,无明显现象。第二种配合物的化学式为_____ ,该配合物的配体是_____ 。

(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子
 层上的未成对电子数为
层上的未成对电子数为(2)硫酸镍溶于氨水形成
 蓝色溶液。
蓝色溶液。①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为(3)将
 应用于超导体、材料科学等领域的探索正在不断地深入。
应用于超导体、材料科学等领域的探索正在不断地深入。 的结构如图1,
的结构如图1,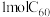 分子中
分子中 键的数目为
键的数目为 能在二硫化碳中溶解而不溶于水的原因是
能在二硫化碳中溶解而不溶于水的原因是(4)某金属
 与
与 可制备一种超导材料,晶胞如图2所示,
可制备一种超导材料,晶胞如图2所示, 原子位于晶胞的棱上与内部。该材料的化学式为
原子位于晶胞的棱上与内部。该材料的化学式为(5)石墨的晶体结构如图3(甲)所示,碳原子的杂化方式为
(6)
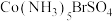 可形成两种配合物,已知
可形成两种配合物,已知 的配位数是6,为确定
的配位数是6,为确定 的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加
的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀;在第二种配合物溶液中加入
溶液时,产生白色沉淀;在第二种配合物溶液中加入 溶液时,无明显现象。第二种配合物的化学式为
溶液时,无明显现象。第二种配合物的化学式为
您最近一年使用:0次
9 . 一种稳定的水溶性(Co)配合物的结构简式如图(Ac表示 ),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。
),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。

回答下列问题:
(1)基态Co的价电子排布式为______ 。Co元素在元素周期表的位置为______ 。
(2)Na、K等金属在焰色试验中可以观察到焰色,Fe、Co等金属则观察不到焰色,请解释原因:______ 。
(3)关于如图所示的配合物,下列说法正确的是______(填标号)。
(4)Co可以形成多种配合物,一种配合物的化学式为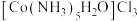 ,该配合物的配体为
,该配合物的配体为______ (填化学式),配位原子的杂化方式为______ 。
(5) 具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于
具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于______ 位置(填“顶点”“棱心”“面心”或“体心”)。已知 的晶体密度为
的晶体密度为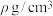 ),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的
),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的 可表示为
可表示为______  (填表达式)。
(填表达式)。

 ),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。
),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。
回答下列问题:
(1)基态Co的价电子排布式为
(2)Na、K等金属在焰色试验中可以观察到焰色,Fe、Co等金属则观察不到焰色,请解释原因:
(3)关于如图所示的配合物,下列说法正确的是______(填标号)。
| A.中心原子Co的配体数为6 |
| B.分子式中所含元素电负性最大的是O |
| C.分子中第二周期元素中第一电离能最大的是N |
| D.分子中2个六元环都是平面正六边形 |
(4)Co可以形成多种配合物,一种配合物的化学式为
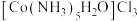 ,该配合物的配体为
,该配合物的配体为(5)
 具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于
具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于 的晶体密度为
的晶体密度为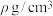 ),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的
),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的 可表示为
可表示为 (填表达式)。
(填表达式)。
您最近一年使用:0次
2024-05-11更新
|
70次组卷
|
2卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
名校
解题方法
10 . 血红素中含有 C、O、N、Fe 五种元素。回答下列问题:
(1)C、N、O、H四种元素中电负性最小的是__________ (填元素符合),写出基态Fe原子的核外电子排布式_________________ 。
(2)下图所示为血红蛋白和肌红蛋白的活性部分――血红素的结构式。血红素中 N 原子的杂化方式有____________ ,在右图的方框内用“→”标出 Fe2+的配位键。______

(3)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和 Fe2+的离子半径分别为 69 pm和78pm,则熔点 NiO________ FeO(填“<”或“>” );
(4)N与H形成的化合物肼(N2H4)可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) H=-1038.7 kJ ·mol 1
若该反应中有4mol N—H键断裂,则形成的 键有___________ mol。
(5)根据等电子原理,写出 CN—的电子式______ , 1 mol O22+中含有的π键数目为________ 。
(6)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为______ ,δ、α两种晶胞中铁原子的配位数之比为______ 。

(1)C、N、O、H四种元素中电负性最小的是
(2)下图所示为血红蛋白和肌红蛋白的活性部分――血红素的结构式。血红素中 N 原子的杂化方式有

(3)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和 Fe2+的离子半径分别为 69 pm和78pm,则熔点 NiO
(4)N与H形成的化合物肼(N2H4)可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) H=-1038.7 kJ ·mol 1
若该反应中有4mol N—H键断裂,则形成的 键有
(5)根据等电子原理,写出 CN—的电子式
(6)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为

您最近一年使用:0次



