1 . 水溶液锌电池(图1)的电极材料是研究热点之一、一种在晶体 中嵌入
中嵌入 的电极材料充放电过程的原理如图2所示。下列叙述中正确的是
的电极材料充放电过程的原理如图2所示。下列叙述中正确的是
 中嵌入
中嵌入 的电极材料充放电过程的原理如图2所示。下列叙述中正确的是
的电极材料充放电过程的原理如图2所示。下列叙述中正确的是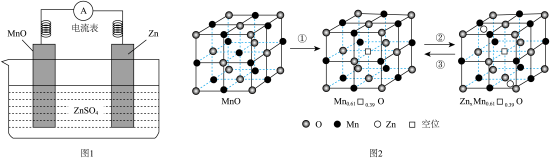
A.①为 活化过程,其中 活化过程,其中 的价态不变 的价态不变 |
| B.该材料在锌电池中作为负极材料 |
| C.②代表电池放电过程 |
D.③中 晶体转移的电子数为 晶体转移的电子数为 |
您最近一年使用:0次
2023-02-24更新
|
2388次组卷
|
8卷引用:江苏省徐州市沛县第二中学2023-2024学年高三下学期开学化学试题
江苏省徐州市沛县第二中学2023-2024学年高三下学期开学化学试题江苏省海安高级中学2022-2023学年高三下学期第五次阶段考试化学试题安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试理科综合化学试题(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(选择题11-13)(已下线)2023四省联考化学学科试卷分析(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试举一反三(选择题11-13)湖南省长沙市麓山国际实验学校2022-2023学年高三下学期3月月考化学试题山东省单县第二中学2023届高三下学期第1次 阶段性质量检测化学试题
名校
2 . 镁单质及其化合物用途广泛,某镁硼化合物的晶体结构单元如图所示。B原子占据独立一层且具有类似石墨的结构。正六棱柱底边边长为 ,高为
,高为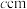 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 ,高为
,高为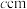 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
A.该镁硼化合物的化学式为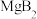 |
| B.如图所示晶体结构单元是该镁硼化合物的晶胞 |
| C.每个B原子周围最近且等距的B原子数为2 |
D.B原子的价层电子轨道表示式为 |
您最近一年使用:0次
2023-02-03更新
|
852次组卷
|
5卷引用:江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题
江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题江苏省无锡市匡园双语学校2022-2023学年高二下学期第一次月考化学试卷湖南省祁阳市第一中学2023届高三月考(六)化学试题(已下线)3.1 物质的聚集状态与晶体-同步学习必备知识(已下线)专题卷20 《物质结构与性质》选择题分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
名校
3 . CuCl可用作有机合成的催化剂。工业上用黄铜矿(主要成分是CuFeS2,还含有少量SiO2)制备CuCl的工艺流程如图1:
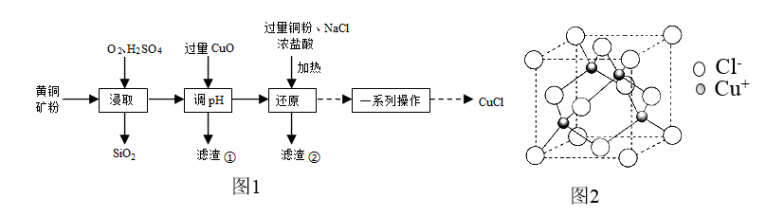
A.“浸取”时的离子方程式为CuFeS2+4O2=Cu2++Fe2++2SO |
| B.“滤渣①”的成分是Fe(OH)3 |
| C.“还原”时加入NaCl和浓盐酸主要是为了提供Cl-,跟铜元素形成可溶于水的物质 |
| D.CuCl的晶胞如图2,每个氯离子周围与之距离最近的氯离子数目是4 |
您最近一年使用:0次
2022-03-05更新
|
1685次组卷
|
15卷引用:江苏省六校2021-2022学年高三下学期期初联合调研考试化学试题
江苏省六校2021-2022学年高三下学期期初联合调研考试化学试题(已下线)黄金卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)黄金卷8-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)必刷卷05-2022年高考化学考前信息必刷卷(江苏专用)(已下线)押江苏卷第9题 化学工艺流程选择题 -备战2022年高考化学临考题号押题(江苏卷)江苏省南京市金陵中学2021-2022学年高三下学期3月学情调研化学试题江苏南京师范大学附属中学2022-2023学年高三一模适应性考试化学试题江苏省扬州中学2022-2023学年高二下学期期中考试化学试题江苏省南京市六校联合体2022-2023学年高二下学期5月期中考试化学试题江苏省盐城市东台中学2023-2024学年高三下学期3月月考化学试题江苏省苏州实验中学2023-2024学年高二下学期3月月考化学试题浙江省“南太湖”联盟2021-2022学年高二下学期第一次联考化学试题 (已下线)题型37 含铜化合物的性质及其之间的转化流程(已下线)专题09 物质的反应及转化湖南省长沙市第一中学2023-2024学年高三下学期2月自主检测化学试题
4 . 以粉煤灰浸取液(含Al3+、Li+、Mg2+、Cl-等)为原料制备电极材料LiFePO4的实验流程如图:

(1)“焙烧”过程中AlCl3最终转化为Al2O3和_____ (填化学式)。
(2)“浸出”后的滤液中主要含Li+、Mg2+、Cl-等。已知Ksp[Mg(OH)2]=5.5×10-12,欲使c(Mg2+)≤5.5×10-6mol•L-1,“除杂”需要调节溶液的pH不低于_____ 。
(3)离子筛法“富集”锂的原理如图1所示。在碱性条件下,离子筛吸附Li+容量较大,其可能原因为_____ 。

(4)已知Li2CO3的溶解度曲线如图2所示。“沉锂”反应1h,测得Li+沉淀率随温度升高而增加,其原因有_____ 。

(5)“合成”在高温下进行,其化学方程式为_____ 。
(6)LiFePO4的晶胞结构示意图如图3所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有_____ 个。


(1)“焙烧”过程中AlCl3最终转化为Al2O3和
(2)“浸出”后的滤液中主要含Li+、Mg2+、Cl-等。已知Ksp[Mg(OH)2]=5.5×10-12,欲使c(Mg2+)≤5.5×10-6mol•L-1,“除杂”需要调节溶液的pH不低于
(3)离子筛法“富集”锂的原理如图1所示。在碱性条件下,离子筛吸附Li+容量较大,其可能原因为

(4)已知Li2CO3的溶解度曲线如图2所示。“沉锂”反应1h,测得Li+沉淀率随温度升高而增加,其原因有

(5)“合成”在高温下进行,其化学方程式为
(6)LiFePO4的晶胞结构示意图如图3所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有

您最近一年使用:0次
2023-03-24更新
|
894次组卷
|
3卷引用:江苏省扬州中学2023-2024学年高三上学期开学考试化学试题
江苏省扬州中学2023-2024学年高三上学期开学考试化学试题江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题 (已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(结构与性质)
名校
解题方法
5 . 金属铼(Re)广泛应用于国防、石油化工以及电子制造等领域,铼可通过还原高铼酸铵(NH4ReO4)制备。以钼精矿(主要成分为钼的硫化物和少量铼的硫化物)制取高铼酸铵的流程如下图所示。

(1)为了提高“焙烧”过程的效率,可以采取的措施为_____ (回答任意两点)。“焙烧”过程加入生石灰,有效解决了SO2的危害,则ReS2转化为Ca(ReO4)2的方程式为_____ 。
(2)“萃取”机理为:R3N+H++ReO =R3N·HReO4,则“反萃取”所用试剂X为
=R3N·HReO4,则“反萃取”所用试剂X为_____ 。
(3)如图表示萃取液流速与铼吸附率关系,萃取剂流速宜选用的范围是6~8BV/h,选择此范围的原因是_____ 。

(4)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是_____ 。
(5)经过上述反应后制备的铼粉中含有少量碳粉和铁粉(其熔沸点见表),在3500℃下,利用氢气提纯可得到纯度达99.995%的铼粉,请分析原因_____ 。

(6)三氧化铼晶胞如下图所示(小黑点代表铼或氧原子),铼原子填在了氧原子围成的_____ (填“四面体”“立方体”或“八面体”)空隙中。


(1)为了提高“焙烧”过程的效率,可以采取的措施为
(2)“萃取”机理为:R3N+H++ReO
 =R3N·HReO4,则“反萃取”所用试剂X为
=R3N·HReO4,则“反萃取”所用试剂X为(3)如图表示萃取液流速与铼吸附率关系,萃取剂流速宜选用的范围是6~8BV/h,选择此范围的原因是

(4)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是
(5)经过上述反应后制备的铼粉中含有少量碳粉和铁粉(其熔沸点见表),在3500℃下,利用氢气提纯可得到纯度达99.995%的铼粉,请分析原因

| 物质 | 熔点(℃) | 沸点(℃) |
| Re | 3180 | 5900 |
| C | 3652 | 4827 |
| Fe | 1535 | 2750 |
(6)三氧化铼晶胞如下图所示(小黑点代表铼或氧原子),铼原子填在了氧原子围成的

您最近一年使用:0次
2023-09-16更新
|
657次组卷
|
5卷引用:江苏省扬州中学2023-2024学年高三下学期阶段练习化学试题
名校
解题方法
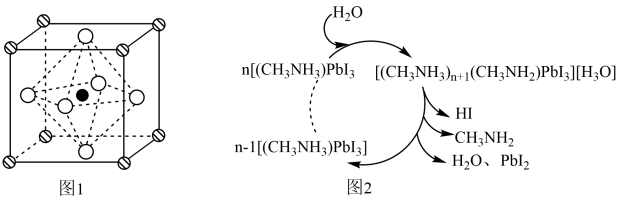
6 . (CH3NH3)PbI3是钙钛矿太阳能电池的重要吸光材料,其晶胞结构如图1所示,Walsh提出H2O降解(CH3NH3)PbI3的机理如图2所示。
下列说法不正确 的是

下列说法
| A.H3O+的键角小于H2O的键角 | B.1个(CH3NH3)PbI3晶胞含有3个I- |
| C.机理中的反应均为非氧化还原反应 | D.H2O可与CH3NH 反应生成H3O+和CH3NH2 反应生成H3O+和CH3NH2 |
您最近一年使用:0次
2022-06-08更新
|
973次组卷
|
8卷引用:江苏省南通市通州湾中学2022-2023学年高三上学期暑期自主学习质量检测化学试题
江苏省南通市通州湾中学2022-2023学年高三上学期暑期自主学习质量检测化学试题江苏省泰州市2021-2022学年高三下学期第四次调研测试化学试题(已下线)考点48 晶体结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)易错点15 化学键-备战2023年高考化学考试易错题(已下线)易错点04 氧化还原反应-备战2023年高考化学考试易错题浙江省宁波市北仑中学2022-2023学年高二下学期期中考试化学试题河北省衡水中学2023届高三下学期第五次综合素养测评化学试题江苏省淮安市二校楚州中学新马中学2023-2024学年高三上学期10月化学试卷
名校
解题方法
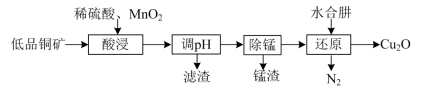
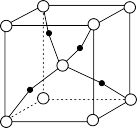
7 . 用低品铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如下:
下列说法正确的是


下列说法正确的是
A.“酸浸”过程中CuS发生反应的离子方程式为: S2-+MnO2+4H+ Mn2++S+2H2O Mn2++S+2H2O |
| B.“酸浸”所得溶液中的阳离子主要有H+、Mn2+、Cu2+和Fe2+ |
| C.1个Cu2O晶胞(如图)中含4个氧原子 |
| D.水合肼浓度过大,Cu2O产率下降,可能的原因是Cu2O进一步被还原成单质铜 |
您最近一年使用:0次
2022-05-31更新
|
545次组卷
|
3卷引用:江苏省南通市通州湾中学2022-2023学年高三上学期暑期自主学习质量检测化学试题
名校
8 . 由含硒废料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)制取硒的流程如下:
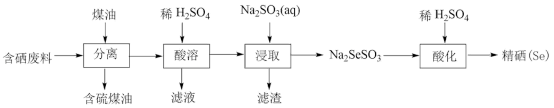
下列有关说法正确的是

下列有关说法正确的是

| A.“分离”的方法是蒸馏 |
B.“滤液”中主要存在的阴离子有:SO 、SiO 、SiO |
C.“酸化”时发生的离子反应方程式为SeSO +H2O=Se↓+SO2↑+2OH- +H2O=Se↓+SO2↑+2OH- |
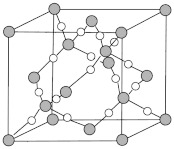
| D.SiO2晶胞如图所示,1个SiO2晶胞中有16个O原子 |
您最近一年使用:0次
2022-02-18更新
|
910次组卷
|
13卷引用:江苏省南通市八校2022-2023学年高三上学期期初联考化学试题
江苏省南通市八校2022-2023学年高三上学期期初联考化学试题江苏省南通市2022届高三第一次调研测试化学试题(已下线)黄金卷6-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省常熟市2022-2023学年高三上学期阶段性抽测一化学试题江苏省盐城市三校(盐城一中、亭湖高中、大丰中学)2022-2023学年高二下学期期中联考化学试题江苏省盐城市滨海县部分学校联考2022-2023学年高二下学期第二次月考化学试题江苏省前黄高级中学2023-2024学年高三上学期第一次阶段检测化学试题江苏省苏南八校2023-2024学年高二上学期12月联考化学(创新班)试卷湖北省武汉市部分重点中学2021-2022学年高二下学期3月联考化学试题河北省衡水市第十四中学2022-2023学年高二下学期第一次选择性考试化学试题吉林省长春市新解放学校2022-2023学年高二下学期4月月考化学试题河北省保定市河北安国中学等4校2022-2023学年高三上学期11月期中化学试题吉林省通化市梅河口市第五中学2023-2024学年高三上学期11月期中化学试题
名校
解题方法
9 . 天然硅酸盐组成复杂,其阴离子基本结构单元大多是SiO4四面体。在 中,
中, 表示硅氧四面体,则该结构式的通式为
表示硅氧四面体,则该结构式的通式为
 中,
中, 表示硅氧四面体,则该结构式的通式为
表示硅氧四面体,则该结构式的通式为A.(Si2O5) | B.(SiO3) | C.(Si6O17) | D.(Si8O24) |
您最近一年使用:0次
2020-09-07更新
|
1567次组卷
|
4卷引用:江苏省扬州中学2020-2021学年高一上学期开学考暨奥赛选拔化学试题
江苏省扬州中学2020-2021学年高一上学期开学考暨奥赛选拔化学试题(已下线)小题必刷17 碳、硅与无机非金属材料——2021年高考化学一轮复习小题必刷(通用版)(已下线)【浙江新东方】32020年浙江省高中学生化学竞赛试题
名校
10 . 葡萄糖的银镜反应实验如下:
步骤1:向试管中加入1mL 2% AgNO3溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1mL 10%葡萄糖溶液,振荡,在60~70℃水浴中加热,观察到试管内壁形成了光亮银镜。
下列说法不正确 的是
步骤1:向试管中加入1mL 2% AgNO3溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1mL 10%葡萄糖溶液,振荡,在60~70℃水浴中加热,观察到试管内壁形成了光亮银镜。
下列说法
| A.步骤1中观察到的白色沉淀为AgOH |
| B.步骤2中沉淀溶解是因为生成了银氨配合物 |
| C.步骤3中产生银镜说明葡萄糖具有还原性 |
D.右图所示银的晶胞中有14个银原子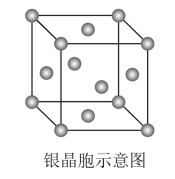 |
您最近一年使用:0次
2021-01-25更新
|
1024次组卷
|
7卷引用:江苏省苏州市苏州高新区第一中学2020-2021学年高二下学期期初考试化学试题



