18. 运用化学反应原理对研究部分单质及其化合物的反应有重要意义。
(1)氨是氮循环过程中的重要物质,是氮肥工业的重要原料。氨的合成是目前普遍使用的人工固氮方法:N
2(g)+3H
2(g)

2NH
3(g)。请回答:
①已知H—H键键能为436kJ·mol
-1,N≡N键键能为945 kJ·mol
-1,N—H键键能为391 kJ·mol
-1。由键能计算消耗1 mol N
2时的ΔH=
_____。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡
____(填“向左”、“向右”或“不”)移动。
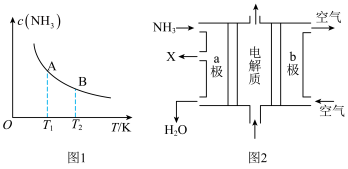
②如图中,当温度由T
1变化到T
2时,K
A___(填“>”、“<”或“=”)K
B。
③废氨水可以转化成氨,氨再设计成碱性燃料电池。如图是该燃料电池示意图,产生的X气体可直接排放到大气中。a电极作
____(填“正”、“负”、“阴”或“阳”)极,其电极反应式为
____。
(2)某温度下在容积固定的密闭容器中,下列反应达到平衡:CO(g)+H
2O(g)

CO
2(g)+H
2(g)
| 起始n(CO)∶n(H2O) | CO转化率 | H2O转化率 |
| 1∶1 | 0.5 | 0.5 |
| 1∶2 | 0.67 | 0.33 |
| 1∶3 | 0.75 | 0.25 |
①该反应的平衡常数为
_____。该温度下,向容器中充入1 mol CO、3 mol H
2O、2 mol CO
2、1.5 mol H
2,则起始时该反应速率v(正)
______(填“>”、“<”或“=”)v(逆)。
②结合表中数据,判断下列说法正确的是
_______(填字母)。
A.增加H
2O(g)的量,CO的转化率升高而H
2O(g)的转化率降低
B.若CO与H
2O(g)的转化率相同,二者的初始投入量一定相同
C.CO和H
2O(g)初始物质的量之比等于二者转化率之比
D.当CO与H
2O(g)物质的量之比为1∶4时,CO的转化率为0.85
③该温度下,向容器中充入2 mol CO、2 mol H
2O,达平衡时放出a kJ热量,则该反应的ΔH=
_____。