18. 硫代硫酸钠晶体(Na
2S
2O
3·5H
2O)俗名“大苏打”。已知它易溶于水,难溶于乙醇,在中性或碱性环境中稳定,受热、遇酸易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
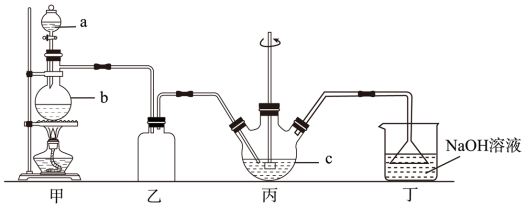
(1)装置甲中,a仪器的名称是
_______;a中盛有浓硫酸,b中盛有亚硫酸钠,实验中要控制SO
2生成速率,可以采取的措施有
_______(写出一条即可)
(2)装置乙的作用是
_______(3)装置丙中,将Na
2S和Na
2CO
3以2:1的物质的量之比配成溶液再通入SO
2,便可制得Na
2S
2O
3和CO
2。写出反应的化学方程式:
_______(4)本实验所用的Na
2CO
3中含有少量NaOH,检验含有NaOH的实验方案为
_______。
[实验中供选择的试剂及仪器:CaCl
2溶液、Ca(OH)
2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管。提示:室温时CaCO
3饱和溶液的PH=9.5]
(5)反应结束后过滤丙中的混合物,滤液经蒸发、结晶、过滤、洗涤、干燥等得到产品,生成的硫代硫酸钠粗品可用
_______洗涤。为了测定粗产品中Na
2S
2O
3·5H
2O的含量,采用在酸性条件下用KMnO
4标准液滴定的方法(假设粗产品中的杂质与酸性KMnO
4溶液不反应)。称取1.50g粗产品溶于水,用0.20 mol/L
的KMnO
4溶液(加适量稀硫酸酸化)滴定,当溶液中S
2O

被氧化为SO

时消耗高锰酸钾溶液的体积为40.00mL。则产品中Na
2S
2O
3·5H
2O的质量分数为
_______(保留小数点后一位)