江苏省苏州市2024届高三下学期三模考试化学试卷
江苏
高三
三模
2024-05-27
662次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、物质结构与性质、常见无机物及其应用、化学反应原理、有机化学基础、化学实验基础
江苏省苏州市2024届高三下学期三模考试化学试卷
江苏
高三
三模
2024-05-27
662次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、物质结构与性质、常见无机物及其应用、化学反应原理、有机化学基础、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 材料是人类赖以生存和发展的物质基础,下列材料主要成分属于有机物的是
| A.石墨烯 | B.不锈钢 | C.石英光导纤维 | D.聚酯纤维 |
您最近一年使用:0次
2023-06-21更新
|
5052次组卷
|
11卷引用:2023年高考浙江卷化学真题(6月)
2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题1-5)(已下线)考点01 物质的分类和转化(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第7讲 碳、硅及无机非金属材料(已下线)专题01 化学与STSE 物质的组成、性质和用途-2023年高考化学真题题源解密(全国通用)5.3.1有机合成设计 课前宁夏银川市第二中学2023-2024学年高三上学期统练二化学试题河南省九师联盟2023-2024学年高三上学期12月月考理综试题江西省宜春市百树学校2023-2024学年高三上学期暑期阶段测试化学试卷江苏省苏州市2024届高三下学期三模考试化学试卷(已下线)第01讲 物质的分类及转化(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
2. 由 与
与 为原料可生产尿素
为原料可生产尿素 。下列说法正确的是
。下列说法正确的是
 与
与 为原料可生产尿素
为原料可生产尿素 。下列说法正确的是
。下列说法正确的是A.中子数为8的氮原子: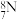 | B.元素的电负性: |
C. 的电子式为: 的电子式为: | D. 的空间填充模型为: 的空间填充模型为: |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 下列制备、干燥、收集NH3,并进行喷泉实验的原理与装置能达到实验目的的是

| A.用装置甲制备NH3 | B.用装置乙干燥NH3 |
| C.用装置丙收集NH3 | D.用装置丁进行喷泉实验 |
您最近一年使用:0次
2022-02-18更新
|
966次组卷
|
3卷引用:江苏省南通市2022届高三第一次调研测试化学试题
4.  、
、 、
、 位于周期表第三周期。下列说法正确的是
位于周期表第三周期。下列说法正确的是
 、
、 、
、 位于周期表第三周期。下列说法正确的是
位于周期表第三周期。下列说法正确的是A.离子半径: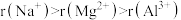 |
B.碱性: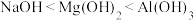 |
C.第一电离能: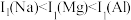 |
D. 、 、 、 、 晶体类型相同 晶体类型相同 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 硫单质及其化合物应用广泛。硫的一种单质 难溶于水,易溶于
难溶于水,易溶于 溶液。
溶液。 可用于制作锂硫电池,放电总反应为
可用于制作锂硫电池,放电总反应为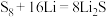 。硫的重要化合物还包括
。硫的重要化合物还包括 、甲硫醇
、甲硫醇 、
、 、多硫化钠
、多硫化钠 、过二硫酸钠
、过二硫酸钠 等。
等。 下,锂硫剂
下,锂硫剂 与
与 共同作用可用于脱除
共同作用可用于脱除 生成
生成 和
和 ;
; 具有强氧化性,在酸性条件下能将
具有强氧化性,在酸性条件下能将 氧化为
氧化为 。下列说法正确的是
。下列说法正确的是
 难溶于水,易溶于
难溶于水,易溶于 溶液。
溶液。 可用于制作锂硫电池,放电总反应为
可用于制作锂硫电池,放电总反应为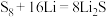 。硫的重要化合物还包括
。硫的重要化合物还包括 、甲硫醇
、甲硫醇 、
、 、多硫化钠
、多硫化钠 、过二硫酸钠
、过二硫酸钠 等。
等。 下,锂硫剂
下,锂硫剂 与
与 共同作用可用于脱除
共同作用可用于脱除 生成
生成 和
和 ;
; 具有强氧化性,在酸性条件下能将
具有强氧化性,在酸性条件下能将 氧化为
氧化为 。下列说法正确的是
。下列说法正确的是A. 空间构型为直线形 空间构型为直线形 | B. 、 、 中 中 原子均采用 原子均采用 杂化 杂化 |
C. 中的阴、阳离子个数比为 中的阴、阳离子个数比为 | D. 中 中 的化合价为 的化合价为 |
您最近一年使用:0次
单选题
|
适中(0.65)
6. 硫单质及其化合物应用广泛。硫的一种单质 难溶于水,易溶于
难溶于水,易溶于 溶液。
溶液。 可用于制作锂硫电池,放电总反应为
可用于制作锂硫电池,放电总反应为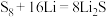 。硫的重要化合物还包括
。硫的重要化合物还包括 、甲硫醇
、甲硫醇 、
、 、多硫化钠
、多硫化钠 、过二硫酸钠
、过二硫酸钠 等。
等。 下,锂硫剂
下,锂硫剂 与
与 共同作用可用于脱除
共同作用可用于脱除 生成
生成 和
和 ;
; 具有强氧化性,在酸性条件下能将
具有强氧化性,在酸性条件下能将 氧化为
氧化为 。下列化学反应表示正确的是
。下列化学反应表示正确的是
 难溶于水,易溶于
难溶于水,易溶于 溶液。
溶液。 可用于制作锂硫电池,放电总反应为
可用于制作锂硫电池,放电总反应为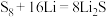 。硫的重要化合物还包括
。硫的重要化合物还包括 、甲硫醇
、甲硫醇 、
、 、多硫化钠
、多硫化钠 、过二硫酸钠
、过二硫酸钠 等。
等。 下,锂硫剂
下,锂硫剂 与
与 共同作用可用于脱除
共同作用可用于脱除 生成
生成 和
和 ;
; 具有强氧化性,在酸性条件下能将
具有强氧化性,在酸性条件下能将 氧化为
氧化为 。下列化学反应表示正确的是
。下列化学反应表示正确的是A. 水解: 水解: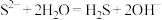 |
B.锂硫电池放电时的正极反应: |
C.脱硫剂除烟气中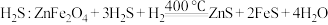 |
D. 氧化 氧化 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
7. 硫单质及其化合物应用广泛。硫的一种单质 难溶于水,易溶于
难溶于水,易溶于 溶液。
溶液。 可用于制作锂硫电池,放电总反应为
可用于制作锂硫电池,放电总反应为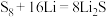 。硫的重要化合物还包括
。硫的重要化合物还包括 、甲硫醇
、甲硫醇 、
、 、多硫化钠
、多硫化钠 、过二硫酸钠
、过二硫酸钠 等。
等。 下,锂硫剂
下,锂硫剂 与
与 共同作用可用于脱除
共同作用可用于脱除 生成
生成 和
和 ;
; 具有强氧化性,在酸性条件下能将
具有强氧化性,在酸性条件下能将 氧化为
氧化为 。下列物质结构与性质或性质与用途具有对应关系的是
。下列物质结构与性质或性质与用途具有对应关系的是
 难溶于水,易溶于
难溶于水,易溶于 溶液。
溶液。 可用于制作锂硫电池,放电总反应为
可用于制作锂硫电池,放电总反应为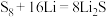 。硫的重要化合物还包括
。硫的重要化合物还包括 、甲硫醇
、甲硫醇 、
、 、多硫化钠
、多硫化钠 、过二硫酸钠
、过二硫酸钠 等。
等。 下,锂硫剂
下,锂硫剂 与
与 共同作用可用于脱除
共同作用可用于脱除 生成
生成 和
和 ;
; 具有强氧化性,在酸性条件下能将
具有强氧化性,在酸性条件下能将 氧化为
氧化为 。下列物质结构与性质或性质与用途具有对应关系的是
。下列物质结构与性质或性质与用途具有对应关系的是A. 为非极性分子,易溶于 为非极性分子,易溶于 溶液 溶液 |
B. 单质具有氧化性,常用于实验室处理汞 单质具有氧化性,常用于实验室处理汞 |
C.甲硫醇 具有还原性,常被掺入家用煤气以检验是否泄漏 具有还原性,常被掺入家用煤气以检验是否泄漏 |
D. 分子间能形成氢键,浓硫酸具有很强的吸水性 分子间能形成氢键,浓硫酸具有很强的吸水性 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
8. 在给定条件下,下列物质转化或方程式正确的是
A.工业制漂白粉: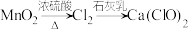 |
B.工业制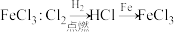 |
C.电解饱和食盐水: |
D. 碱性溶液与 碱性溶液与 反应: 反应: |
您最近一年使用:0次
7日内更新
|
310次组卷
|
3卷引用:江苏省苏州市2024届高三下学期三模考试化学试卷
江苏省苏州市2024届高三下学期三模考试化学试卷(已下线)第一章 物质及其变化(测试)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)山东省烟台市龙口第一中学东校2023-2024学年高二下学期6月月考化学试题
单选题
|
适中(0.65)
解题方法
9. 化合物Z是合成抗肿瘤药物异甘草素的重要中间体,其合成路线如下:

| A.X分子中的所有原子一定共平面 |
| B.Y能发生加成、氧化和消去反应 |
| C.Z与足量的氢气加成后的产物分子中含有3个手性碳原子 |
| D.Y转化为Z的过程中,要控制氯甲基甲醚的用量 |
您最近一年使用:0次
2023-12-05更新
|
281次组卷
|
2卷引用:江苏省镇江市2023-2024学年高三上学期期中考试化学试题
单选题
|
适中(0.65)
10. 活性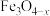 催化反应
催化反应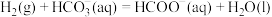 的部分机理如图所示。下列说法正确的是
的部分机理如图所示。下列说法正确的是
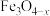 催化反应
催化反应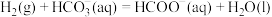 的部分机理如图所示。下列说法正确的是
的部分机理如图所示。下列说法正确的是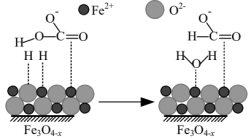
A.该反应的 |
B.该反应平衡常数 |
| C.反应前后碳原子杂化方式没有发生变化 |
D.吸附在 表面的 表面的 与 与 中的羟基结合生成水 中的羟基结合生成水 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 取少量 水溶液,进行水溶液性质探究。下列实验方案不能达到实验目的的是
水溶液,进行水溶液性质探究。下列实验方案不能达到实验目的的是
 水溶液,进行水溶液性质探究。下列实验方案不能达到实验目的的是
水溶液,进行水溶液性质探究。下列实验方案不能达到实验目的的是| 选项 | 探究性质 | 实验方案 |
| A | 氧化性 | 滴加几滴盐酸酸化的 溶液,再滴加 溶液,再滴加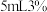 的 的 溶液,振荡,观察实验现象 溶液,振荡,观察实验现象 |
| B | 还原性 | 滴加几滴酸性 溶液,振荡,观察溶液颜色的变化 溶液,振荡,观察溶液颜色的变化 |
| C | 酸性 | 滴加紫色石蕊溶液,观察溶液颜色变化 |
| D | 漂白性 | 滴加几滴品红溶液,振荡,加热试管,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化硫的化学性质
您最近一年使用:0次
单选题
|
较难(0.4)
12. 以磷石膏(主要成分 ,杂质
,杂质 、
、 等)和氨水为原料可实现
等)和氨水为原料可实现 矿物封存同时制备轻质
矿物封存同时制备轻质 ,转化部分流程如图。
,转化部分流程如图。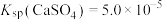 ,
,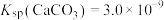 ,
,
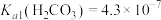 ,
,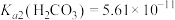 。
。
下列说法正确的是
 ,杂质
,杂质 、
、 等)和氨水为原料可实现
等)和氨水为原料可实现 矿物封存同时制备轻质
矿物封存同时制备轻质 ,转化部分流程如图。
,转化部分流程如图。
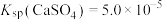 ,
,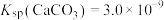 ,
,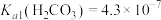 ,
,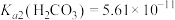 。
。下列说法正确的是
A.氨水中存在: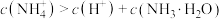 |
B.“转化”步骤,通入 后清液中始终存在 后清液中始终存在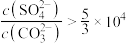 |
C.“转化”步骤,若通入 至溶液 至溶液 为6.5,此时溶液中 为6.5,此时溶液中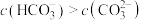 |
D.“滤液”中存在: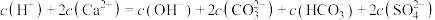 |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
13.  催化加氢制甲醇主要反应:
催化加氢制甲醇主要反应:
反应Ⅰ.
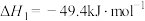
反应Ⅱ.

压强分别为 、
、 时,将
时,将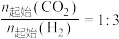 的混合气体置于密闭容器中反应,不同温度下体系中
的混合气体置于密闭容器中反应,不同温度下体系中 或
或 的平衡选择性如图所示。(
的平衡选择性如图所示。( (或
(或 )的平衡选择性
)的平衡选择性 )
)
 催化加氢制甲醇主要反应:
催化加氢制甲醇主要反应:反应Ⅰ.

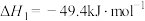
反应Ⅱ.


压强分别为
 、
、 时,将
时,将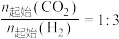 的混合气体置于密闭容器中反应,不同温度下体系中
的混合气体置于密闭容器中反应,不同温度下体系中 或
或 的平衡选择性如图所示。(
的平衡选择性如图所示。( (或
(或 )的平衡选择性
)的平衡选择性 )
)
A.曲线①、②表示的是 平衡选择性 平衡选择性 |
B.曲线①、②表示的压强: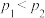 |
C.随温度升高, 的平衡转化率受压强影响减小 的平衡转化率受压强影响减小 |
D.相同温度下,压强分别为 、 、 时,反应Ⅰ的平衡常数 时,反应Ⅰ的平衡常数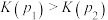 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-原理综合题
|
困难(0.15)
14.  、
、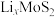 、
、 等均可作锂离子电池的电极材料。
等均可作锂离子电池的电极材料。
(1) 电极。将
电极。将 、
、 与
与 溶液发生共沉淀反应,所得沉淀经
溶液发生共沉淀反应,所得沉淀经 真空干燥、高温成型,制得电池的正极材料
真空干燥、高温成型,制得电池的正极材料 。
。
①投料时,先将 与
与___________ 直接混合,再向其中加入另一种溶液。
②共沉淀的化学方程式为___________ 。
③高温成型前,常向 中加入少量活性炭黑,其作用是
中加入少量活性炭黑,其作用是___________ 。
(2)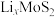 电极。层状
电极。层状 晶体与石墨晶体结构类似,将
晶体与石墨晶体结构类似,将 嵌入层状
嵌入层状 充电后得到的
充电后得到的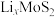 可作电池负极。
可作电池负极。
①该负极放电时的电极反应式为___________ 。
②结合原子结构分析, 能嵌入
能嵌入 层间可能的原因是
层间可能的原因是___________ 。
(3) 电极。从废锂电池正极材料
电极。从废锂电池正极材料 回收
回收 、
、 等金属路线如下:
等金属路线如下:___________ 。
② 空气中加热时,固体残留率随温度的变化如图所示。已知
空气中加热时,固体残留率随温度的变化如图所示。已知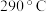 以上,
以上, 已完全脱水,在
已完全脱水,在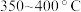 范围内,剩余固体成分为
范围内,剩余固体成分为___________ 。(写出计算过程)。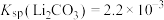 ,“沉锂”时使用饱和
,“沉锂”时使用饱和 的目的是
的目的是___________ 。
 、
、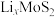 、
、 等均可作锂离子电池的电极材料。
等均可作锂离子电池的电极材料。(1)
 电极。将
电极。将 、
、 与
与 溶液发生共沉淀反应,所得沉淀经
溶液发生共沉淀反应,所得沉淀经 真空干燥、高温成型,制得电池的正极材料
真空干燥、高温成型,制得电池的正极材料 。
。①投料时,先将
 与
与②共沉淀的化学方程式为
③高温成型前,常向
 中加入少量活性炭黑,其作用是
中加入少量活性炭黑,其作用是(2)
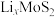 电极。层状
电极。层状 晶体与石墨晶体结构类似,将
晶体与石墨晶体结构类似,将 嵌入层状
嵌入层状 充电后得到的
充电后得到的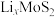 可作电池负极。
可作电池负极。①该负极放电时的电极反应式为
②结合原子结构分析,
 能嵌入
能嵌入 层间可能的原因是
层间可能的原因是(3)
 电极。从废锂电池正极材料
电极。从废锂电池正极材料 回收
回收 、
、 等金属路线如下:
等金属路线如下:
②
 空气中加热时,固体残留率随温度的变化如图所示。已知
空气中加热时,固体残留率随温度的变化如图所示。已知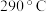 以上,
以上, 已完全脱水,在
已完全脱水,在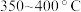 范围内,剩余固体成分为
范围内,剩余固体成分为
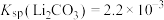 ,“沉锂”时使用饱和
,“沉锂”时使用饱和 的目的是
的目的是
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
15. 一种合成抗病毒生物活性类化合物 的路线部分如下:
的路线部分如下: 的化学式为
的化学式为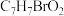 ,写出其结构简式:
,写出其结构简式:___________ 。 过程中
过程中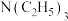 的作用是
的作用是___________ 。
(2) 是一种不稳定的中间体,
是一种不稳定的中间体, 的反应类型是
的反应类型是___________ 。
(3)物质 呈酸性的原因是
呈酸性的原因是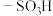 (结构为
(结构为 )中羟基的氧氢键断裂,且极性越强,氧氢键越易断裂。下列物质的酸性由强到弱的顺序是
)中羟基的氧氢键断裂,且极性越强,氧氢键越易断裂。下列物质的酸性由强到弱的顺序是___________ 。 的同分异构体
的同分异构体___________ 。
①能发生银镜反应且能使溴的 溶液褪色;②碱性条件水解后酸化的一种产物能与
溶液褪色;②碱性条件水解后酸化的一种产物能与 溶液发生显色反应;③核磁共振氢谱中存在4组峰。
溶液发生显色反应;③核磁共振氢谱中存在4组峰。
(5)写出以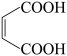 、
、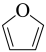 为原料制备
为原料制备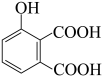 的合成路线流程图
的合成路线流程图___________ 。(无机试剂和有机溶剂任用,合成路线示例见本题题干)
 的路线部分如下:
的路线部分如下: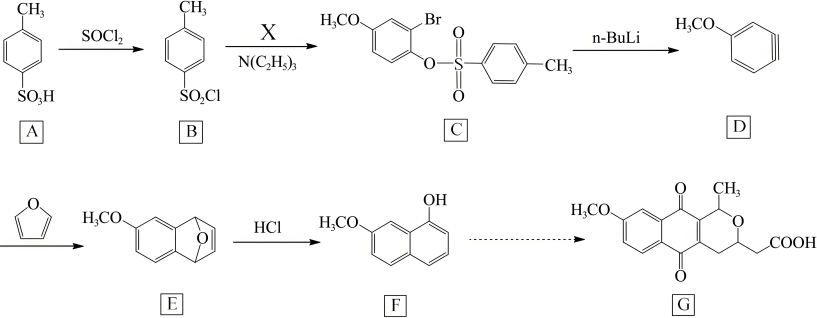
已知:
 的化学式为
的化学式为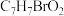 ,写出其结构简式:
,写出其结构简式: 过程中
过程中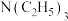 的作用是
的作用是(2)
 是一种不稳定的中间体,
是一种不稳定的中间体, 的反应类型是
的反应类型是(3)物质
 呈酸性的原因是
呈酸性的原因是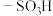 (结构为
(结构为 )中羟基的氧氢键断裂,且极性越强,氧氢键越易断裂。下列物质的酸性由强到弱的顺序是
)中羟基的氧氢键断裂,且极性越强,氧氢键越易断裂。下列物质的酸性由强到弱的顺序是①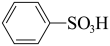 ②
② ③
③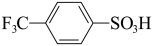
 的同分异构体
的同分异构体①能发生银镜反应且能使溴的
 溶液褪色;②碱性条件水解后酸化的一种产物能与
溶液褪色;②碱性条件水解后酸化的一种产物能与 溶液发生显色反应;③核磁共振氢谱中存在4组峰。
溶液发生显色反应;③核磁共振氢谱中存在4组峰。(5)写出以
 、
、 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
三、填空题 添加题型下试题
16. 乙二胺四乙酸铁钠(化学式 )是一种重要补铁剂,某小组以铁屑为原料制备
)是一种重要补铁剂,某小组以铁屑为原料制备 并测定其含量。
并测定其含量。
已知:① 是一种配合物,微溶于乙醇,
是一种配合物,微溶于乙醇, 时水中的溶解度为
时水中的溶解度为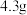 。
。
②乙二胺四乙酸( ,用
,用 表示)是一种弱酸。
表示)是一种弱酸。
Ⅰ.制备
实验室用铁屑制备 的主要流程如下:
的主要流程如下:___________
A.升高温度 B.加快搅拌速率 C.缩短浸取时间
(2)向酸浸所得滤液中通入足量 ,过程中浓度减少的离子有
,过程中浓度减少的离子有___________ (填离子符号)。
(3)“制备”步骤,向氧化所得的 溶液中加入一定量
溶液中加入一定量
 ,控制反应温度为
,控制反应温度为 ,加入
,加入 溶液调节
溶液调节 为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为
为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为 。
。
①从反应后的混合物中获得较高产率的 粗品的实验操作是,
粗品的实验操作是,___________ ,过滤,水洗,干燥。检验 是否洗净的试剂是
是否洗净的试剂是___________
②保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液 的变化如图1所示。
的变化如图1所示。 过低或过高产品产率均减小的主要原因是
过低或过高产品产率均减小的主要原因是___________ 。
样品中乙二胺四乙酸铁钠纯度可用 标准溶液滴定。原理是在
标准溶液滴定。原理是在 为
为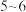 发生反应:
发生反应: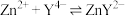 ,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。
,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。
(4)补充完整实验方案:准确称取 样品,溶于一定量的蒸馏水,加入掩蔽剂排除
样品,溶于一定量的蒸馏水,加入掩蔽剂排除 干扰,得到待测溶液
干扰,得到待测溶液 ,将溶液
,将溶液 完全转移到
完全转移到 容量瓶中定容;按规定操作分别将
容量瓶中定容;按规定操作分别将 标准溶液和待测溶液
标准溶液和待测溶液 装入如图2所示的滴定管中:
装入如图2所示的滴定管中:___________ 。
 )是一种重要补铁剂,某小组以铁屑为原料制备
)是一种重要补铁剂,某小组以铁屑为原料制备 并测定其含量。
并测定其含量。已知:①
 是一种配合物,微溶于乙醇,
是一种配合物,微溶于乙醇, 时水中的溶解度为
时水中的溶解度为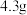 。
。②乙二胺四乙酸(
 ,用
,用 表示)是一种弱酸。
表示)是一种弱酸。Ⅰ.制备

实验室用铁屑制备
 的主要流程如下:
的主要流程如下:
A.升高温度 B.加快搅拌速率 C.缩短浸取时间
(2)向酸浸所得滤液中通入足量
 ,过程中浓度减少的离子有
,过程中浓度减少的离子有(3)“制备”步骤,向氧化所得的
 溶液中加入一定量
溶液中加入一定量
 ,控制反应温度为
,控制反应温度为 ,加入
,加入 溶液调节
溶液调节 为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为
为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为 。
。①从反应后的混合物中获得较高产率的
 粗品的实验操作是,
粗品的实验操作是, 是否洗净的试剂是
是否洗净的试剂是②保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液
 的变化如图1所示。
的变化如图1所示。 过低或过高产品产率均减小的主要原因是
过低或过高产品产率均减小的主要原因是
样品中乙二胺四乙酸铁钠纯度可用
 标准溶液滴定。原理是在
标准溶液滴定。原理是在 为
为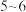 发生反应:
发生反应: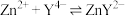 ,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。
,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。(4)补充完整实验方案:准确称取
 样品,溶于一定量的蒸馏水,加入掩蔽剂排除
样品,溶于一定量的蒸馏水,加入掩蔽剂排除 干扰,得到待测溶液
干扰,得到待测溶液 ,将溶液
,将溶液 完全转移到
完全转移到 容量瓶中定容;按规定操作分别将
容量瓶中定容;按规定操作分别将 标准溶液和待测溶液
标准溶液和待测溶液 装入如图2所示的滴定管中:
装入如图2所示的滴定管中:
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-原理综合题
|
较难(0.4)
17. 研究 的综合利用具有重要的意义。
的综合利用具有重要的意义。
Ⅰ. 催化重整制氢气
催化重整制氢气
一种 与
与 催化重整制取
催化重整制取 的过程如图1所示。在反应管中加入
的过程如图1所示。在反应管中加入 和催化剂,先通入
和催化剂,先通入 ,待步骤Ⅰ完成后,再将
,待步骤Ⅰ完成后,再将 以一定流速通入,并控制温度为
以一定流速通入,并控制温度为 ,进行步骤Ⅱ。
,进行步骤Ⅱ。___________ 。
(2)步骤Ⅱ中还存在少量副反应: ,测得出口处
,测得出口处 和
和 的流量随时间变化如图2所示。
的流量随时间变化如图2所示。 时出口处气体流量
时出口处气体流量 略高于
略高于 的原因是
的原因是___________ 。
②反应进行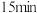 后,反应管中仍残留较多
后,反应管中仍残留较多 ,但
,但 流量迅速降低,
流量迅速降低, 流量升高,可能的原因是
流量升高,可能的原因是___________ 。
Ⅱ. 用于烟气脱硝
用于烟气脱硝
(3) 烟气脱硝相关反应如下:
烟气脱硝相关反应如下:
反应Ⅰ

反应Ⅱ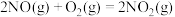

反应Ⅲ
①反应Ⅲ的
___________  。
。
②反应Ⅰ和反应II的平衡常数分别为 、
、 ,则相同温度下反应Ⅲ的
,则相同温度下反应Ⅲ的
___________ (用 、
、 表示)。
表示)。
(4)模拟烟气脱硝:一定条件下,将 、
、 和
和 按
按 匀速通过催化脱硝反应器,测得
匀速通过催化脱硝反应器,测得 去除率和
去除率和 转化率随反应温度的变化如图3所示。
转化率随反应温度的变化如图3所示。 时,
时, 的去除率随温度升高而升高,可能原因是
的去除率随温度升高而升高,可能原因是___________ 。
②当温度高于 时,
时, 的去除率随温度升高而降低,可能原因是
的去除率随温度升高而降低,可能原因是___________ 。
 的综合利用具有重要的意义。
的综合利用具有重要的意义。Ⅰ.
 催化重整制氢气
催化重整制氢气一种
 与
与 催化重整制取
催化重整制取 的过程如图1所示。在反应管中加入
的过程如图1所示。在反应管中加入 和催化剂,先通入
和催化剂,先通入 ,待步骤Ⅰ完成后,再将
,待步骤Ⅰ完成后,再将 以一定流速通入,并控制温度为
以一定流速通入,并控制温度为 ,进行步骤Ⅱ。
,进行步骤Ⅱ。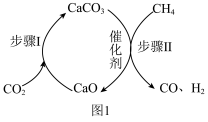
(2)步骤Ⅱ中还存在少量副反应:
 ,测得出口处
,测得出口处 和
和 的流量随时间变化如图2所示。
的流量随时间变化如图2所示。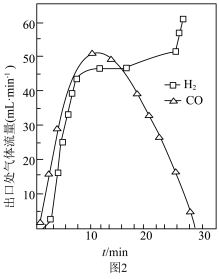
 时出口处气体流量
时出口处气体流量 略高于
略高于 的原因是
的原因是②反应进行
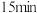 后,反应管中仍残留较多
后,反应管中仍残留较多 ,但
,但 流量迅速降低,
流量迅速降低, 流量升高,可能的原因是
流量升高,可能的原因是Ⅱ.
 用于烟气脱硝
用于烟气脱硝(3)
 烟气脱硝相关反应如下:
烟气脱硝相关反应如下:反应Ⅰ


反应Ⅱ
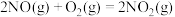

反应Ⅲ

①反应Ⅲ的

 。
。②反应Ⅰ和反应II的平衡常数分别为
 、
、 ,则相同温度下反应Ⅲ的
,则相同温度下反应Ⅲ的
 、
、 表示)。
表示)。(4)模拟烟气脱硝:一定条件下,将
 、
、 和
和 按
按 匀速通过催化脱硝反应器,测得
匀速通过催化脱硝反应器,测得 去除率和
去除率和 转化率随反应温度的变化如图3所示。
转化率随反应温度的变化如图3所示。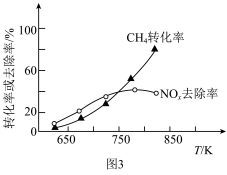
 时,
时, 的去除率随温度升高而升高,可能原因是
的去除率随温度升高而升高,可能原因是②当温度高于
 时,
时, 的去除率随温度升高而降低,可能原因是
的去除率随温度升高而降低,可能原因是
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、化学与STSE、物质结构与性质、常见无机物及其应用、化学反应原理、有机化学基础、化学实验基础
试卷题型(共 17题)
题型
数量
单选题
13
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 无机物与有机物 高分子材料 常见合金的组成 光导纤维与硅芯片 | |
| 2 | 0.65 | 共价化合物的结构及形成过程 电子式的书写与判断 元素、核素、同位素 元素性质与电负性的关系 | |
| 3 | 0.65 | 氨的喷泉实验 氨气的实验室制法 | |
| 4 | 0.65 | 元素金属性强弱的比较方法 微粒半径大小的比较方法 电离能变化规律 化学键类别与晶体类别间的关系 | |
| 5 | 0.65 | 利用杂化轨道理论判断分子的空间构型 利用杂化轨道理论判断化学键杂化类型 | |
| 6 | 0.65 | 离子方程式的正误判断 氧化还原反应方程式的书写与配平 水解的离子方程式书写 原电池电极反应式书写 | |
| 7 | 0.65 | 硫与金属单质的反应 浓硫酸的吸水性 相似相溶原理及应用 | |
| 8 | 0.65 | 物质的转化 离子方程式的正误判断 氯气的实验室制法 氯碱工业 | |
| 9 | 0.65 | 分子的手性 有机分子中原子共面的判断 多官能团有机物的结构与性质 | |
| 10 | 0.65 | 催化剂对化学反应速率的影响 化学平衡常数的概念及表达方式 反应进行方向判据的应用 羧酸 | |
| 11 | 0.65 | 二氧化硫的化学性质 | |
| 12 | 0.4 | 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 溶度积常数相关计算 | |
| 13 | 0.4 | 化学平衡图像分析 温度对化学平衡移动的影响 压强对化学平衡移动的影响 化学平衡常数的影响因素及应用 | |
| 二、解答题 | |||
| 14 | 0.15 | 原电池电极反应式书写 常见无机物的制备 物质制备的探究 | 原理综合题 |
| 15 | 0.65 | 根据要求书写同分异构体 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |
| 17 | 0.4 | 盖斯定律与热化学方程式 浓度对化学平衡移动的影响 温度对化学平衡移动的影响 化学平衡常数的影响因素及应用 | 原理综合题 |
| 三、填空题 | |||
| 16 | 0.65 | 氧化还原反应方程式的书写与配平 酸碱中和滴定原理的应用 物质分离、提纯综合应用 常见无机物的制备 | |



