北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
北京
高三
阶段练习
2024-10-09
101次
整体难度:
适中
考查范围:
物质结构与性质、常见无机物及其应用、化学反应原理、认识化学科学、有机化学基础、化学实验基础
北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
北京
高三
阶段练习
2024-10-09
101次
整体难度:
适中
考查范围:
物质结构与性质、常见无机物及其应用、化学反应原理、认识化学科学、有机化学基础、化学实验基础
一、单选题 添加题型下试题
单选题-单题
|
较易(0.85)
解题方法
1. 我国在可控核聚变研究上处于世界领先水平。核聚变原料的制备与核聚变的产物如图。 、
、 、
、 中仅
中仅 具有放射性。下列说法
具有放射性。下列说法不正确 的是

 、
、 、
、 中仅
中仅 具有放射性。下列说法
具有放射性。下列说法| A.元素的第一电离能:H>He>Li | B.可用质谱区分 、 、 和 和 |
C.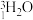 具有放射性 具有放射性 | D. 、 、 的化学性质基本相同 的化学性质基本相同 |
【知识点】 元素、核素、同位素解读 电离能的概念及变化规律解读
您最近一年使用:0次
单选题-单题
|
较易(0.85)
名校
2. 下列所用的物质中,利用了其还原性的是
A.用 溶液腐蚀覆铜板 溶液腐蚀覆铜板 | B.用Zn块防止钢铁船体腐蚀 |
C.用石灰乳脱除烟气中的 | D.用明矾[ ]处理污水 ]处理污水 |
您最近一年使用:0次
2024-10-28更新
|
82次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
单选题-单题
|
较易(0.85)
名校
解题方法
3. 下列化学用语或图示正确的是
A. 的电子式: 的电子式: |
B. 的VSEPR模型: 的VSEPR模型: |
C.基态Sc原子的价层电子排布式: |
D. 分子中 分子中 键的形成: 键的形成: |
您最近一年使用:0次
2024-10-28更新
|
178次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
单选题-单题
|
较易(0.85)
名校
解题方法
4. 下列化学用语与所给事实不相符 的是
A.炽热的铁水注入模具前,模具必须充分干燥,防止发生: |
B. 溶液吸收少量 溶液吸收少量 : :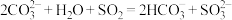 |
C. 去除废水中的 去除废水中的 : : |
D.电解熔融 的阴极反应: 的阴极反应: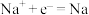 |
您最近一年使用:0次
2024-10-28更新
|
104次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
单选题-单题
|
适中(0.65)
名校
5. 氨是一种重要的化工产品和化工原料,下图为合成氨以及氨氧化制硝酸的流程示意图。不正确 的是

A.合成塔发生的反应中, 作氧化剂 作氧化剂 |
B.氧化炉中发生的反应为: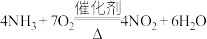 |
| C.向吸收塔中通入A气体,有利于提高硝酸的产率 |
| D.工业生产中为了盛装大量浓硝酸,可选择铝作为罐体材料 |
您最近一年使用:0次
2024-10-28更新
|
161次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
单选题-单题
|
适中(0.65)
名校
解题方法
6. 我国科学家研究成果“无细胞化学酶系统催化 合成淀粉”取得重要进展,其中一步核心反应如下图所示:
合成淀粉”取得重要进展,其中一步核心反应如下图所示:
 合成淀粉”取得重要进展,其中一步核心反应如下图所示:
合成淀粉”取得重要进展,其中一步核心反应如下图所示:
A.淀粉和纤维素分子式均为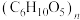 ,互为同分异构体 ,互为同分异构体 |
B.反应②中 与 与 的物质的量之比为 的物质的量之比为 |
C.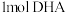 最多可与 最多可与 反应 反应 |
D. 和 和 均易溶于水,都可与 均易溶于水,都可与 分子形成氢键 分子形成氢键 |
【知识点】 酮 淀粉和纤维素组成与结构 氢键对物质性质的影响解读
您最近一年使用:0次
2024-10-28更新
|
120次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
7. 完成下列实验,所用仪器或操作合理的是
|
|
A.用 标准溶液滴定 标准溶液滴定 溶液 溶液 | B.验证相同温度下的 : :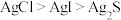 |
|
|
| C.铁件镀铜 | D.验证卤素单质的氧化性: |
| A.A | B.B | C.C | D.D |
【知识点】 沉淀转化解读 电镀解读 化学实验方案的设计与评价
您最近一年使用:0次
2024-10-28更新
|
162次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
二、多选题 添加题型下试题
多选题-2个答案
|
适中(0.65)
名校
8. 利用如图所示装置(夹持装置略)进行实验,b中现象可以证明a中产物生成的是
| a中反应 | b中检测试剂及现象 |
| |
| A | 浓 分解生成 分解生成 | 淀粉-KI溶液变蓝 | |
| B | Cu与浓 生成 生成 | 紫色石蕊变红 | |
| C | 浓 与 与 溶液生成 溶液生成 | 酚酞溶液变红 | |
| D |  和浓盐酸生成 和浓盐酸生成 |  溶液变浑浊 溶液变浑浊 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-11-01更新
|
111次组卷
|
3卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
三、单选题 添加题型下试题
单选题-单题
|
较易(0.85)
名校
9. 下列依据相关数据作出的推断中,不正确 的是
| A.依据金属与水或酸反应的难易程度,可推断元素金属性的强弱 |
B.依据所含化学键的键能,可推断 和 和 的熔点 的熔点 |
| C.依据是否存在氢键及氢键类型,可推断邻羟基苯甲醛和对羟基苯甲醛的熔点 |
| D.根据元素电负性的大小,可判断元素金属性和非金属性的强弱 |
您最近一年使用:0次
2024-10-28更新
|
72次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
单选题-单题
|
适中(0.65)
名校
解题方法
10. 全钒液流电池是一种新型绿色的二次电池。其工作原理如图所示。下列叙述不正确 的是

| A.放电时,电子由Y极流出,经负载到X极 |
B.放电时,每转移 电子,理论上有 电子,理论上有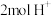 迁移至X极区 迁移至X极区 |
| C.充电过程中,Y极区溶液pH降低 |
| D.将电解液储存在储液罐中,可增大液流电池储能容量 |
【知识点】 原电池原理
您最近一年使用:0次
2024-10-06更新
|
195次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
四、多选题 添加题型下试题
多选题-2个答案
|
适中(0.65)
11. 铁的配合物离子(用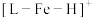 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
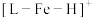 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示: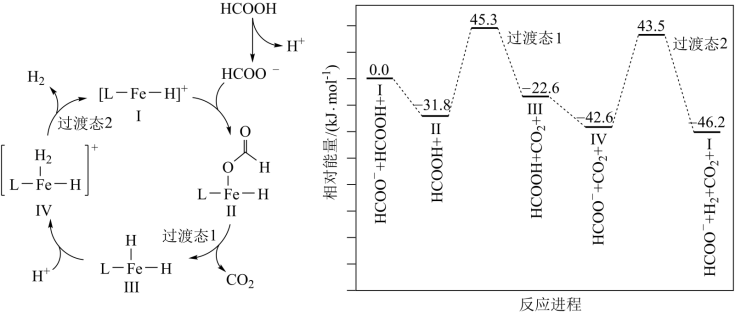
A.该过程的总反应为 |
| B.c(H+)过大或者过小,均导致反应速率降低 |
C.该催化循环中 元素的化合价发生了变化 元素的化合价发生了变化 |
| D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定 |
【知识点】 催化剂对化学反应速率的影响解读
您最近一年使用:0次
2021-06-09更新
|
9972次组卷
|
43卷引用:2021年新高考湖南化学高考真题
2021年新高考湖南化学高考真题(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省如皋中学2021-2022学年高三上学期期初测试化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)安徽省合肥工业大学附属中学2021-2022学年高三上学期第一次阶段考试化学试题辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)2021年湖南省高考化学试卷变式题11-19北京市第八中学2021-2022学年高二上学期期中考试化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题10 化学反应与能量-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)卷10 化学反应机理选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)秘籍08 反应历程探究与催化原理图象分析-备战2022年高考化学抢分秘籍(全国通用)(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)(已下线)2020年山东卷化学高考真题变式题11-15(已下线)专题09 化学反应速率、化学平衡-三年(2020-2022)高考真题分项汇编(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)江苏省海安高级中学2021-2022学年高二上学期阶段测试(二)化学试题(已下线)第15讲 化学反应的热效应 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题36 高考“明星”考点—催化剂-备战2023年高考化学一轮复习考点微专题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题湖南省衡阳师范学院祁东附属中学2021-2022学年高三上学期12月月考化学试题(已下线)专题12 化学反应机理(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)素养卷02 循环转化过渡态理论图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)考点21 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)热点题型训练 催化剂与反应历程(机理)(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)山东省泰安市部分学校2023-2024学年高二上学期期末调研化学试题北京大学附属中学2021-2022学年高二下学期期末考试化学试卷(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题山东省威海市乳山市银滩高级中学2023-2024学年高二上学期1月模块考试化学试题(已下线)专题11 化学反应中的热效应与反应机理-备战2025年高考化学真题题源解密(新高考通用)(已下线)专题13 化学反应速率与化学平衡-备战2025年高考化学真题题源解密(新高考通用)北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题北京市清华大学附属中学朝阳学校2024-2025学年高三上学期10月月考化学试题
五、单选题 添加题型下试题
单选题-单题
|
适中(0.65)
解题方法
12. 常温下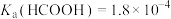 ,向
,向 溶液中缓慢滴入相同浓度的
溶液中缓慢滴入相同浓度的 溶液,混合溶液中某两种离子的浓度随加入
溶液,混合溶液中某两种离子的浓度随加入 溶液体积的变化关系如图所示。
溶液体积的变化关系如图所示。不正确 的是
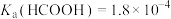 ,向
,向 溶液中缓慢滴入相同浓度的
溶液中缓慢滴入相同浓度的 溶液,混合溶液中某两种离子的浓度随加入
溶液,混合溶液中某两种离子的浓度随加入 溶液体积的变化关系如图所示。
溶液体积的变化关系如图所示。
A.①表示 随加入 随加入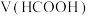 的变化关系 的变化关系 |
B.M点: |
C.N点: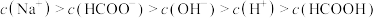 |
| D.水的电离程度:M<N |
【知识点】 影响水电离的因素解读 盐溶液中离子浓度大小的比较解读
您最近一年使用:0次
单选题-单题
|
适中(0.65)
名校
13. 下列实验中,均产生白色沉淀。不正确 的是

A. 能促进 能促进 、 、 水解 水解 |
B. 对 对 水解和 水解和 电离的影响方向一致 电离的影响方向一致 |
| C.前2个实验产生沉淀成分相同,后2个实验产生沉淀成分相同 |
| D.4个实验中,溶液滴入后,试管中溶液pH均降低 |
【知识点】 盐类双水解反应解读 浓度对盐类水解的影响解读
您最近一年使用:0次
2024-10-28更新
|
425次组卷
|
4卷引用:3.3.1 盐类的水解-同步学习必备知识
(已下线)3.3.1 盐类的水解-同步学习必备知识北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题(已下线)专题11盐类的水解——重难点北京市清华大学附属中学朝阳学校2024-2025学年高三上学期10月月考化学试题
单选题-单题
|
适中(0.65)
名校
解题方法
14. 某学生对 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:
下列叙述不正确 的是
 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:| 操作 | 现象 |
①取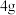 漂粉精固体,加入 漂粉精固体,加入 水 水 | 部分固体溶解,溶液略有颜色 |
| ②过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
③ | ⅰ.液面上方出现白雾 ⅱ.稍后,出现浑浊,溶液变为黄绿色 ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
④用酸化的 溶液检验③中白雾 溶液检验③中白雾 | 产生白色沉淀 |
| A.②中pH试纸颜色的变化说明漂粉精溶液具有碱性、漂白性 |
B.③中产生大量白色沉淀,推测白色沉淀主要为 |
C.③中溶液黄绿色褪去,反应为: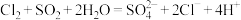 |
D.依据④中产生白色沉淀,说明③中液面上方产生的白雾中含有 |
您最近一年使用:0次
2024-10-28更新
|
138次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
六、解答题 添加题型下试题
解答题-结构与性质
|
适中(0.65)
名校
解题方法
15. 某钙钛矿 是一种新型半导体材料,用于制造太阳能电池。可用
是一种新型半导体材料,用于制造太阳能电池。可用 、
、 、
、 、
、 制备钙钛矿。
制备钙钛矿。
(1)Pb位于元素周期表第6周期ⅣA族,写出基态Pb原子价层电子轨道表示式___________ 。
(2) 分子的VSEPR模型名称是
分子的VSEPR模型名称是___________ , 的N—H键是由N的
的N—H键是由N的___________ 轨道与H的 轨道重叠形成
轨道重叠形成 键。
键。
(3)制备 的过程如下所示:
的过程如下所示:

①Ⅰ中, 的沸点高于
的沸点高于 的沸点,原因是
的沸点,原因是___________ 。
②Ⅱ中,由于 分子中的
分子中的___________ 具有孤电子对,容易与 反应生成盐
反应生成盐 。
。
(4)钙钛矿晶体的晶胞形状为立方体,边长为a nm,结构如图: 最近的
最近的 有
有___________ 个。
② 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体密度为
,则该晶体密度为___________  。(
。( )
)
(5)钙钛矿的稳定性受空气中 、
、 、紫外线等因素的影响。
、紫外线等因素的影响。
ⅰ.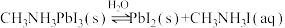
ⅱ.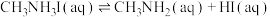
研究发现,一旦生成HI,钙钛矿的分解程度就会增大,请结合化学平衡移动原理解释:___________ ,我国研究人员利用聚乙二醇有效地解决了该问题。
 是一种新型半导体材料,用于制造太阳能电池。可用
是一种新型半导体材料,用于制造太阳能电池。可用 、
、 、
、 、
、 制备钙钛矿。
制备钙钛矿。(1)Pb位于元素周期表第6周期ⅣA族,写出基态Pb原子价层电子轨道表示式
(2)
 分子的VSEPR模型名称是
分子的VSEPR模型名称是 的N—H键是由N的
的N—H键是由N的 轨道重叠形成
轨道重叠形成 键。
键。(3)制备
 的过程如下所示:
的过程如下所示:
①Ⅰ中,
 的沸点高于
的沸点高于 的沸点,原因是
的沸点,原因是②Ⅱ中,由于
 分子中的
分子中的 反应生成盐
反应生成盐 。
。(4)钙钛矿晶体的晶胞形状为立方体,边长为a nm,结构如图:

 最近的
最近的 有
有②
 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体密度为
,则该晶体密度为 。(
。( )
)(5)钙钛矿的稳定性受空气中
 、
、 、紫外线等因素的影响。
、紫外线等因素的影响。ⅰ.
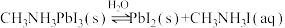
ⅱ.
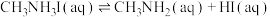
研究发现,一旦生成HI,钙钛矿的分解程度就会增大,请结合化学平衡移动原理解释:
您最近一年使用:0次
2024-10-28更新
|
65次组卷
|
2卷引用:北京市朝阳外国语学校2024-2025学年高三上学期第二次反馈(10月考)化学试题
解答题-原理综合题
|
适中(0.65)
16.  是一种重要的工业原料,可采用不同的方法制备
是一种重要的工业原料,可采用不同的方法制备 。
。
(1)方法一:早期以氯化铵和熟石灰制备 ,反应的化学方程式为
,反应的化学方程式为___________ 。
(2)方法二:以铁为主的催化剂在400~500℃和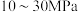 的条件下,由
的条件下,由 和
和 合成氨。
合成氨。
①该反应放热,但仍选择较高温度400~500℃。其原因是___________ 。
②对 和
和 的反应进行研究:在容积可变的密闭容器中,充入
的反应进行研究:在容积可变的密闭容器中,充入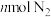 和
和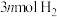 进行反应。在不同压强下(
进行反应。在不同压强下( 、
、 、
、 ),反应达到平衡时,测得
),反应达到平衡时,测得 的体积分数(
的体积分数( )随温度的变化如图所示。判断A点的容器容积和B点的容器容积的大小,并解释原因
)随温度的变化如图所示。判断A点的容器容积和B点的容器容积的大小,并解释原因___________ 。___________ 。
②阳极氧化产物只有 。电解时实际生成的
。电解时实际生成的 的总量远远小于由理论计算所得
的总量远远小于由理论计算所得 的量,结合电极反应式解释原因:
的量,结合电极反应式解释原因:___________ 。
(4)方法四:一种分解 实现产物分离的物质转化关系如下,其中b、d代表
实现产物分离的物质转化关系如下,其中b、d代表 或
或 中的一种。
中的一种。___________ 。
②该转化过程中会生成副产物 ,通入水蒸气可减少
,通入水蒸气可减少 的产生,反应的方程式为
的产生,反应的方程式为___________ 。
 是一种重要的工业原料,可采用不同的方法制备
是一种重要的工业原料,可采用不同的方法制备 。
。(1)方法一:早期以氯化铵和熟石灰制备
 ,反应的化学方程式为
,反应的化学方程式为(2)方法二:以铁为主的催化剂在400~500℃和
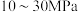 的条件下,由
的条件下,由 和
和 合成氨。
合成氨。①该反应放热,但仍选择较高温度400~500℃。其原因是
②对
 和
和 的反应进行研究:在容积可变的密闭容器中,充入
的反应进行研究:在容积可变的密闭容器中,充入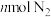 和
和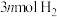 进行反应。在不同压强下(
进行反应。在不同压强下( 、
、 、
、 ),反应达到平衡时,测得
),反应达到平衡时,测得 的体积分数(
的体积分数( )随温度的变化如图所示。判断A点的容器容积和B点的容器容积的大小,并解释原因
)随温度的变化如图所示。判断A点的容器容积和B点的容器容积的大小,并解释原因

②阳极氧化产物只有
 。电解时实际生成的
。电解时实际生成的 的总量远远小于由理论计算所得
的总量远远小于由理论计算所得 的量,结合电极反应式解释原因:
的量,结合电极反应式解释原因:(4)方法四:一种分解
 实现产物分离的物质转化关系如下,其中b、d代表
实现产物分离的物质转化关系如下,其中b、d代表 或
或 中的一种。
中的一种。
②该转化过程中会生成副产物
 ,通入水蒸气可减少
,通入水蒸气可减少 的产生,反应的方程式为
的产生,反应的方程式为
您最近一年使用:0次
17. 中国在氢能研究方面已取得显著进展。绿氢的生产及储存作为氢能利用的关键技术,是当前关注的热点之一、
I.制氢
(1)化学制氢。工业上制取氢气时涉及的一个重要反应是: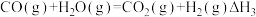
已知:①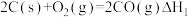
②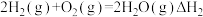
利用 和
和 计算
计算 时,还需要利用
时,还需要利用_______ 反应的 。
。
(2)电化学制氢。光、电催化——化学环反应耦合分解 制
制 的原理示意图如下图所示。
的原理示意图如下图所示。_______ 。
②除了 外,
外,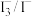 也能实现如图所示循环过程。结合化学用语,说明
也能实现如图所示循环过程。结合化学用语,说明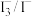 能够使S源源不断产生的原因:
能够使S源源不断产生的原因:_______ 。
Ⅱ.储氢与释氢
(3) 是一种重要的储氢载体,能与水反应生成
是一种重要的储氢载体,能与水反应生成 ,且反应前后B的化合价不变,反应消耗
,且反应前后B的化合价不变,反应消耗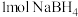 时转移的电子数目为
时转移的电子数目为_______ 。
(4)有机物释氢与储氢。其中一种方法为利用环己烷和苯之间的可逆反应来实现释氢和储氢。
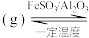
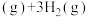
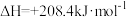 。
。
①在某温度下,向恒容容器中加入环己烷,其起始浓度为 ,平衡时苯的浓度为
,平衡时苯的浓度为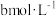 ,该反应的平衡常数
,该反应的平衡常数
_______ 。
②有利于释氢的措施为:_______ (从反应限度的角度回答)。
(5)一定条件下,下图所示装置可实现有机物的电化学储氢(忽略其它有机物)。_______ 。
②该储氢装置的电流效率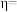
_______ 。( )(计算结果保留小数点后一位)
)(计算结果保留小数点后一位)
I.制氢
(1)化学制氢。工业上制取氢气时涉及的一个重要反应是:
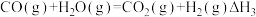
已知:①
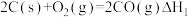
②
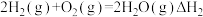
利用
 和
和 计算
计算 时,还需要利用
时,还需要利用 。
。(2)电化学制氢。光、电催化——化学环反应耦合分解
 制
制 的原理示意图如下图所示。
的原理示意图如下图所示。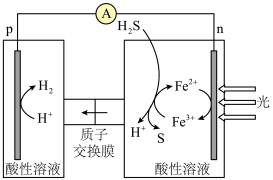
②除了
 外,
外,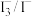 也能实现如图所示循环过程。结合化学用语,说明
也能实现如图所示循环过程。结合化学用语,说明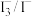 能够使S源源不断产生的原因:
能够使S源源不断产生的原因:Ⅱ.储氢与释氢
(3)
 是一种重要的储氢载体,能与水反应生成
是一种重要的储氢载体,能与水反应生成 ,且反应前后B的化合价不变,反应消耗
,且反应前后B的化合价不变,反应消耗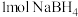 时转移的电子数目为
时转移的电子数目为(4)有机物释氢与储氢。其中一种方法为利用环己烷和苯之间的可逆反应来实现释氢和储氢。

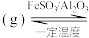

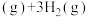
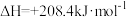 。
。①在某温度下,向恒容容器中加入环己烷,其起始浓度为
 ,平衡时苯的浓度为
,平衡时苯的浓度为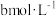 ,该反应的平衡常数
,该反应的平衡常数
②有利于释氢的措施为:
(5)一定条件下,下图所示装置可实现有机物的电化学储氢(忽略其它有机物)。
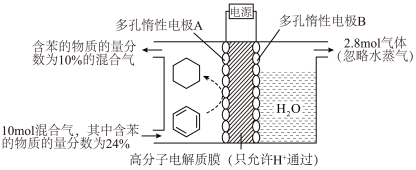
②该储氢装置的电流效率
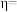
 )(计算结果保留小数点后一位)
)(计算结果保留小数点后一位)
您最近一年使用:0次
2024-05-22更新
|
79次组卷
|
2卷引用:安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试题
解答题-工业流程题
|
较难(0.4)
18. 工业上以磷矿石[主要成分: 、
、 、
、 和有机碳等]为原料生产磷酸和石膏(
和有机碳等]为原料生产磷酸和石膏( ),流程示意图如下:
),流程示意图如下:
回答下列问题:
(1)为提高酸浸速率,可采取的措施有_______ 。(写出1条即可)
(2)生成的HF与 反应,生成二元强酸
反应,生成二元强酸 的离子方程式是:
的离子方程式是:_______ 。
(3)酸浸时 与
与 反应的化学方程式是:
反应的化学方程式是:_______ 。
(4)粗磷酸中的有机碳被 氧化为
氧化为 脱除。相同投料比、相同反应时间,不同温度下的有机碳脱除率如下表所示。分析
脱除。相同投料比、相同反应时间,不同温度下的有机碳脱除率如下表所示。分析 时有机碳脱除率最高的原因:
时有机碳脱除率最高的原因:_______ 。
(5)脱氟过程中发生的化学反应方程式是:_______ ,若按物质的量之比 加入
加入 脱氟,充分反应后,
脱氟,充分反应后,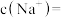
_______  ;
;
(6)脱硫过程中,分批加入一定量的 达到脱硫的目的,其反应离子方程式是
达到脱硫的目的,其反应离子方程式是_______ 。
(7)该工艺中通常使用一定浓度的 溶液洗涤磷石膏(
溶液洗涤磷石膏(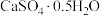 ),原因是
),原因是_____ 。
(8) 浓度(以
浓度(以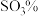 计)、
计)、 浓度(以
浓度(以 计)。一定温度下,石膏存在形式与溶液中
计)。一定温度下,石膏存在形式与溶液中 和
和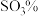 的关系如图所示,下列条件能实现
的关系如图所示,下列条件能实现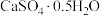 转化为
转化为 的是
的是_______ (填字母)。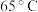 、
、 、
、
B. 、
、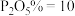 、
、
C.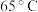 、
、 、
、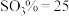
(9)取a g所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗
,消耗 溶液
溶液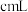 ,精制磷酸中
,精制磷酸中 的质量分数是
的质量分数是_______ 。
 、
、 、
、 和有机碳等]为原料生产磷酸和石膏(
和有机碳等]为原料生产磷酸和石膏( ),流程示意图如下:
),流程示意图如下:
| 物质 | 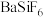 |  |  |  |  |
 |  |  |  | 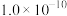 |  |
(1)为提高酸浸速率,可采取的措施有
(2)生成的HF与
 反应,生成二元强酸
反应,生成二元强酸 的离子方程式是:
的离子方程式是:(3)酸浸时
 与
与 反应的化学方程式是:
反应的化学方程式是:(4)粗磷酸中的有机碳被
 氧化为
氧化为 脱除。相同投料比、相同反应时间,不同温度下的有机碳脱除率如下表所示。分析
脱除。相同投料比、相同反应时间,不同温度下的有机碳脱除率如下表所示。分析 时有机碳脱除率最高的原因:
时有机碳脱除率最高的原因:温度 | 40 | 50 | 60 | 70 | 80 | 85 | 90 |
有机碳脱出率约为 | 72 | 75 | 78 | 80 | 82 | 78 | 75 |
 加入
加入 脱氟,充分反应后,
脱氟,充分反应后,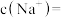
 ;
;(6)脱硫过程中,分批加入一定量的
 达到脱硫的目的,其反应离子方程式是
达到脱硫的目的,其反应离子方程式是(7)该工艺中通常使用一定浓度的
 溶液洗涤磷石膏(
溶液洗涤磷石膏(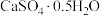 ),原因是
),原因是(8)
 浓度(以
浓度(以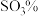 计)、
计)、 浓度(以
浓度(以 计)。一定温度下,石膏存在形式与溶液中
计)。一定温度下,石膏存在形式与溶液中 和
和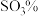 的关系如图所示,下列条件能实现
的关系如图所示,下列条件能实现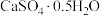 转化为
转化为 的是
的是
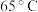 、
、 、
、
B.
 、
、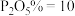 、
、
C.
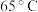 、
、 、
、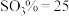
(9)取a g所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用
 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗
,消耗 溶液
溶液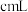 ,精制磷酸中
,精制磷酸中 的质量分数是
的质量分数是
您最近一年使用:0次
2024-05-22更新
|
52次组卷
|
2卷引用:安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试题
解答题-实验探究题
|
较难(0.4)
解题方法
19.  的转化是资源利用和环境保护的重要研究课题。某实验小组在实验室模拟脱除
的转化是资源利用和环境保护的重要研究课题。某实验小组在实验室模拟脱除 并获得硫黄的装置如下(夹持装置略)。已知:
并获得硫黄的装置如下(夹持装置略)。已知: (黑色),
(黑色),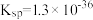
(1)装置A中发生的化学反应方程式是_______ 。
(2)加入药品前,检验装置气密性,方法是_______ 。
(3)装置B的作用是_______ 。
(4)实验Ⅲ中生成黑色沉淀的离子方程式是_______ 。
(5)对于实验Ⅱ的沉淀比实验Ⅰ少的现象,某同学通过分析并得出结论如下:
① 气体持续通入
气体持续通入 溶液中,发生
溶液中,发生 及电离
及电离_______ 。
②完善下列离子方程式:_______ 。
_______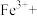 _______
_______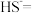 _______
_______ _______
_______ _______。
_______。
结论:实验Ⅱ的pH比实验Ⅰ的小, 增大,不利于
增大,不利于 的溶解和电离,产生沉淀较实验Ⅰ少。
的溶解和电离,产生沉淀较实验Ⅰ少。
(6)对比实验Ⅳ和Ⅰ,实验Ⅳ沉淀比实验Ⅰ多的原因是_______ 。
(7)实验Ⅰ充分反应后,测 浓度:滤出沉淀,取滤液,除去杂质,加入适量稀硫酸,用浓度为
浓度:滤出沉淀,取滤液,除去杂质,加入适量稀硫酸,用浓度为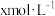 的
的 标准溶液滴定到终点。滴定时发生的离子反应:
标准溶液滴定到终点。滴定时发生的离子反应: ,计算滤液中
,计算滤液中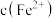 还需要的实验数据:
还需要的实验数据:___ 。
 的转化是资源利用和环境保护的重要研究课题。某实验小组在实验室模拟脱除
的转化是资源利用和环境保护的重要研究课题。某实验小组在实验室模拟脱除 并获得硫黄的装置如下(夹持装置略)。已知:
并获得硫黄的装置如下(夹持装置略)。已知: (黑色),
(黑色),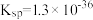
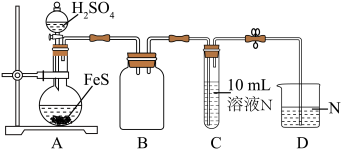
| 序号 | 溶液N | C中实验现象 |
| Ⅰ | 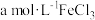 溶液( 溶液( ) ) | 溶液颜色变浅,有乳白色沉淀生成 |
| Ⅱ | 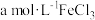 溶液(含少量稀 溶液(含少量稀 , ,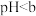 ) ) | 溶液颜色变浅,有乳白色沉淀生成,沉淀比实验Ⅰ少 |
| Ⅲ | 一定浓度的 溶液 溶液 | 溶液颜色变浅,有黑色沉淀生成 |
| Ⅳ | 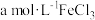 (含有一定浓度的 (含有一定浓度的 溶液, 溶液,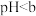 ) ) | 溶液颜色变浅,先有黑色沉淀生成,一段时间后转化为乳白色,沉淀比实验Ⅰ多 |
(1)装置A中发生的化学反应方程式是
(2)加入药品前,检验装置气密性,方法是
(3)装置B的作用是
(4)实验Ⅲ中生成黑色沉淀的离子方程式是
(5)对于实验Ⅱ的沉淀比实验Ⅰ少的现象,某同学通过分析并得出结论如下:
①
 气体持续通入
气体持续通入 溶液中,发生
溶液中,发生 及电离
及电离②完善下列离子方程式:
_______
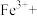 _______
_______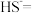 _______
_______ _______
_______ _______。
_______。结论:实验Ⅱ的pH比实验Ⅰ的小,
 增大,不利于
增大,不利于 的溶解和电离,产生沉淀较实验Ⅰ少。
的溶解和电离,产生沉淀较实验Ⅰ少。(6)对比实验Ⅳ和Ⅰ,实验Ⅳ沉淀比实验Ⅰ多的原因是
(7)实验Ⅰ充分反应后,测
 浓度:滤出沉淀,取滤液,除去杂质,加入适量稀硫酸,用浓度为
浓度:滤出沉淀,取滤液,除去杂质,加入适量稀硫酸,用浓度为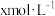 的
的 标准溶液滴定到终点。滴定时发生的离子反应:
标准溶液滴定到终点。滴定时发生的离子反应: ,计算滤液中
,计算滤液中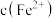 还需要的实验数据:
还需要的实验数据:
您最近一年使用:0次
2024-05-22更新
|
46次组卷
|
2卷引用:安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试题
试卷分析
导出
整体难度:适中
考查范围:物质结构与性质、常见无机物及其应用、化学反应原理、认识化学科学、有机化学基础、化学实验基础
试卷题型(共 19题)
题型
数量
单选题
12
多选题
2
解答题
5
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 元素、核素、同位素 电离能的概念及变化规律 | 单题 |
| 2 | 0.85 | 二氧化硫的化学性质 印刷电路板 盐类水解规律理解及应用 金属的防护 | 单题 |
| 3 | 0.85 | 电子式 电子排布式 共价键的形成及主要类型 利用杂化轨道理论判断分子的空间构型 | 单题 |
| 4 | 0.85 | 离子方程式的正误判断 沉淀转化 电解池电极反应式及化学方程式的书写 | 单题 |
| 5 | 0.65 | 氨的还原性 二氧化氮的化学反应 硝酸的强氧化性 | 单题 |
| 6 | 0.65 | 酮 淀粉和纤维素组成与结构 氢键对物质性质的影响 | 单题 |
| 7 | 0.65 | 沉淀转化 电镀 化学实验方案的设计与评价 | 单题 |
| 9 | 0.85 | 元素非金属性强弱的比较方法 元素性质与电负性的关系 含有氢键的物质 | 单题 |
| 10 | 0.65 | 原电池原理 | 单题 |
| 12 | 0.65 | 影响水电离的因素 盐溶液中离子浓度大小的比较 | 单题 |
| 13 | 0.65 | 盐类双水解反应 浓度对盐类水解的影响 | 单题 |
| 14 | 0.65 | 氯及其化合物 次氯酸及其性质和用途 二氧化硫的化学性质 二氧化硫与其他强氧化剂的反应 | 单题 |
| 二、多选题 | |||
| 8 | 0.65 | 氯气的实验室制法 二氧化氮的化学反应 铵根离子的检验 浓硫酸的强氧化性 | 2个答案 |
| 11 | 0.65 | 催化剂对化学反应速率的影响 | 2个答案 |
| 三、解答题 | |||
| 15 | 0.65 | 轨道表示式 简单配合物的成键 氢键对物质性质的影响 离子晶体 | 结构与性质 |
| 16 | 0.65 | 氨气的实验室制法 影响化学平衡的因素 电解原理的应用 | 原理综合题 |
| 17 | 0.4 | 盖斯定律的应用 化学平衡常数的计算 原电池、电解池综合考查 电子转移计算 | 原理综合题 |
| 18 | 0.4 | 温度对化学反应速率的影响 酸碱中和滴定原理的应用 沉淀转化 溶度积常数相关计算 | 工业流程题 |
| 19 | 0.4 | 氧化还原反应方程式的书写与配平 沉淀的溶解与生成 化学实验方案的设计与评价 氧化还原原理滴定 | 实验探究题 |









