按要求回答以下内容。
(1)已知H2的燃烧热285.8kJ/mol,写出液态水电解生成H2和O2的热化学方程式_______ ;
(2)已知2SO2(g)+O2(g) 2SO3(g) ΔH=-197 kJ/mol,相同温度和压强下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q kJ,则Q
2SO3(g) ΔH=-197 kJ/mol,相同温度和压强下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q kJ,则Q_______ 394kJ(填“>”“<”或“=”)
甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
(3)由表中数据判断ΔH2 _______ 0(填“>”、“<”或“=”)。
(4)若容器容积不变,下列措施可增加甲醇产率的是_______ 。
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.恒温恒容充入He,使体系总压强增大
E.按原比例再充入CO和H2
(5)某温度下,将2 mol CO和6 mol H2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol·L-1,则CO的转化率为_______ ,此时的温度为_______ (从上表中选择);
按如图所示装置进行实验,并回答下列问题:

(6)甲池,通入CH3OH(甲醇)的电极反应式为_______ 。
(7)乙池中的总反应化学方程式为_______ 。
(8)当甲池中消耗O2为0.56L(标准状况下)时,理论上乙池中B极的质量增加_______ g;此时丙装置中_______ (填“C”或“D”)电极析出3.20g金属,则按丙装置中的的某盐溶液可能是_______ (填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(1)已知H2的燃烧热285.8kJ/mol,写出液态水电解生成H2和O2的热化学方程式
(2)已知2SO2(g)+O2(g)
 2SO3(g) ΔH=-197 kJ/mol,相同温度和压强下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q kJ,则Q
2SO3(g) ΔH=-197 kJ/mol,相同温度和压强下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q kJ,则Q甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1反应II:CO(g)+2H2(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(4)若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.恒温恒容充入He,使体系总压强增大
E.按原比例再充入CO和H2
(5)某温度下,将2 mol CO和6 mol H2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol·L-1,则CO的转化率为
按如图所示装置进行实验,并回答下列问题:

(6)甲池,通入CH3OH(甲醇)的电极反应式为
(7)乙池中的总反应化学方程式为
(8)当甲池中消耗O2为0.56L(标准状况下)时,理论上乙池中B极的质量增加
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
更新时间:2022-06-29 10:53:59
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①ΔH 1_____ 0,ΔH 3_____ 0。(填“>”或“<”)
②N2(g)+O2(g) = 2NO(g) ΔH=______ kJ·mol-1。
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是_______ (填字母)。
A.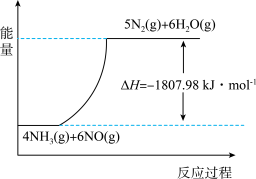
B.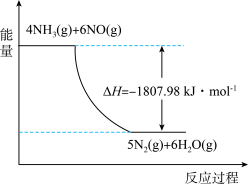
C.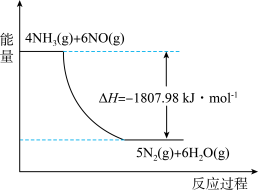
(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=________ ,1.6 g CH4还原NO2 生成N2和液态水时放出的热量为______ kJ。
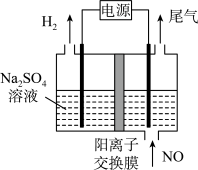
(4)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极),电解过程中NO转化为硝酸的化学方程式为______ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | ΔH 1 | ΔH 2 | ΔH 3 |
| 热量值kJ·mol-1 | 945 | 498 | 630 |
①ΔH 1
②N2(g)+O2(g) = 2NO(g) ΔH=
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是
A.

B.

C.

(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=
(4)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极),电解过程中NO转化为硝酸的化学方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】我国力争于2030年前做到碳达峰,2060年前实现碳中和。利用反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H,可减少CO2排放,并合成清洁能源。
CH3OH(g)+H2O(g)△H,可减少CO2排放,并合成清洁能源。
(1)该反应一般认为通过如下步骤来实现:。
①CO2(g)+H2(g) H2O(g)+CO(g)△H1=+41kJ·mol-1
H2O(g)+CO(g)△H1=+41kJ·mol-1
②CO(g)+2H2(g) CH3OH(g)△H2=-90kJ·mol-1
CH3OH(g)△H2=-90kJ·mol-1
①总反应的△H=___________ kJ·mol-1;
②该反应在___________ 能自发(填“高温”、“低温”、“任何温度”、“一定不”);
③若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
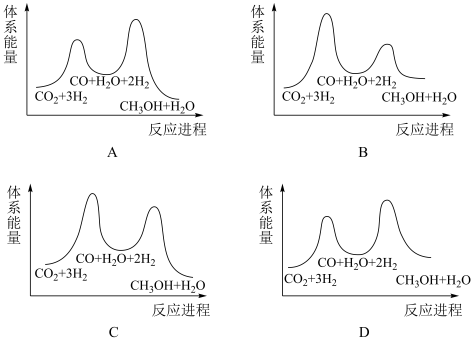
(2)500°C时,在容积为2L的密闭容器中充入3molCO2和8molH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得t=5min时,反应达到平衡,此时n(CO2)=1.0mol。
CH3OH(g)+H2O(g),测得t=5min时,反应达到平衡,此时n(CO2)=1.0mol。
①从反应开始到平衡,H2的平均反应速率v(H2)=___________ ;平衡时H2的转化率为___________ ;该反应的平衡常数为___________ 。
②该温度下,某时刻测得容器内CO2、H2、CH3OH、H2O的物质的量分别为2mol、2mol、lmol和lmol,此时该反应正、逆反应速率的关系式是___________ (填代号)。
a.v(正)>v(逆)b.v(正)<v(逆)
c.v(正)=v(逆)d.无法判断
 CH3OH(g)+H2O(g)△H,可减少CO2排放,并合成清洁能源。
CH3OH(g)+H2O(g)△H,可减少CO2排放,并合成清洁能源。(1)该反应一般认为通过如下步骤来实现:。
①CO2(g)+H2(g)
 H2O(g)+CO(g)△H1=+41kJ·mol-1
H2O(g)+CO(g)△H1=+41kJ·mol-1②CO(g)+2H2(g)
 CH3OH(g)△H2=-90kJ·mol-1
CH3OH(g)△H2=-90kJ·mol-1①总反应的△H=
②该反应在
③若反应①为慢反应,下列示意图中能体现上述反应能量变化的是

(2)500°C时,在容积为2L的密闭容器中充入3molCO2和8molH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得t=5min时,反应达到平衡,此时n(CO2)=1.0mol。
CH3OH(g)+H2O(g),测得t=5min时,反应达到平衡,此时n(CO2)=1.0mol。①从反应开始到平衡,H2的平均反应速率v(H2)=
②该温度下,某时刻测得容器内CO2、H2、CH3OH、H2O的物质的量分别为2mol、2mol、lmol和lmol,此时该反应正、逆反应速率的关系式是
a.v(正)>v(逆)b.v(正)<v(逆)
c.v(正)=v(逆)d.无法判断
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】 与烷烃耦合等很多反应均有利于减少空气中
与烷烃耦合等很多反应均有利于减少空气中 的含量,实现“碳达峰”“碳中和”的目标。
的含量,实现“碳达峰”“碳中和”的目标。
Ⅰ. 与
与 的耦合反应
的耦合反应
已知反应:
①
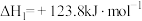
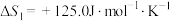
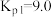
②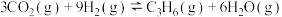
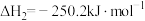
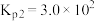
③
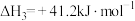
(1) 与
与 耦合反应在
耦合反应在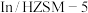 催化剂作用下的微观过程如下:
催化剂作用下的微观过程如下:
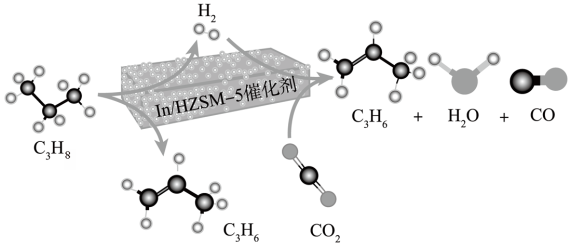
写出该过程的热化学方程式___________ 。
(2)为提高丙烷与 耦合过程中
耦合过程中 的产率,可采取的措施有
的产率,可采取的措施有___________ (填标号)。
a.恒容时充入惰性气体 b.增大 的浓度 c.改善催化剂的性能
的浓度 c.改善催化剂的性能
(3)在一定温度下,向恒容密闭容器中充入一定量的 ,发生反应①,达到平衡时压强增大20%,则平衡时
,发生反应①,达到平衡时压强增大20%,则平衡时 的转化率为
的转化率为___________ 。
(4) 与
与 耦合反应时发生另一反应:
耦合反应时发生另一反应: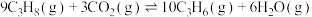 ,则该反应的平衡常数
,则该反应的平衡常数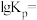
___________ 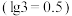 。
。
Ⅱ. 催化加氢制甲醇
催化加氢制甲醇
已知反应:④
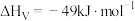
⑤
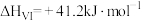
(5)不同条件下,相同的时间段内 的选择性和产率随温度的变化如图。(
的选择性和产率随温度的变化如图。( 的选择性=
的选择性=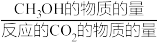 ×100%
×100%
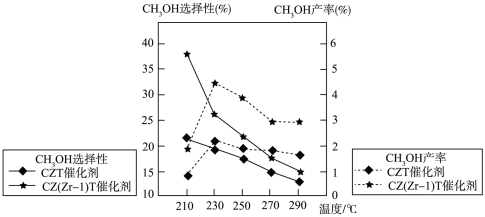
①由图可知,合成甲醇的适宜条件为___________ (填标号)。
A.CZT催化剂 B.CZ(Zr-1)T催化剂 C.230℃ D.290℃
②在230℃以上,升高温度, 的平衡转化率增大,但甲醇的产率降低,原因是
的平衡转化率增大,但甲醇的产率降低,原因是___________ 。
Ⅲ.利用电催化可将 同时转化为多种燃料,装置如图:
同时转化为多种燃料,装置如图:
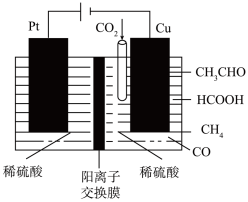
(6)其中铜电极上产生HCOOH的电极反应式为___________ 。
 与烷烃耦合等很多反应均有利于减少空气中
与烷烃耦合等很多反应均有利于减少空气中 的含量,实现“碳达峰”“碳中和”的目标。
的含量,实现“碳达峰”“碳中和”的目标。Ⅰ.
 与
与 的耦合反应
的耦合反应已知反应:
①

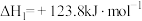
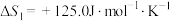
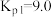
②
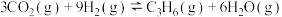
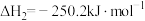
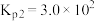
③

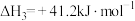
(1)
 与
与 耦合反应在
耦合反应在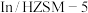 催化剂作用下的微观过程如下:
催化剂作用下的微观过程如下:
写出该过程的热化学方程式
(2)为提高丙烷与
 耦合过程中
耦合过程中 的产率,可采取的措施有
的产率,可采取的措施有a.恒容时充入惰性气体 b.增大
 的浓度 c.改善催化剂的性能
的浓度 c.改善催化剂的性能(3)在一定温度下,向恒容密闭容器中充入一定量的
 ,发生反应①,达到平衡时压强增大20%,则平衡时
,发生反应①,达到平衡时压强增大20%,则平衡时 的转化率为
的转化率为(4)
 与
与 耦合反应时发生另一反应:
耦合反应时发生另一反应: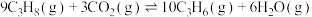 ,则该反应的平衡常数
,则该反应的平衡常数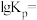
 。
。Ⅱ.
 催化加氢制甲醇
催化加氢制甲醇已知反应:④

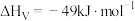
⑤

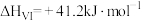
(5)不同条件下,相同的时间段内
 的选择性和产率随温度的变化如图。(
的选择性和产率随温度的变化如图。( 的选择性=
的选择性=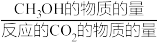 ×100%
×100%
①由图可知,合成甲醇的适宜条件为
A.CZT催化剂 B.CZ(Zr-1)T催化剂 C.230℃ D.290℃
②在230℃以上,升高温度,
 的平衡转化率增大,但甲醇的产率降低,原因是
的平衡转化率增大,但甲醇的产率降低,原因是Ⅲ.利用电催化可将
 同时转化为多种燃料,装置如图:
同时转化为多种燃料,装置如图:
(6)其中铜电极上产生HCOOH的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】肼是一种高能燃料。已知各共价键键能(断裂或形成1mol共价键时吸收或释放的能量)如表:
(1)N2H4(g)+O2(g)⇌N2(g)+2H2O(l) ∆H=________ kJ•mol﹣1。
(2)密闭容器中进行反应:3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g) ∆H<0反应的化学平衡表达式为K=
Fe3O4(s)+4H2(g) ∆H<0反应的化学平衡表达式为K=________ 。
(3)已知:600℃时,上述反应的平衡常数K=16。现有如图甲(恒温恒压)和如图乙(恒温恒容)两容器:
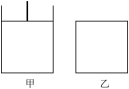
起始时按下表所示分别加入各物质,体积为2L,在600℃时反应经过一段时间后均达平衡。
①关于甲、乙容器,下列说法正确的是________ 。
A.反应开始时两容器内的逆反应速率:甲<乙
B.若甲容器内气体的密度不再变化,则说明反应已达到平衡状态
C.若乙容器内气体的压强不再变化,则说明反应已达到平衡状态
D.平衡后添加Fe3O4,两容器内的平衡均逆向移动
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=________ 。
③平衡后若将乙容器体系温度突然降低100℃,图象中能正确反映平衡移动过程中容器内变化情况的是________ 。
A. B.
B. C.
C.
(4)如图为恒容绝热容器:

进行上述反应,起始与平衡时的各物质的量见表:
若在达到平衡后的容器丙中,分别按照下列A、B、C三种情况继续添加各物质,则再次达平衡时,容器丙中H2的百分含量按由大到小的顺序______ (用A、B、C表示)。
| N≡N | O=O | N-N | N-H | O-H | |
| 键能(KJ•mol﹣1) | 946 | 497 | 154 | 391 | 463 |
(1)N2H4(g)+O2(g)⇌N2(g)+2H2O(l) ∆H=
(2)密闭容器中进行反应:3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g) ∆H<0反应的化学平衡表达式为K=
Fe3O4(s)+4H2(g) ∆H<0反应的化学平衡表达式为K=(3)已知:600℃时,上述反应的平衡常数K=16。现有如图甲(恒温恒压)和如图乙(恒温恒容)两容器:

起始时按下表所示分别加入各物质,体积为2L,在600℃时反应经过一段时间后均达平衡。
| Fe | H2O(g) | Fe3O4 | H2 | |
| 甲/mol | 2.0 | 1.0 | 2.0 | 0.5 |
| 乙/mol | 2.0 | 2.0 | 2.0 | 1.0 |
①关于甲、乙容器,下列说法正确的是
A.反应开始时两容器内的逆反应速率:甲<乙
B.若甲容器内气体的密度不再变化,则说明反应已达到平衡状态
C.若乙容器内气体的压强不再变化,则说明反应已达到平衡状态
D.平衡后添加Fe3O4,两容器内的平衡均逆向移动
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=
③平衡后若将乙容器体系温度突然降低100℃,图象中能正确反映平衡移动过程中容器内变化情况的是
A.
 B.
B. C.
C.
(4)如图为恒容绝热容器:

进行上述反应,起始与平衡时的各物质的量见表:
| Fe | H2O(g) | Fe3O4 | H2 | |
| 起始/mol | 3.0 | 3.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| Fe | H2O(g) | Fe3O4 | H2 | |
| A/mol | 3.0 | 3.0 | 0 | 0 |
| B/mol | 0 | 0 | 3.0 | 3.0 |
| C/mol | m | n | p | q |
若在达到平衡后的容器丙中,分别按照下列A、B、C三种情况继续添加各物质,则再次达平衡时,容器丙中H2的百分含量按由大到小的顺序
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】我国拥有众多非物质文化遗产,如建窑建盏烧制技艺、浦城剪纸、武夷岩茶(大红袍)制作技艺等。
I.建盏的魅力斑纹是由釉面里面由内至外呈现的,三维立体,栩栩如生,主要因建阳水吉附近的南方红壤土中蕴含大量的铁,通过高温烧制控制进入的氧气量,把坯体铁析晶和釉水铁析晶呈现出来,这些表现在建盏的釉色当中,该过程会形成不同形态的铁(如Fe2O3、FeO、,Fe3O4等)。以下是烧制过程中可能发生反应的热化学方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=akJ·mol-1
FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH2=bkJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=ckJ·mol-1
(1)写出CO气体还原Fe2O3固体得到Fe3O4固体和CO2气体的热化学方程式:________ 。
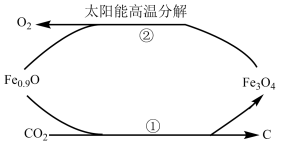
(2)在太阳能的作用下,缺铁氧化物(如Fe0.9O)能催化分解CO2,其过程如图所示。过程①的化学方程式是___________ ,过程②能量转化的主要形式为___________ 。
II.一种以CO2为碳源,在催化剂作用下催化加氢制备可再生能源甲醇的反应如下:
反应i:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH4=-49.1kJ·mol-1
反应ii:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH5=+41.1kJ·mol-1
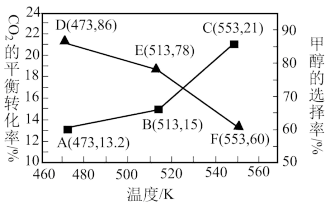
(3)往恒容密闭容器中按n(CO2):n(H2)=1:3(总量为a mol)充入反应物,在合适催化剂作用下,发生反应i、ii,CO2的平衡转化率和甲醇的选择率(转化为甲醇的CO2物质的量与参加反应的CO2总物质的量之比)如图所示。在513K达平衡时,甲醇的物质的量为________ (列出计算式)mol。随着温度的升高,CO2的平衡转化率升高但甲醇的选择率降低的原因是_______ 。
(4)现向恒温恒压(0.1MPa)的密闭容器中充入1molCO2、3molH2和6molHe,选择合适的催化剂使其仅按反应i进行,上述反应达平衡时,测得CO2的转化率为20%,则该反应的Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,结果精确到0.1)MPa-2。CO2制备CH3OH的过程中,往往伴随着反应ii,从而导致CH3OH的选择率下降,有研究表明,在原料气中掺入适量CO,能提高CH3OH的选择率,试说明其可能的原因:___________ 。
I.建盏的魅力斑纹是由釉面里面由内至外呈现的,三维立体,栩栩如生,主要因建阳水吉附近的南方红壤土中蕴含大量的铁,通过高温烧制控制进入的氧气量,把坯体铁析晶和釉水铁析晶呈现出来,这些表现在建盏的釉色当中,该过程会形成不同形态的铁(如Fe2O3、FeO、,Fe3O4等)。以下是烧制过程中可能发生反应的热化学方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=akJ·mol-1
FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH2=bkJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=ckJ·mol-1
(1)写出CO气体还原Fe2O3固体得到Fe3O4固体和CO2气体的热化学方程式:

(2)在太阳能的作用下,缺铁氧化物(如Fe0.9O)能催化分解CO2,其过程如图所示。过程①的化学方程式是
II.一种以CO2为碳源,在催化剂作用下催化加氢制备可再生能源甲醇的反应如下:
反应i:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH4=-49.1kJ·mol-1
反应ii:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH5=+41.1kJ·mol-1
(3)往恒容密闭容器中按n(CO2):n(H2)=1:3(总量为a mol)充入反应物,在合适催化剂作用下,发生反应i、ii,CO2的平衡转化率和甲醇的选择率(转化为甲醇的CO2物质的量与参加反应的CO2总物质的量之比)如图所示。在513K达平衡时,甲醇的物质的量为

(4)现向恒温恒压(0.1MPa)的密闭容器中充入1molCO2、3molH2和6molHe,选择合适的催化剂使其仅按反应i进行,上述反应达平衡时,测得CO2的转化率为20%,则该反应的Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】N2O和CO是常见的环境污染气体。
(1)对于反应N2O(g)+CO(g)⇌CO2(g)+N2(g)来说,Fe+可作为此反应的催化剂。其总反应分两步进行,第一步为Fe++N2O⇌FeO++N2,第二步为_______ (写方程式)。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g)⇌2N2(g)+O2(g)。容器I、II、III中N2O的平衡转化率如图乙所示,请回答:
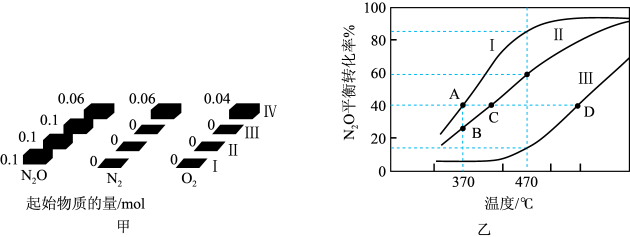
①该反应的ΔH_______ (填“>”或“<”)0.
②若容器I的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为_______ 。B点对应的平衡常数K=_______ (保留两位有效数字)。
③图中A、C、D三点容器内气体密度由大到小的顺序是_______ 。
④若容器IV体积为1L,反应在370℃下进行,则起始时反应______ (填“正向”“逆向”或“不”)进行。
(1)对于反应N2O(g)+CO(g)⇌CO2(g)+N2(g)来说,Fe+可作为此反应的催化剂。其总反应分两步进行,第一步为Fe++N2O⇌FeO++N2,第二步为
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g)⇌2N2(g)+O2(g)。容器I、II、III中N2O的平衡转化率如图乙所示,请回答:

①该反应的ΔH
②若容器I的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为
③图中A、C、D三点容器内气体密度由大到小的顺序是
④若容器IV体积为1L,反应在370℃下进行,则起始时反应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮的化合物在生产、生活中有广泛应用。
(1)已知几种共价键的键能数据如表所示:
根据表格数据,N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =___________ kJ•mol-1。
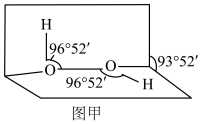
(2)H2O可与H+结合生成H3O+,H2O中H-O-H的键角比H3O+中的___________ (填“大”或“小”)。H2O2是常用的氧化剂,其分子结构如图甲所示。H2O2能与水混溶,却不溶于CCl4的原因是 ___________ 。 H<0。测得相同时间内NO的转化率随温度的变化如图乙所示。
H<0。测得相同时间内NO的转化率随温度的变化如图乙所示。___________ (填“>”、“<”或“=”) v逆(NO)。
②bc段NO的转化率随温度升高而降低,可能的原因是___________ 。(任答一点)
(4)工业上用天然气处理NO2,消除NO2发生的反应为CH4(g)+2NO2(g) CO2(g)+2H2O(g)+N2(g)。在一定温度下,充入1molCH4和2molNO2,发生上述反应,起始时测得总压强为90kPa.N2的分压与时间的关系如图丙所示。
CO2(g)+2H2O(g)+N2(g)。在一定温度下,充入1molCH4和2molNO2,发生上述反应,起始时测得总压强为90kPa.N2的分压与时间的关系如图丙所示。___________ kPa•min-1
②该温度下,平衡常数Kp=___________ kPa。(提示:用气体分压计算的平衡常数为Kp,气体分压=总压×物质的量分数)
(5)工业上制备HCN的反应为CH4(g)+NH3(g)⇌HCN(g)+3H2(g) ∆H>0。速率方程为v正=k正c(CH4)•c(NH3),v逆=k逆c(HCN)•c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。
①其他条件不变,反应达到平衡后,NH3的转化率随着条件X的增大而增大,则X可能是___________ 。(答一种即可)
②升高温度,k逆增大的倍数___________ k正增大的倍数(填“>”、“<”或“=”)。
(1)已知几种共价键的键能数据如表所示:
| 共价键 | H-N | N-N | N≡N | O=O | H-O |
| 键能/kJ•mol-1 | 391 | 160 | 945 | 498 | 467 |
(2)H2O可与H+结合生成H3O+,H2O中H-O-H的键角比H3O+中的
 H<0。测得相同时间内NO的转化率随温度的变化如图乙所示。
H<0。测得相同时间内NO的转化率随温度的变化如图乙所示。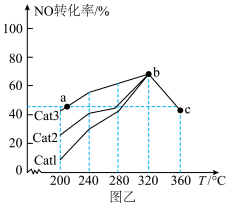
②bc段NO的转化率随温度升高而降低,可能的原因是
(4)工业上用天然气处理NO2,消除NO2发生的反应为CH4(g)+2NO2(g)
 CO2(g)+2H2O(g)+N2(g)。在一定温度下,充入1molCH4和2molNO2,发生上述反应,起始时测得总压强为90kPa.N2的分压与时间的关系如图丙所示。
CO2(g)+2H2O(g)+N2(g)。在一定温度下,充入1molCH4和2molNO2,发生上述反应,起始时测得总压强为90kPa.N2的分压与时间的关系如图丙所示。
②该温度下,平衡常数Kp=
(5)工业上制备HCN的反应为CH4(g)+NH3(g)⇌HCN(g)+3H2(g) ∆H>0。速率方程为v正=k正c(CH4)•c(NH3),v逆=k逆c(HCN)•c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。
①其他条件不变,反应达到平衡后,NH3的转化率随着条件X的增大而增大,则X可能是
②升高温度,k逆增大的倍数
您最近一年使用:0次
【推荐2】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO  2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H______ 0(填写“>”、“<”、“=”。
(2)前2s内的平均反应速率v(N2)=_____________ 。
(3)在该温度下,反应的平衡常数K=______________ 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是_____ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
①请在上表格中填入剩余的实验条件数据________________ 。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________________ 。

 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol/L | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol/L | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在上述条件下反应能够自发进行,则反应的△H
(2)前2s内的平均反应速率v(N2)=
(3)在该温度下,反应的平衡常数K=
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 | T/℃ | NO初始浓度mol/L | CO初始浓度mol/L | 催化剂的比表面积m2/g |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氮及其化合物在生产、生活中有着重要的作用。请回答下列问题:
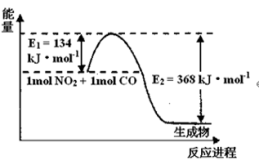
(1)下图是常温下1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:_______
(2)在恒温、恒容的密闭容器中,通入一定量的N2O4发生反应N2O4(g)⇌2NO2(g) △H 如图
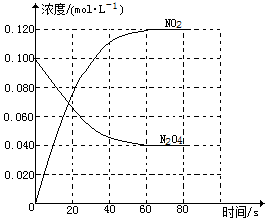
①在0-60s时段,反应速率v (N2O4)为_______ mol·L-1·s-1。
②温度升高,混合气体的颜色变深,则△H_______ 0 (填“>”或“<”)。
③改变条件重新达到平衡时,要使N2O4的体积分数变大,可采取的措施有_______ (填字母)。
A.向混合气体中通入N2O4 B.升高温度
C.向混合气体中通入NO2 D.使用高效催化剂
(3)实验室可用NaOH溶液吸收NO2 ,反应2NO2 +2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2molNO2 恰好完全反应得1L溶液A,溶液B为0.1mol·L-1的CH3COONa溶液。
①A、B两溶液中c( )、c(
)、c( )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为_______ (已知HNO2的电离常数Ka=7.1×10-4mol·L-1,CH3COOH的电离常数Ka=1.7×10-5mol·L-1)。
②可使A、B两溶液的PH相等的方法是_______ (填字母)。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH
(1)下图是常温下1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

(2)在恒温、恒容的密闭容器中,通入一定量的N2O4发生反应N2O4(g)⇌2NO2(g) △H 如图

①在0-60s时段,反应速率v (N2O4)为
②温度升高,混合气体的颜色变深,则△H
③改变条件重新达到平衡时,要使N2O4的体积分数变大,可采取的措施有
A.向混合气体中通入N2O4 B.升高温度
C.向混合气体中通入NO2 D.使用高效催化剂
(3)实验室可用NaOH溶液吸收NO2 ,反应2NO2 +2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2molNO2 恰好完全反应得1L溶液A,溶液B为0.1mol·L-1的CH3COONa溶液。
①A、B两溶液中c(
 )、c(
)、c( )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为②可使A、B两溶液的PH相等的方法是
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】钨(74W)是熔点最高的金属,是重要的战略物资。自然界中钨矿石的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、P、As的化合物。由黑钨矿冶炼钨的工艺流程如下:
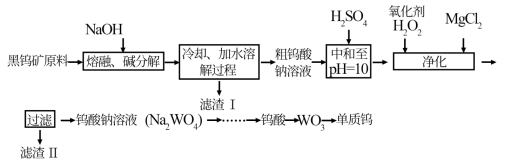
已知:①滤渣I的主要成分是Fe2O3、MnO2。②上述流程中,除最后一步外,其余步骤钨的化合价未变。③常温下钨酸难溶于水。
回答下列问题:
(1)钨酸中钨元素的化合价为_________ ,写出MnWO4在熔融条件下发生碱分解反应生成MnO2的化学方程式___________________________________________ 。
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为_______________________________ 。
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则T1________ T2(填“>”或“<”)。

将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为_________________ ,T2时该反应的平衡常数为_________________ 。
(4)硬质合金刀具中含碳化钨(WC),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸并放出CO2。该阳极反应式为_________________ 。

已知:①滤渣I的主要成分是Fe2O3、MnO2。②上述流程中,除最后一步外,其余步骤钨的化合价未变。③常温下钨酸难溶于水。
回答下列问题:
(1)钨酸中钨元素的化合价为
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则T1

将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为
(4)硬质合金刀具中含碳化钨(WC),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸并放出CO2。该阳极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】 资源化能有效应对全球的气候变化,并且能充分利用碳资源。
资源化能有效应对全球的气候变化,并且能充分利用碳资源。
(1) 催化加氢合成
催化加氢合成 其过程中主要发生下列反应:
其过程中主要发生下列反应:
反应Ⅰ:
反应Ⅱ: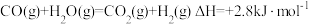
反应Ⅲ: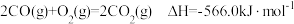
则反应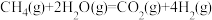 的
的
___________  。
。
(2)电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理示意图如图1。
的原理示意图如图1。
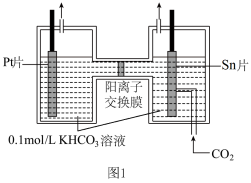
写出阴极 还原为
还原为 的电极反应式:
的电极反应式:___________ ,电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是___________ 。
(3) 催化加氢合成二甲醚。
催化加氢合成二甲醚。
反应Ⅰ:
反应Ⅱ:
①反应Ⅱ的平衡常数表达式
___________ 。
②在恒压、 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性(
的选择性( 的选择性
的选择性 )随温度的变化如图2。
)随温度的变化如图2。
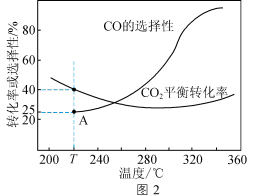
T℃时,起始投入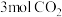 、
、 ,达到平衡时反应I理论上消耗
,达到平衡时反应I理论上消耗 的物质的量为
的物质的量为___________  。合成二甲醚时较适宜的温度为260℃,其原因是
。合成二甲醚时较适宜的温度为260℃,其原因是___________ 。
 资源化能有效应对全球的气候变化,并且能充分利用碳资源。
资源化能有效应对全球的气候变化,并且能充分利用碳资源。(1)
 催化加氢合成
催化加氢合成 其过程中主要发生下列反应:
其过程中主要发生下列反应:反应Ⅰ:

反应Ⅱ:
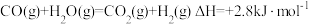
反应Ⅲ:
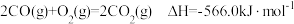
则反应
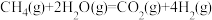 的
的
 。
。(2)电解法转化
 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理示意图如图1。
的原理示意图如图1。
写出阴极
 还原为
还原为 的电极反应式:
的电极反应式: 溶液浓度降低,其原因是
溶液浓度降低,其原因是(3)
 催化加氢合成二甲醚。
催化加氢合成二甲醚。反应Ⅰ:

反应Ⅱ:

①反应Ⅱ的平衡常数表达式

②在恒压、
 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性(
的选择性( 的选择性
的选择性 )随温度的变化如图2。
)随温度的变化如图2。
T℃时,起始投入
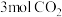 、
、 ,达到平衡时反应I理论上消耗
,达到平衡时反应I理论上消耗 的物质的量为
的物质的量为 。合成二甲醚时较适宜的温度为260℃,其原因是
。合成二甲醚时较适宜的温度为260℃,其原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:
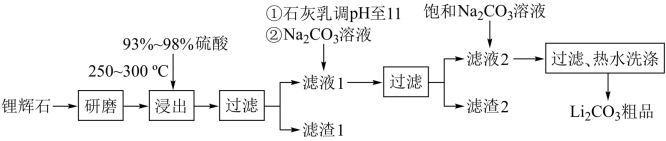
已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2+H2SO4(浓) Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O
③某些物质的溶解度(s)如下表所示。
(1)滤渣2的主要成分有___ 。
(2)向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)____ 。
(3)最后一个步骤中,用“热水洗涤”的目的是____ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用阳离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热沉锂,过滤、烘干可得高纯Li2CO3。
①a中,阳极的电极反应式是__ 。
②电解一段时间后,当外电路转移2mol电子,LiOH溶液质量增加___ g,b中生成Li2CO3反应的化学方程式是___ 。
(5)磷酸亚铁锂电池总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:___ 。

已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2+H2SO4(浓)
 Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O③某些物质的溶解度(s)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(2)向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)
(3)最后一个步骤中,用“热水洗涤”的目的是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用阳离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热沉锂,过滤、烘干可得高纯Li2CO3。
①a中,阳极的电极反应式是
②电解一段时间后,当外电路转移2mol电子,LiOH溶液质量增加
(5)磷酸亚铁锂电池总反应为:FePO4+Li
 LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
您最近一年使用:0次



