1 . 废物利用对保护环境、节约资源和带动社会效益起着积极作用。某废旧金属材料主要为铜、铝、铁及其氧化物的混合物,利用该材料得到胆矾的一种流程如下:
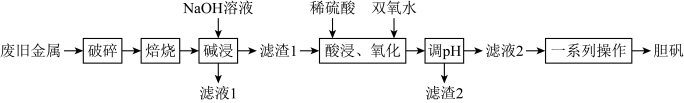
已知:调pH可将Fe2+与Cu2+分离,但不易将Fe2+与Cu2+分离。
请回答下列问题:
(1)流程中“粉碎”的目的是___________ 。
(2)“碱浸”时发生反应的离子方程式为___________ 。
(3)“酸浸”后“氧化”时发生反应的离子方程式为___________ ;该过程温度不宜过高,原因为___________ 。
(4)“滤渣2”的成分为___________ (填化学式);“一系列操作”不能采用直接蒸发结晶的原因为___________ 。
(5)有同学从上述流程中的“氧化”和“调pH”联想到过氧化钠也具有氧化性,且与水反应能生成氢氧化钠。于是向硫酸亚铁溶液中加入一定量的过氧化钠固体,观察到有红褐色固体产生且无气体生成。若过氧化钠与硫酸亚铁反应的物质的量之比为1:2,则该反应的离子方程式为___________ 。

已知:调pH可将Fe2+与Cu2+分离,但不易将Fe2+与Cu2+分离。
请回答下列问题:
(1)流程中“粉碎”的目的是
(2)“碱浸”时发生反应的离子方程式为
(3)“酸浸”后“氧化”时发生反应的离子方程式为
(4)“滤渣2”的成分为
(5)有同学从上述流程中的“氧化”和“调pH”联想到过氧化钠也具有氧化性,且与水反应能生成氢氧化钠。于是向硫酸亚铁溶液中加入一定量的过氧化钠固体,观察到有红褐色固体产生且无气体生成。若过氧化钠与硫酸亚铁反应的物质的量之比为1:2,则该反应的离子方程式为
您最近一年使用:0次
2 . 室温下,经指定操作后,下列各组溶液中离子还能大量共存的是
A.加入Na2SO3:Ca2+、Al3+、ClO-、 |
B.加入NaOH:Ba2+、Fe3+、 、ClO- 、ClO- |
C.加入FeSO4:H+、Cu2+、 、 、 |
D.加入(NH4)2SO4:K+、Zn2+、Cl-、 |
您最近一年使用:0次
2024-03-08更新
|
168次组卷
|
2卷引用:贵州省贵阳市白云区第二高级中学2023-2024学年高三上学期月11质量监测化学试卷
3 . 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系,下列说法错误的是
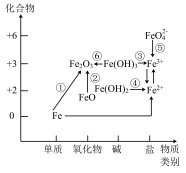

| A.铁在高温条件下与水蒸气反应不能实现转化① |
B.酸性 溶液敞口放置在空气中发生反应的离子方程式为 溶液敞口放置在空气中发生反应的离子方程式为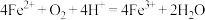 |
C.由图可预测高铁酸盐( )具有强氧化性 )具有强氧化性 |
D. 生成 生成 不可通过化合反应制得 不可通过化合反应制得 |
您最近一年使用:0次
名校
4 . 已知氧化性: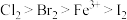 ,还原性:
,还原性: ,下列反应的化学方程式或离子方程式不成立的是
,下列反应的化学方程式或离子方程式不成立的是
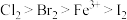 ,还原性:
,还原性: ,下列反应的化学方程式或离子方程式不成立的是
,下列反应的化学方程式或离子方程式不成立的是A. |
B.向 溶液中通入少量氯气; 溶液中通入少量氯气; |
C.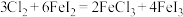 |
D.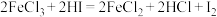 |
您最近一年使用:0次
2024-03-07更新
|
49次组卷
|
2卷引用:湖北省武汉西藏中学2023-2024学年高一下学期5月期中考试化学试题
名校
解题方法
5 . 微观粒子在物质世界中扮演着不可或缺的角色,下列微粒在给定溶液中能大量共存的是
A.加入镁粉产生氢气的溶液:Na+、NO 、SO 、SO 、Cl- 、Cl- |
B.常温下pH<7的溶液:Na+、Mg2+、NO 、SO 、SO |
| C.无色透明的溶液:K+、Fe3+、Cl-、OH- |
D.使pH试纸变蓝的溶液:NH 、Al3+、SO 、Al3+、SO 、CH3COOH 、CH3COOH |
您最近一年使用:0次
2024-03-07更新
|
545次组卷
|
4卷引用:湖南省长沙市湖南师范大学附属中学2023-2024学年高一下学期入学考试化学试卷
名校
6 . 下列实验中的现象及现象过程中与氧化还原反应无关的是
| 选项 | A | B | C | D |
| 实验 | 过量的硫酸亚铁溶液加入到高锰酸钾溶液中 | 向碳酸钠溶液中边振荡边滴加稀盐酸直至过量 | 漂白粉长期暴露在潮湿的空气中 | 紫色石蕊试液滴入新制氯水中 |
| 现象及现象过程中 | 紫色褪去,溶液最终变为浅黄色 | 最初没有现象,继续滴加稀盐酸产生气泡 | 白色粉末失效最终变成团块,无法均匀地溶解在水中 | 最初没有现象,继续滴加稀盐酸产生气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 化学与生产、生活及环境密切相关,下列说法错误的是
A.维生素C具有还原性,因此常与补铁剂(有效成分为 )同服 )同服 |
| B.纯铝具有强度高、密度小、抗腐蚀能力强等优点,常用于制造飞机外壳 |
| C.从石墨中剥离出的石墨烯薄片能导电,因此石墨烯是电解质 |
| D.国家速滑馆采用二氧化碳制冰技术,比传统制冷剂氟利昂更加环保 |
您最近一年使用:0次
8 . 下列反应对应的离子方程式正确的是
A.将过量的铁粉加入稀硝酸中: |
B.向 溶液中加入过量 溶液中加入过量 : :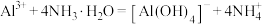 |
C.向碳酸氢钙溶液中加入过量的NaOH溶液: |
D. 溶解在HI溶液中: 溶解在HI溶液中: |
您最近一年使用:0次
9 . 室温下,下列各组粒子在指定溶液中能大量共存的是
A.使pH试纸变红的溶液: |
B. 溶液: 溶液: |
C. 溶液: 溶液: |
D.加入铁粉放出氢气的溶液: |
您最近一年使用:0次
10 . 铁是人类较早使用的金属之一,根据铁及其化合物之间的相互转化,回答下列问题:
(1)Fe2+易被人体吸收,医生建议在服用补铁剂时,同时服用维生素C.维生素C的作用是______ 。
(2)印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的离子方程式:______ 。
(3)某废料铁泥的主要成分为Fe2O3、FeO、Fe和杂质(杂质不与硫酸反应)。现取wg废料铁泥提取Fe2O3,设计实验流程如下:

①分离溶液A和沉淀C的实验操作为______ 。
②能检验溶液A中含有Fe2+的试剂是______ (填字母)。
A.铁粉 B.酸性KMnO4溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为______ 。
④若最终获得ngFe2O3,则废料铁泥中铁元素的质量分数为______ 。
(1)Fe2+易被人体吸收,医生建议在服用补铁剂时,同时服用维生素C.维生素C的作用是
(2)印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的离子方程式:
(3)某废料铁泥的主要成分为Fe2O3、FeO、Fe和杂质(杂质不与硫酸反应)。现取wg废料铁泥提取Fe2O3,设计实验流程如下:

①分离溶液A和沉淀C的实验操作为
②能检验溶液A中含有Fe2+的试剂是
A.铁粉 B.酸性KMnO4溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为
④若最终获得ngFe2O3,则废料铁泥中铁元素的质量分数为
您最近一年使用:0次



