1 . 碘是一种紫黑色固体,微溶于水,碘单质及碘的化合物被广泛用于医疗、染料等方面。一种以海水为原料制备碘单质的方法如图所示。
(1)将海水中的 “富集”得到悬浊液,有关反应的离子方程式是
“富集”得到悬浊液,有关反应的离子方程式是________ 。
(2)“转化”时用铁粉而不用铁片的原因是________ 。 进入“氧化”环节,通入
进入“氧化”环节,通入 的过程中,若氧化产物只有一种,反应的化学方程式为
的过程中,若氧化产物只有一种,反应的化学方程式为________ ;若反应物用量比 时,氧化产物为
时,氧化产物为________ ;
(3)欲判断经一系列处理后的水溶液中是否含有 ,应进行的操作是
,应进行的操作是________ 。
(4)成品中 的含量可以用“碘量法”测得。称取mg样品,置于碘量瓶中,移取
的含量可以用“碘量法”测得。称取mg样品,置于碘量瓶中,移取 的
的 溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的
溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的 用
用 溶液除去,反应式为
溶液除去,反应式为 。测定时消耗
。测定时消耗 溶液体积VmL样品中
溶液体积VmL样品中 的含量为
的含量为________ (用质量分数表示)。

(1)将海水中的
 “富集”得到悬浊液,有关反应的离子方程式是
“富集”得到悬浊液,有关反应的离子方程式是(2)“转化”时用铁粉而不用铁片的原因是
 进入“氧化”环节,通入
进入“氧化”环节,通入 的过程中,若氧化产物只有一种,反应的化学方程式为
的过程中,若氧化产物只有一种,反应的化学方程式为 时,氧化产物为
时,氧化产物为(3)欲判断经一系列处理后的水溶液中是否含有
 ,应进行的操作是
,应进行的操作是(4)成品中
 的含量可以用“碘量法”测得。称取mg样品,置于碘量瓶中,移取
的含量可以用“碘量法”测得。称取mg样品,置于碘量瓶中,移取 的
的 溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的
溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的 用
用 溶液除去,反应式为
溶液除去,反应式为 。测定时消耗
。测定时消耗 溶液体积VmL样品中
溶液体积VmL样品中 的含量为
的含量为
您最近一年使用:0次
2 . 高纯硅制备过程中会产生副产物 ,某同学在实验室以
,某同学在实验室以 和硅镁石(含
和硅镁石(含 、
、 及少量Fe的氧化物)为原料,制备氯化镁晶体(
及少量Fe的氧化物)为原料,制备氯化镁晶体( )并回收
)并回收 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)写出 “水溶”过程中发生反应的化学方程式:
“水溶”过程中发生反应的化学方程式:_______ 。
(2)“氧化”时加 发生反应的离子方程式为
发生反应的离子方程式为_______ ,反应温度不易过高,主要原因是_______ 。
(3)试剂X的作用为“调pH”将杂质转化为沉淀而除去,同时不引入杂质,试剂X可以是下列试剂中的_______ (填字母),“调pH”的范围为_______ 。
A.NaOH B. C.
C. D.MgO
D.MgO
(4)“沉淀1”灼烧后所得固体与“沉淀2”共同用于回收 ,“沉淀1”灼烧时应在
,“沉淀1”灼烧时应在_______ (填仪器名称)中进行。
(5)若以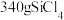 为原料,理论上制得
为原料,理论上制得 的质量为
的质量为_______ g(假设反应过程中Cl元素无损耗)。
 ,某同学在实验室以
,某同学在实验室以 和硅镁石(含
和硅镁石(含 、
、 及少量Fe的氧化物)为原料,制备氯化镁晶体(
及少量Fe的氧化物)为原料,制备氯化镁晶体( )并回收
)并回收 的工艺流程如图所示:
的工艺流程如图所示: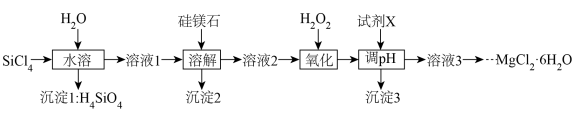
 |  | |
| 开始沉淀的pH | 2.2 | 9.6 |
| 沉淀完全的pH | 3.5 | 11.6 |
(1)写出
 “水溶”过程中发生反应的化学方程式:
“水溶”过程中发生反应的化学方程式:(2)“氧化”时加
 发生反应的离子方程式为
发生反应的离子方程式为(3)试剂X的作用为“调pH”将杂质转化为沉淀而除去,同时不引入杂质,试剂X可以是下列试剂中的
A.NaOH B.
 C.
C. D.MgO
D.MgO(4)“沉淀1”灼烧后所得固体与“沉淀2”共同用于回收
 ,“沉淀1”灼烧时应在
,“沉淀1”灼烧时应在(5)若以
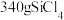 为原料,理论上制得
为原料,理论上制得 的质量为
的质量为
您最近一年使用:0次
名校
3 . 下列实验方案能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 探究浓硫酸的吸水性 | 向表面皿中加入少量 ,再加入约3mL浓硫酸,搅拌,观察实验现象 ,再加入约3mL浓硫酸,搅拌,观察实验现象 |
B | 比较浓硝酸和浓盐酸的氧化性强弱 | 室温下,在浓硝酸和浓盐酸中分别投入光亮的铁钉 |
C | 探究浓硫酸与木炭反应的气体产物中是否含有 | 将浓硫酸与木炭混合加热生成的气体通入足量澄清石灰水中,观察是否有白色沉淀产生 |
D | 检验 | 将 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-11更新
|
501次组卷
|
2卷引用:陕西省咸阳市实验中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
4 . 有关反应的离子方程式书写正确的是(均充分反应)
A.向 明矾溶液中滴入几滴 明矾溶液中滴入几滴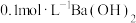 溶液: 溶液: |
B.向KI与稀硫酸的混合溶液中通入氧气: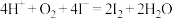 |
C. 溶液中通入 溶液中通入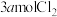 : :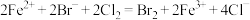 |
D.在澄清石灰水中加入少量碳酸氢镁(易溶)溶液: |
您最近一年使用:0次
名校
5 . 下列物质的应用中,利用了氧化还原反应原理的是
A. 补血剂与维生素C配合使用效果 补血剂与维生素C配合使用效果 |
| B.二氧化碳灭火 |
| C.小苏打中和胃酸 |
| D.稀硫酸除铁锈更佳 |
您最近一年使用:0次
名校
6 . 下列各组离子在强酸性条件下能大量共存的是
A.Ba2+、Na+、I-、NO | B.Ca2+、SO 、NO 、NO 、Cl- 、Cl- |
C.K+、Na+、Cl-、SO | D.NH 、Fe2+、Cl-、NO 、Fe2+、Cl-、NO |
您最近一年使用:0次
名校
解题方法
7 . 利用下列装置(夹持装置略)进行实验,下列说法不正确的是


| A.用甲装置检验H2中的HCl |
| B.用乙装置可以制取H2、CO2、SO2、NH3、NO等气体 |
| C.装置丙从FeSO4溶液中获得纯净的FeSO4固体 |
| D.甲丁所示仪器不能提纯Fe(OH)3胶体 |
您最近一年使用:0次
名校
解题方法
8 . 某兴趣小组研究铁盐的制备和性质。
实验I.制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。
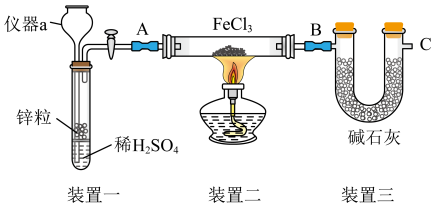
(1)仪器a的名称是_______ 。
(2)装置二中制备FeCl2的化学方程式是_____ ,装置三的作用是①_____ ;②_____ 。
(3)该装置存在一定的缺陷,可在_______ 位置(填“A”“B”或“C”)增加如下装置。如下装置中气体从_______ (填“a”或“b”)流入;洗气瓶中盛装的是_______ 。
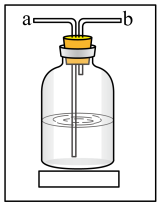
(4)为消除工业废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示处理过程的原理_______ 。
实验Ⅱ.探究性质
(5) FeCl2溶液滴加NaOH溶液后会出现灰绿色沉淀,有同学猜测灰绿色沉淀是Fe(OH)2和Fe(OH)3的混合物。为探究是否存在Fe(OH)2,可取灰绿色沉淀,向其中加入_______ 溶液,再加入_______ 溶液,若观察到_______ 现象,证明灰绿色沉淀中含有Fe(OH)2。
实验I.制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。

(1)仪器a的名称是
(2)装置二中制备FeCl2的化学方程式是
(3)该装置存在一定的缺陷,可在

(4)为消除工业废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示处理过程的原理
实验Ⅱ.探究性质
(5) FeCl2溶液滴加NaOH溶液后会出现灰绿色沉淀,有同学猜测灰绿色沉淀是Fe(OH)2和Fe(OH)3的混合物。为探究是否存在Fe(OH)2,可取灰绿色沉淀,向其中加入
您最近一年使用:0次
解题方法
9 . 下列离子方程式书写正确的是
A.硫酸铝溶液与过量氨水反应: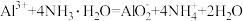 |
B. 与 与 溶液反应: 溶液反应: |
C.向次氯酸钠溶液中通入少量二氧化碳: |
D.向碘化亚铁溶液中通入过量氯气: |
您最近一年使用:0次
10 . 铁矿(主要成分为FeS2)在酸性条件和催化剂作用下,可发生如图所示的转化。下列说法错误的是
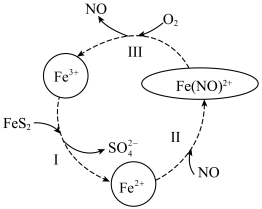

| A.反应Ⅰ、Ⅱ、Ⅲ均属于氧化还原反应 |
B.反应Ⅰ的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2 +16H+ +16H+ |
| C.反应Ⅲ中氧化剂与还原剂的物质的量比为1∶4 |
| D.该过程中Fe3+、NO是催化剂 |
您最近一年使用:0次

 固体是否氧化变质
固体是否氧化变质

