名校
解题方法
1 . 设计如图所示装置回收金属钴。保持细菌所在环境的pH稳定,借助细菌降解乙酸盐生成 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料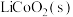 转化为
转化为 。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
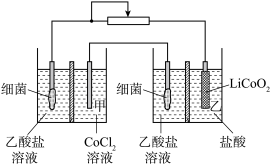
 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料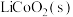 转化为
转化为 。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
| A.装置工作时,甲室溶液的pH逐渐减小 |
B.乙室电极反应式为 |
| C.为了保持细菌所在环境的pH稳定,两侧都应选择阳离子交换膜 |
D.若甲室 减少150mg,乙室 减少150mg,乙室 增加300mg,则此时已进行过溶液转移 增加300mg,则此时已进行过溶液转移 |
您最近一年使用:0次
2024-01-06更新
|
411次组卷
|
2卷引用:辽宁省盘锦市高级中学2023-2024学年高二上学期12月阶段联考化学试卷
名校
2 . 用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.常温下,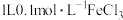 溶液中,所含 溶液中,所含 总数为 总数为 |
B. 溶液中含有的 溶液中含有的 数为 数为 |
C.向 溶液中滴入适量氨水至中性,此时溶液中所含 溶液中滴入适量氨水至中性,此时溶液中所含 的数目为 的数目为 |
D.在钢铁吸氧腐蚀中,若生成 ,被还原的 ,被还原的 分子数为 分子数为 |
您最近一年使用:0次
3 . 化学与生活关系密切,下列说法错误的是
A.在 和 和 的平衡体系中,加压后颜色变深可用勒夏特列原理解释 的平衡体系中,加压后颜色变深可用勒夏特列原理解释 |
| B.需要加热才能进行的化学反应不一定是吸热反应 |
| C.打开剧烈摇动后的碳酸饮料会产生大量气泡的原因可以用压强对化学平衡的影响解释 |
| D.用外加电流法防止钢铁腐蚀需附加惰性电极作阳极 |
您最近一年使用:0次
名校
解题方法
4 . 乙烯是一种重要的化工原料,具有广阔的开发和应用前景。
(1)常温常压下:①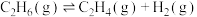
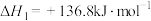
②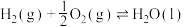
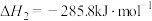
③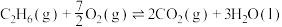

则表征 燃烧热的热化学方程式为
燃烧热的热化学方程式为__________ 。
利用 和
和 合成乙烯:
合成乙烯: 。
。
(2)在恒容密闭容器中,起始压强相同,反应温度、投料比[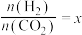 ]对
]对 平衡转化率的影响如图1所示。M、N两点的化学平衡常数
平衡转化率的影响如图1所示。M、N两点的化学平衡常数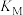
__________ (填“>”或“<”)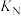 。
。

(3)300℃时,向1L恒容密闭容器中通入 、
、 ,平衡时
,平衡时 转化率为50%,
转化率为50%,
__________ (结果保留两位有效数字)。
根据如图2所示装置完成下列问题:

(4)乙烯燃料电池的负极上发生的反应为__________ 。
(5)写出乙池中电解的总反应的化学方程式:__________ 。
(6)甲池中消耗224mL(标准状况下) ,此时丙池中理论上最多产生
,此时丙池中理论上最多产生__________ g沉淀,此时乙池中溶液的体积为400mL,该溶液的
__________  。
。
(7)若以该乙烯燃料电池为电源,用石墨作电极电解200mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),电路中转移的电子的物质的量是__________ mol。
(1)常温常压下:①
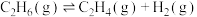
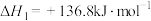
②
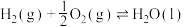
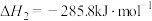
③
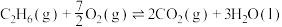

则表征
 燃烧热的热化学方程式为
燃烧热的热化学方程式为利用
 和
和 合成乙烯:
合成乙烯: 。
。(2)在恒容密闭容器中,起始压强相同,反应温度、投料比[
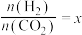 ]对
]对 平衡转化率的影响如图1所示。M、N两点的化学平衡常数
平衡转化率的影响如图1所示。M、N两点的化学平衡常数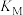
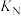 。
。
(3)300℃时,向1L恒容密闭容器中通入
 、
、 ,平衡时
,平衡时 转化率为50%,
转化率为50%,
根据如图2所示装置完成下列问题:

(4)乙烯燃料电池的负极上发生的反应为
(5)写出乙池中电解的总反应的化学方程式:
(6)甲池中消耗224mL(标准状况下)
 ,此时丙池中理论上最多产生
,此时丙池中理论上最多产生
 。
。(7)若以该乙烯燃料电池为电源,用石墨作电极电解200mL含有如下离子的溶液。
离子 |
|
|
|
|
| 0.5 | 2 | 2 | 0.5 |
您最近一年使用:0次
名校
解题方法
5 . 由菱锰矿(主要成分为 ,还含有少量Si、Fe、Ni等元素)制备一种新型锂电池的正极材料(
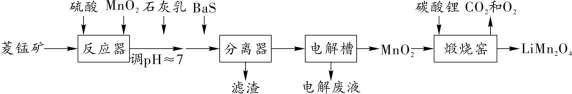
,还含有少量Si、Fe、Ni等元素)制备一种新型锂电池的正极材料( )的工艺流程如图所示:
)的工艺流程如图所示:
已知:① ,
, ,
,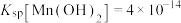 ,
, ,
,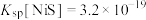 。
。
②当溶液中离子浓度小于 时,可视为沉淀完全。
时,可视为沉淀完全。
③BaS可溶于水。
(1)为提高反应器中的溶矿速率,可采取的措施有__________ (写一条)。
(2)加入少量 的目的是氧化
的目的是氧化 ,实际生产中不用
,实际生产中不用 替代
替代 的原因是
的原因是__________ 。
(3)溶矿反应完成后,先向反应后的溶液中加入石灰乳至溶液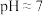 ,再加BaS进一步除去
,再加BaS进一步除去 。加石灰乳调节溶液pH时,不直接将
。加石灰乳调节溶液pH时,不直接将 完全沉淀为
完全沉淀为 的原因是
的原因是__________ 。
(4)若分离后的溶液中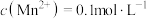 ,要使
,要使 完全除尽,则需控制
完全除尽,则需控制 的范围为
的范围为__________ ;生产中也可用__________ (填化学式)代替BaS除去 ,同时还可以增加
,同时还可以增加 产量。
产量。
(5)在电解槽中,发生电解反应的离子方程式为__________ 。
(6)高温煅烧时,生成 的化学方程式为
的化学方程式为__________ 。
 ,还含有少量Si、Fe、Ni等元素)制备一种新型锂电池的正极材料(
,还含有少量Si、Fe、Ni等元素)制备一种新型锂电池的正极材料( )的工艺流程如图所示:
)的工艺流程如图所示:
已知:①
 ,
, ,
,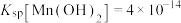 ,
, ,
,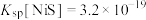 。
。②当溶液中离子浓度小于
 时,可视为沉淀完全。
时,可视为沉淀完全。③BaS可溶于水。
(1)为提高反应器中的溶矿速率,可采取的措施有
(2)加入少量
 的目的是氧化
的目的是氧化 ,实际生产中不用
,实际生产中不用 替代
替代 的原因是
的原因是(3)溶矿反应完成后,先向反应后的溶液中加入石灰乳至溶液
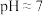 ,再加BaS进一步除去
,再加BaS进一步除去 。加石灰乳调节溶液pH时,不直接将
。加石灰乳调节溶液pH时,不直接将 完全沉淀为
完全沉淀为 的原因是
的原因是(4)若分离后的溶液中
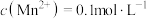 ,要使
,要使 完全除尽,则需控制
完全除尽,则需控制 的范围为
的范围为 ,同时还可以增加
,同时还可以增加 产量。
产量。(5)在电解槽中,发生电解反应的离子方程式为
(6)高温煅烧时,生成
 的化学方程式为
的化学方程式为
您最近一年使用:0次
名校
6 . 我们的日常生产、生活与化学有着紧密的联系。
Ⅰ.已知次磷酸( )是一元中强酸,请回答:
)是一元中强酸,请回答:
(1)写出其正盐在水溶液中水解的离子方程式:__________ 。
Ⅱ.现有常温下 的盐酸溶液和
的盐酸溶液和 的醋酸溶液,请根据下列操作回答问题:
的醋酸溶液,请根据下列操作回答问题:
(2)①常温下, 溶液加水稀释,下列数值增大的是
溶液加水稀释,下列数值增大的是__________ (填字母)。
A. B.
B. C.
C. D.
D.
②取10mL醋酸溶液,加入少量无水 固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将__________ (填“增大”“减小”或“不变”)。
③相同条件下,取等体积的盐酸溶液和醋酸溶液,分别与0.1mol/LNaOH溶液恰好反应,消耗NaOH溶液的体积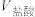
__________ (填“>”“<”或“=”)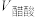 。
。
(3)某温度下,测得 的HCl溶液中,水电离出的氢离子的浓度
的HCl溶液中,水电离出的氢离子的浓度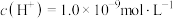 ,此温度下,将
,此温度下,将 盐酸溶液和
盐酸溶液和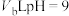 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
__________ 。(忽略混合后溶液体积变化)
Ⅲ.25℃时,有浓度均为0.10mol/L的下列4种溶液及几种酸的电离平衡常数:
①NaCN溶液②NaOH溶液③ 溶液④
溶液④ 溶液
溶液
(4)这4种溶液的pH由大到小的顺序是__________ (填序号)。
(5)向NaCN溶液中通入少量 ,则发生反应的离子方程式为
,则发生反应的离子方程式为__________ 。
(6)测得HCN和NaCN的混合溶液的 ,则
,则 约为
约为__________ (保留1位有效数字)。
(7) 和
和 混合溶液中,若溶液
混合溶液中,若溶液 ,则溶液中
,则溶液中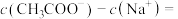
__________ (填精确值)mol/L。
Ⅰ.已知次磷酸(
 )是一元中强酸,请回答:
)是一元中强酸,请回答:(1)写出其正盐在水溶液中水解的离子方程式:
Ⅱ.现有常温下
 的盐酸溶液和
的盐酸溶液和 的醋酸溶液,请根据下列操作回答问题:
的醋酸溶液,请根据下列操作回答问题:(2)①常温下,
 溶液加水稀释,下列数值增大的是
溶液加水稀释,下列数值增大的是A.
 B.
B. C.
C. D.
D.
②取10mL醋酸溶液,加入少量无水
 固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将③相同条件下,取等体积的盐酸溶液和醋酸溶液,分别与0.1mol/LNaOH溶液恰好反应,消耗NaOH溶液的体积
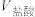
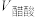 。
。(3)某温度下,测得
 的HCl溶液中,水电离出的氢离子的浓度
的HCl溶液中,水电离出的氢离子的浓度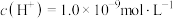 ,此温度下,将
,此温度下,将 盐酸溶液和
盐酸溶液和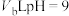 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
Ⅲ.25℃时,有浓度均为0.10mol/L的下列4种溶液及几种酸的电离平衡常数:
①NaCN溶液②NaOH溶液③
 溶液④
溶液④ 溶液
溶液HCN |
|
|
|
|
|
(5)向NaCN溶液中通入少量
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为(6)测得HCN和NaCN的混合溶液的
 ,则
,则 约为
约为(7)
 和
和 混合溶液中,若溶液
混合溶液中,若溶液 ,则溶液中
,则溶液中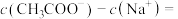
您最近一年使用:0次
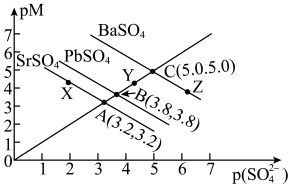
7 . T℃下,三种硫酸盐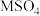 (M表示
(M表示 或
或 或
或 )的沉淀溶解平衡曲线如图所示。已知
)的沉淀溶解平衡曲线如图所示。已知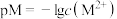 ,
, 。下列说法正确的是
。下列说法正确的是
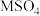 (M表示
(M表示 或
或 或
或 )的沉淀溶解平衡曲线如图所示。已知
)的沉淀溶解平衡曲线如图所示。已知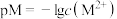 ,
, 。下列说法正确的是
。下列说法正确的是
A.Y点对应的是 的过饱和溶液,不能继续溶解 的过饱和溶液,不能继续溶解 |
B.X点和Z点分别是 和 和 的饱和溶液,对应的溶液中 的饱和溶液,对应的溶液中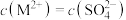 |
C.在T℃时,用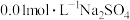 溶液滴定20mL等体积、浓度均为 溶液滴定20mL等体积、浓度均为 的 的 和 和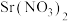 的混合溶液, 的混合溶液, 先沉淀 先沉淀 |
D.T℃下,反应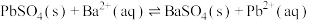 的平衡常数为 的平衡常数为 |
您最近一年使用:0次
名校
解题方法
8 . 400℃时,向容积为2L的密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测得的部分数据见下表:
。反应过程中测得的部分数据见下表:
下列说法中,正确的是
 ,发生如下反应:
,发生如下反应: 。反应过程中测得的部分数据见下表:
。反应过程中测得的部分数据见下表:
| 0 | 10 | 20 | 30 |
| 0.10 | 0.04 | 0.02 | |
| 0.20 | 0.04 |
A.反应在前10min内的平均速率为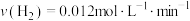 |
B.保持其他条件不变,再向平衡体系中同时通入物质的量均为0.08mol的CO、 和 和 ,则达到新平衡前 ,则达到新平衡前 |
C.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的 |
D.保持其他条件不变,起始时向容器中充入0.05molCO和 ,达到平衡时, ,达到平衡时,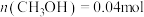 |
您最近一年使用:0次
名校
解题方法
9 . 如图所示为不同温度下水的电离平衡曲线,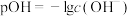 ,下列说法正确的是
,下列说法正确的是

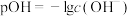 ,下列说法正确的是
,下列说法正确的是
A. 和 和 的关系是 的关系是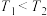 |
| B.A点到D点:加入少量碱可实现 |
C. 的关系是 的关系是 |
D. 时, 时, 的硫酸与 的硫酸与 的NaOH溶液等体积混合,溶液呈中性 的NaOH溶液等体积混合,溶液呈中性 |
您最近一年使用:0次
名校
解题方法
10 . 下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 证明 溶液中存在 溶液中存在 的水解平衡 的水解平衡 | 向含有酚酞的 |
B | 制得 | 将 |
C | 比较盐酸和醋酸的酸性强弱 | 相同温度下,用pH计分别测定 盐酸溶液和 盐酸溶液和 醋酸溶液的pH 醋酸溶液的pH |
D | 探究温度对反应速率的影响 | 向2支试管中各加入相同体积、相同浓度的 溶液,再分别加入相同体积、相同浓度的稀硫酸,分别放入冷水和热水中 溶液,再分别加入相同体积、相同浓度的稀硫酸,分别放入冷水和热水中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次





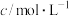


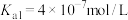
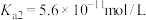
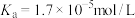


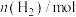
 溶液,观察溶液颜色的变化
溶液,观察溶液颜色的变化 固体
固体

