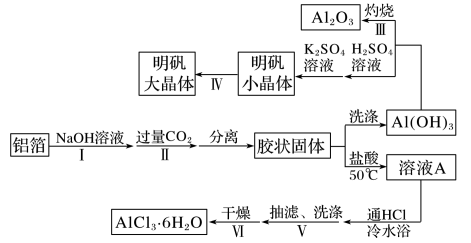
1 . 某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下:
请回答:
(1)步骤Ⅰ中的化学方程式______________________________________ 。步骤Ⅱ中生成Al(OH)3的离子方程式________________________________________ 。
(2)步骤Ⅲ,下列操作合理的是______________________ 。
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序_______________ 。
①迅速降至室温 ②用玻璃棒摩擦器壁③配制90℃的明矾饱和溶液 ④自然冷却至室温
⑤选规则明矾小晶体并悬挂在溶液中央⑥配制高于室温10~20℃的明矾饱和溶液
(4)由溶液A制备AlCl3·6H2O的装置如图:________________ 。
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是____________________________ ;
洗涤时,合适的洗涤剂是______________________ 。
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是___________________ 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| 溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)步骤Ⅰ中的化学方程式
(2)步骤Ⅲ,下列操作合理的是
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序
①迅速降至室温 ②用玻璃棒摩擦器壁③配制90℃的明矾饱和溶液 ④自然冷却至室温
⑤选规则明矾小晶体并悬挂在溶液中央⑥配制高于室温10~20℃的明矾饱和溶液
(4)由溶液A制备AlCl3·6H2O的装置如图:
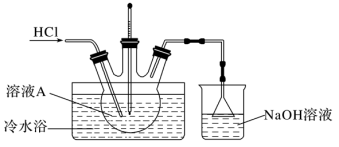
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是
洗涤时,合适的洗涤剂是
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是
您最近一年使用:0次
2017-11-06更新
|
4641次组卷
|
6卷引用:吉林省通化县综合高级中学2021-2022学年高三上学期第一次模拟考试化学试题
吉林省通化县综合高级中学2021-2022学年高三上学期第一次模拟考试化学试题浙江省2017年11月普通高校招生选考科目考试化学试题2017年11月浙江省普通高校招生选考科目考试化学试题2019届高三化学镁、铝及其化合物一轮复习针对训练题(已下线)专题21.化学工艺流程分析-十年(2012-2021)高考化学真题分项汇编(浙江专用)江西省宁冈中学2021-2022学年高三上学期9月份开学考化学试题
2 . 亚硝酸钠是重要的防腐剂.某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠.(夹持装置和A中加热装置已略,气密性已检验) 
查阅资料:①HNO2为弱酸,室温下存在反应3HNO2═HNO3+2NO↑+H2O;
②NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸。
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热。
(1)A中反应的化学方程式是_________________________________________ 。
(2)B中观察到的主要现象是_______________________ 。D装置的作用是___________________ 。
(3)实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是________ 。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸溶液pH=1
c.0.1mol/L亚硝酸钠溶液中存在:c(Na+)+c(H+)=c(NO2﹣)+c(OH﹣)
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2﹣)>c(Na+)>c(OH﹣)>c(H+)

查阅资料:①HNO2为弱酸,室温下存在反应3HNO2═HNO3+2NO↑+H2O;
②NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸。
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热。
(1)A中反应的化学方程式是
(2)B中观察到的主要现象是
(3)实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸溶液pH=1
c.0.1mol/L亚硝酸钠溶液中存在:c(Na+)+c(H+)=c(NO2﹣)+c(OH﹣)
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2﹣)>c(Na+)>c(OH﹣)>c(H+)
您最近一年使用:0次
2018-01-13更新
|
119次组卷
|
2卷引用:吉林省辽源市田家炳高级中学等五校2018届高三上学期期末联考化学试题
3 . 锡为第IVA族具有可变价的金属元素,其单质沸点为2260℃。四氯化锡(SnCl4)是无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备SnCl4 (夹持装置已略去)。

(1)仪器C的名称为___________ ,装置乙中的试剂是_____________ 。
(2)装置甲中发生反应的化学方程式为___________________________________ 。
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是_____________ 。
(4)你认为该实验装置需要进行的改进是:__________________________________________ 。
(5)用下列方法和步骤测定所用金属锡样品的纯度(杂质不参加反应)
①将2.000g锡完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液,最后得100.00mL 溶液。写出第二步反应的离子方程式:_____________________________ 。
②取①所得溶液amL用0.100 mol·L-1 的K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+ 14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
K2Cr2O7溶液应注入到____ 式(填"酸或碱”) 滴定管中。到达滴定终点时用去bmL。则样品中锡的质量分数为_______ %(用含a、b 的最简代数式表示)。

(1)仪器C的名称为
(2)装置甲中发生反应的化学方程式为
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是
(4)你认为该实验装置需要进行的改进是:
(5)用下列方法和步骤测定所用金属锡样品的纯度(杂质不参加反应)
①将2.000g锡完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液,最后得100.00mL 溶液。写出第二步反应的离子方程式:
②取①所得溶液amL用0.100 mol·L-1 的K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+ 14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
K2Cr2O7溶液应注入到
您最近一年使用:0次
2017-12-25更新
|
283次组卷
|
2卷引用:吉林省(双辽市一中、长岭县一中、大安市一中、通榆县一中)2022届高三上学期摸底联考理综化学试题
名校
解题方法
4 . (1)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867.0kJ·mol-1
2NO2(g) N2O4(g) △H=-56.9kJ·mol-1
N2O4(g) △H=-56.9kJ·mol-1
H2O(g)=H2O(l) △H=-44.0kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式______________
(2)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:请回答下列问题:甲烷燃料电池的负极反应式是_______________
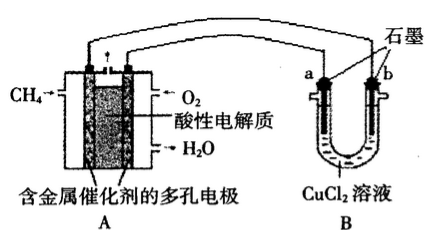
电解法制备高铁酸钾时铁和石墨分别做两个电极的电极材料,氢氧化钠溶液做电解液实现电解制备。写出阳极的电极反应式为____________________________ 。
2NO2(g)
 N2O4(g) △H=-56.9kJ·mol-1
N2O4(g) △H=-56.9kJ·mol-1H2O(g)=H2O(l) △H=-44.0kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式
(2)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:请回答下列问题:甲烷燃料电池的负极反应式是

电解法制备高铁酸钾时铁和石墨分别做两个电极的电极材料,氢氧化钠溶液做电解液实现电解制备。写出阳极的电极反应式为
您最近一年使用:0次
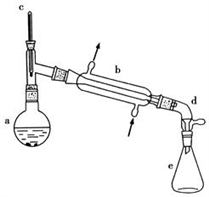
5 . 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:

可能用到的有关数据如下:
(1)合成反应:在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
(2)分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置b的名称____________
(2)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_________ (填正确答案标号)
A.立刻补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为_______________________
(4)在本实验的分离过程中,产物应从分液漏斗的_________________ (填“上口倒出”或“下口倒出”)
(5)分离提纯过程中加入无水氯化钙的目的是________________________
(6)在蒸馏收集产品时, 控制的温度应在____________ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是______________ (填序号)
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出


可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
(2)分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置b的名称
(2)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是
A.立刻补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为
(4)在本实验的分离过程中,产物应从分液漏斗的
(5)分离提纯过程中加入无水氯化钙的目的是
(6)在蒸馏收集产品时, 控制的温度应在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
您最近一年使用:0次
2018-01-12更新
|
134次组卷
|
2卷引用:吉林省长春市田家炳实验中学2017-2018学年高二上学期期末考试化学试题
6 . 阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

制备基本操作流程如下:

主要试剂和产品的物理常数如下表所示:
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是________________________________ 。
(2)合成阿司匹林时,最合适 的加热方法是______________________ 。

(3)提纯粗产品流程如下,加热回流装置如图:

①沸石的作用是__________________________________ ;
②冷凝水的流出方向是________________ (填“b”或“c”);
③使用温度计的目的是_____________________________________________________ 。
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(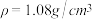 ),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为
),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为__________________ (用百分数表示,小数点后一位)。
 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
制备基本操作流程如下:

主要试剂和产品的物理常数如下表所示:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是
(2)合成阿司匹林时,

(3)提纯粗产品流程如下,加热回流装置如图:

①沸石的作用是
②冷凝水的流出方向是
③使用温度计的目的是
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(
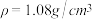 ),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为
),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为
您最近一年使用:0次
7 . 一氧化氮与过氧化钠反应可以制备亚硝酸钠,反应方程式为:2NO+Na2O2→2NaNO2 。一氧化氮可由木炭、浓硝酸、水和铜为原料制备。实验装置图下图所示(部分夹持装置略)。
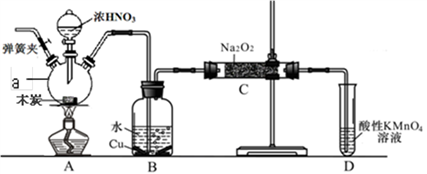


已知:室温下,①3NaNO2+3HCl→3NaCl+HNO3+2NO↑+H2O;
②酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
完成下列填空:
(1)仪器a的名称_________ ;
(2)写出浓硝酸与木炭反应的化学方程式___________________________________ 。
(3)B中观察到的主要现象是_____________________________________________ 。
(4)D装置的作用是______________________________ ;D中发生反应的离子方程式____________ 。
(5)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和______ ,为避免产生这些副产物应在B、C装置间增加装置_______ (填入“E”或“F”)



已知:室温下,①3NaNO2+3HCl→3NaCl+HNO3+2NO↑+H2O;
②酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
完成下列填空:
(1)仪器a的名称
(2)写出浓硝酸与木炭反应的化学方程式
(3)B中观察到的主要现象是
(4)D装置的作用是
(5)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和
您最近一年使用:0次
名校
8 . 某实验小组利用下图所示装置制取氨气。请回答下列问题:

(1)实验室制备氨气的化学方程式是__________________
(2)请指出装置中的两处错误
①_______________________
②_______________________ 。
(3)检验试管中收集满氨气的方法是__________________
(4)用下列装置吸收多余的氨气,最合理的是_____ 。


(1)实验室制备氨气的化学方程式是
(2)请指出装置中的两处错误
①
②
(3)检验试管中收集满氨气的方法是
(4)用下列装置吸收多余的氨气,最合理的是

您最近一年使用:0次
2017-11-03更新
|
177次组卷
|
3卷引用:吉林省长春外国语学校2017-2018学年高二上学期期中考试(文)化学试题
名校
9 . 下列装置及药品和实验室制备的气体相匹配的是
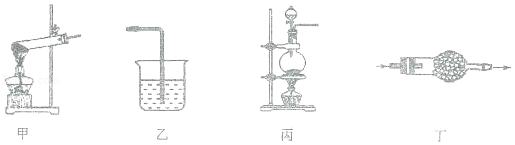
| A.甲装置用来制备氧气 | B.乙装置用来尾气处理氯化氢气体 |
| C.丙装置用来制取氯气 | D.丁装置中盛有碱石灰用来干燥二氧化碳气体 |
您最近一年使用:0次
2017-12-02更新
|
359次组卷
|
9卷引用:【全国百强校】吉林省长春市第十一高中2018-2019学年高一上学期期末考试化学试题
【全国百强校】吉林省长春市第十一高中2018-2019学年高一上学期期末考试化学试题上海交通大学附属中学2017-2018学年高一上学期期中考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高一下学期开学考试化学试题上海交大附中2017-2018学年高一(上)期中化学试卷安徽省滁州市定远县炉桥中学2019—2020学年高一上学期期末检测化学试题河北省石家庄市第二十三中学2020-2021学年高一上学期12月阶段考试化学试题河北省石家庄市第二十三中学2020-2021学年高一上学期第三次月考化学试题湖北省武汉市青山区2021-2022学年高一上学期期末考试化学试题湖北省襄阳市第五中学2022-2023学年高一上学期12月月考化学试题
10 . 实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
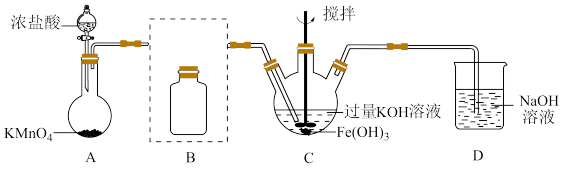
①A为氯气发生装置。A中反应方程式是________________ (锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。_______
③C中得到紫色固体和溶液,C中Cl2发生的反应有
3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl+8H2O,另外还有
2K2FeO4+6KCl+8H2O,另外还有________________ 。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________ 产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2________  (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是________________ 。
③资料表明,酸性溶液中的氧化性 >
> ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
> 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:________________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应方程式是
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液,C中Cl2发生的反应有
3Cl2+2Fe(OH)3+10KOH
 2K2FeO4+6KCl+8H2O,另外还有
2K2FeO4+6KCl+8H2O,另外还有(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性
 >
> ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
> 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次
2018-06-09更新
|
9680次组卷
|
31卷引用:吉林省吉林市第五十五中学2018-2019学年高二下学期期末考试化学试题
吉林省吉林市第五十五中学2018-2019学年高二下学期期末考试化学试题2018年全国普通高等学校招生统一考试化学(北京卷)(已下线)2018年高考题及模拟题汇编 专题16 化学实验综合题(已下线)高考母题题源18 化学实验设计与探究(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第3讲 铁及其化合物 (教学案)(已下线)2019年高考总复习巅峰冲刺-专题03 氧化还原反应 离子反应应试策略(已下线)《2019年高考总复习巅峰冲刺》专题10 化学实验基础应试策略(已下线)专题10.3 化学实验方案的设计与评价 (讲)-《2020年高考一轮复习讲练测》宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题(已下线)专题3.3 铁及其重要化合物(讲)——2020年高考化学一轮复习讲练测(已下线)专题3.3 铁及其重要化合物(练)——2020年高考化学一轮复习讲练测(已下线)第11讲 铁及其重要化合物(精讲)——2021年高考化学一轮复习讲练测(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精讲)——2021年高考化学一轮复习讲练测高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 高考帮人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 高考帮河南省洛阳市第一高级中学2021届高三上学期10月月考化学试题(已下线)易错22 气体实验装置的设计-备战2021年高考化学一轮复习易错题(已下线)专题讲座(九) 热点实验综合探究 (精练)-2021年高考化学一轮复习讲练测(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第7讲 铁及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向14 物质制备探究-备战2022年高考化学一轮复习考点微专题四川省遂宁市射洪中学2021-2022学年高一下学期第一次月考化学试题(强基班)(已下线)第07讲 铁及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第28讲 定性、定量实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)天津市耀华中学2023届高三第一次统练化学试题云南省玉溪市华宁县第二中学2021-2022年高一下学期开学考试化学试题第三章 金属及其化合物 第14讲 铁及其化合物的转化关系(已下线)第一部分 化学综合实验 热点6 物质性质探究实验北京一零一中学2023-2024学年高一上学期11月统练三化学试卷河北省石家庄二中实验学校2023-2024学年高一上学期12月月考化学试题



