名校
解题方法
1 . 实现下列变化时,需要克服相同类型作用力的是
| A.金刚石和干冰的熔化 | B.食盐和醋酸钠的熔化 |
| C.液溴和液汞的汽化 | D. 和 和 溶于水 溶于水 |
您最近一年使用:0次
名校
2 . 长式周期表共有18个纵行,从左到右排为1-18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是
| A.第9列元素中有非金属元素 | B.只有第二列的元素原子最外层电子排布为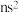 |
C.第四周期第12列元素是 元素 元素 | D.第15列元素原子的最外层电子排布为 |
您最近一年使用:0次
名校
解题方法
3 . 锰元素在一些有机物的氧化过程中会以中间体形式出现一种美丽的亮蓝色离子MnO (次锰酸根离子)。工业上可用低品位锰矿(主要成分MnO2,含Fe、Al、Ni等元素的杂质)与废FeSO4经过一系列转化得到高品位MnO2,同时继续制备次锰酸盐,流程如下:
(次锰酸根离子)。工业上可用低品位锰矿(主要成分MnO2,含Fe、Al、Ni等元素的杂质)与废FeSO4经过一系列转化得到高品位MnO2,同时继续制备次锰酸盐,流程如下:
(1)次锰酸根离子MnO 中Mn的化合价为
中Mn的化合价为___________ 。
(2)“焙烧”过程中的氧化剂为___________ 、___________ (填化学式)。
(3)“除铝”过程中的离子方程式为___________ 。
(4)“滤渣2”的主要成分为___________ 、___________ (填化学式)。
(5)“沉锰”时,Mn2+会转化为MnCO3.若常温下控制溶液pH=8,且最终c(HCO )=0.1 mol·L-1,则此时溶液中c(Mn2+)=
)=0.1 mol·L-1,则此时溶液中c(Mn2+)=___________ mol·L-1。
(6)在“共熔”过程中,需要向煅烧后产生的MnO2固体中添加一定比例的NaNO3、NaOH,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为___________ 。
 (次锰酸根离子)。工业上可用低品位锰矿(主要成分MnO2,含Fe、Al、Ni等元素的杂质)与废FeSO4经过一系列转化得到高品位MnO2,同时继续制备次锰酸盐,流程如下:
(次锰酸根离子)。工业上可用低品位锰矿(主要成分MnO2,含Fe、Al、Ni等元素的杂质)与废FeSO4经过一系列转化得到高品位MnO2,同时继续制备次锰酸盐,流程如下: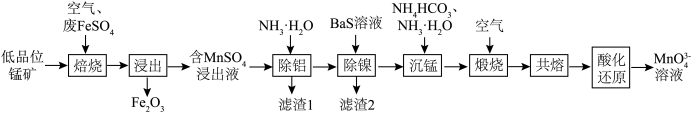
| 物质 | MnCO3 | H2CO3 |
| 25℃数值 | Ksp=2.0×10-11 | Ka1=4×10-7 Ka2=5×10-11 |
(1)次锰酸根离子MnO
 中Mn的化合价为
中Mn的化合价为(2)“焙烧”过程中的氧化剂为
(3)“除铝”过程中的离子方程式为
(4)“滤渣2”的主要成分为
(5)“沉锰”时,Mn2+会转化为MnCO3.若常温下控制溶液pH=8,且最终c(HCO
 )=0.1 mol·L-1,则此时溶液中c(Mn2+)=
)=0.1 mol·L-1,则此时溶液中c(Mn2+)=(6)在“共熔”过程中,需要向煅烧后产生的MnO2固体中添加一定比例的NaNO3、NaOH,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为
您最近一年使用:0次
名校
4 . 空间站处理 的一种重要方法是对
的一种重要方法是对 进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:
进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:
Ⅰ.固态胺吸收与浓缩
在水蒸气存在下固态胺吸收 反应生成酸式碳酸盐(该反应是放热反应),再解吸出
反应生成酸式碳酸盐(该反应是放热反应),再解吸出 的简单方法是加热。
的简单方法是加热。
Ⅱ. 的加氢甲烷化
的加氢甲烷化
 还原
还原 制
制 的部分反应如下:
的部分反应如下:
i.CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g) 
ii.CO(g)+3H2 CH4(g)+H2O(g)
CH4(g)+H2O(g) 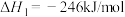
(1)反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的
CH4(g)+2H2O(g)的
___________  。
。
(2)向恒容绝热的密闭容器中充入amolCO与2amolH2,进行反应ii,下列能判断反应已达化学平衡状态的是___________ ;
a.容器中混合气体密度不变 b.混合气体中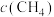 与
与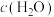 之比不变
之比不变
c.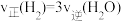 d.容器内温度不变
d.容器内温度不变
Ⅲ.和 合成甲烷也是资源化利用的重要方法。对于上述(1)的反应
合成甲烷也是资源化利用的重要方法。对于上述(1)的反应 ,催化剂的选择是甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得转化率和生成
,催化剂的选择是甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得转化率和生成 选择性随温度变化的影响如下图所示:
选择性随温度变化的影响如下图所示: 转化率仍在上升,其原因是
转化率仍在上升,其原因是___________ 。
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是___________ ,使用的合适温度为___________ 。
(5)控制起始时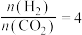 ,P=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
,P=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:___________ (填增大,减小或者不变)。
②图中代表 的曲线是
的曲线是___________ (填“a”、“b”或“c”);温度低于500℃时,CO的物质的量分数约为0,说明此条件下,反应___________ (填“i”或“ii”)化学平衡常数大,反应完全。
③反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的平衡常数
CH4(g)+2H2O(g)的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压总压物质的量分数)。
(用平衡分压代替平衡浓度计算,分压总压物质的量分数)。
 的一种重要方法是对
的一种重要方法是对 进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:
进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:Ⅰ.固态胺吸收与浓缩

在水蒸气存在下固态胺吸收
 反应生成酸式碳酸盐(该反应是放热反应),再解吸出
反应生成酸式碳酸盐(该反应是放热反应),再解吸出 的简单方法是加热。
的简单方法是加热。Ⅱ.
 的加氢甲烷化
的加氢甲烷化 还原
还原 制
制 的部分反应如下:
的部分反应如下:i.CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g) 
ii.CO(g)+3H2
 CH4(g)+H2O(g)
CH4(g)+H2O(g) 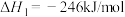
(1)反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的
CH4(g)+2H2O(g)的
 。
。(2)向恒容绝热的密闭容器中充入amolCO与2amolH2,进行反应ii,下列能判断反应已达化学平衡状态的是
a.容器中混合气体密度不变 b.混合气体中
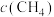 与
与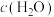 之比不变
之比不变c.
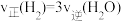 d.容器内温度不变
d.容器内温度不变Ⅲ.和
 合成甲烷也是资源化利用的重要方法。对于上述(1)的反应
合成甲烷也是资源化利用的重要方法。对于上述(1)的反应 ,催化剂的选择是甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得转化率和生成
,催化剂的选择是甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得转化率和生成 选择性随温度变化的影响如下图所示:
选择性随温度变化的影响如下图所示: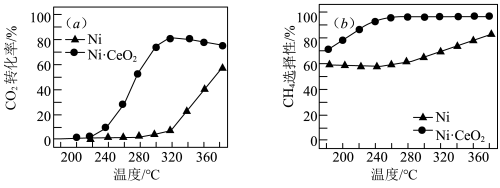
 转化率仍在上升,其原因是
转化率仍在上升,其原因是(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是
(5)控制起始时
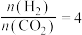 ,P=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
,P=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示: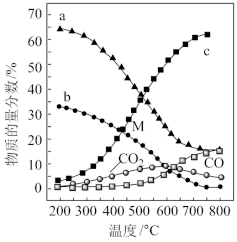
②图中代表
 的曲线是
的曲线是③反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的平衡常数
CH4(g)+2H2O(g)的平衡常数
 (用平衡分压代替平衡浓度计算,分压总压物质的量分数)。
(用平衡分压代替平衡浓度计算,分压总压物质的量分数)。
您最近一年使用:0次
2024-05-05更新
|
577次组卷
|
4卷引用:宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题
宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题(已下线)题型11 反应原理综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)提升练09 化学反应原理综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)湖南省衡阳市衡阳县第一中学2023-2024学年高三下学期4月月考化学试题
5 . 下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | CO还原Fe2O3实验中,Fe2O3是否全部被还原 | 向CO还原Fe2O3所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 |
| B | 比较CH3COO-和ClO-结合H+的能力大小 | 室温下,用pH计分别测定等物质的量浓度的CH3COONa溶液和NaClO溶液的pH |
| C | 比较Ksp(BaSO4)和Ksp (BaCO3)的相对大小 | 将BaSO4粉末和Na2CO3饱和溶液混合,充分振荡,静置,取少量上层清液,滴加盐酸和BaCl2溶液,观察是否有沉淀产生 |
| D | 检验某有机物是否为醛类 | 取少许该有机物滴入盛有银氨溶液的试管中水浴加热,观察试管中是否有银镜产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 短周期主族元素X、Y、Z、Q、R的原子序数依次增大,X的简单阴离子与锂离子具有相同的电子层结构,Y原子最外层电子数等于内层电子数的2倍,Q的单质与稀硫酸剧烈反应生成X的单质。向100mL X2R的水溶液中缓缓通入RZ2气体,溶液pH与RZ2体积关系如图。下列说法错误的是
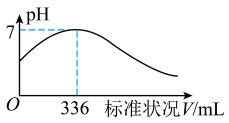
| A.单质的沸点:Q>Z>X |
| B.X2R溶液的浓度为0.3 molL-1 |
| C.最简单气态氢化物稳定性Z>Y |
| D.将RZ2分别通入BaCl2、Ba(NO3)2溶液中,均无明显现象 |
您最近一年使用:0次
名校
7 . 下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向 溶液中滴加过量的 溶液中滴加过量的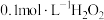 溶液 溶液 | 紫色溶液褪色 |  具有氧化性 具有氧化性 |
| B | 以 为指示剂,用 为指示剂,用 标准溶液滴定溶液中的 标准溶液滴定溶液中的 | 先出现浅黄色沉淀,后出现砖红色沉淀 | Ksp(AgBr)<Ksp(Ag2CrO4) |
| C | 压缩盛有 气体的容器体积 气体的容器体积 | 气体颜色变浅 | 加压, 平衡正向移动 平衡正向移动 |
| D | 向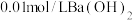 溶液中插入电导率传感器,逐滴加入 溶液中插入电导率传感器,逐滴加入 溶液 溶液 | 电导率先减小后增大 | 电导率最小时,两者恰好完全反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 化学与人类生活、社会可持续发展密切相关。下列有关说法正确的是
| A.石墨烯(由石墨剥离而成的层状结构)可用于制造超级计算机,因其具有优异的导电性能 |
| B.铝制品在空气中不易被腐蚀是因为铝的性质不活泼 |
C.福岛核电站泄漏的放射性物质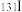 和 和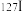 互为同位素,性质相同 互为同位素,性质相同 |
| D.回收制革工厂的边角皮料生产食用明胶,加工成医用胶囊或做食品增稠 |
您最近一年使用:0次
名校
解题方法
9 . 下列指定反应的离子方程式书写正确的是
A.将氯气通入水中: |
B. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
C. 通入酸性高锰酸钾溶液:5SO2+2 通入酸性高锰酸钾溶液:5SO2+2 +2H2O = 5 +2H2O = 5 +2Mn2++4H+ +2Mn2++4H+ |
D.向硫酸酸化的 溶液中通入O2: 溶液中通入O2: |
您最近一年使用:0次
2024-05-03更新
|
255次组卷
|
3卷引用:宁夏石嘴山市平罗中学2023-2024学年高一下学期4月月考化学试题
名校
10 . 铜及其化合物在生活、生产中用途广泛。以黄铜矿为原料冶炼铜涉及多个反应,其中一个反应为
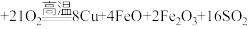 。回答下列问题:
。回答下列问题:
(1)基态铜原子的价层电子的轨道表示式(电子排布图)为___________ ,基态铜原子核外电子的空间运动状态(原子轨道)有___________ 种。
(2)高温下CuO能转化为 的原因是
的原因是___________ (从原子结构角度分析)。
(3) 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是___________ ,属于极性分子的是___________ 。
(4) 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是___________ ,1360℃是___________ 的熔点。
(5) 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为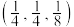 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为___________ 。晶胞参数分别为a pm,a pm、2a pm, 晶体的密度为
晶体的密度为___________  (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。

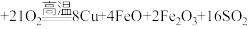 。回答下列问题:
。回答下列问题:(1)基态铜原子的价层电子的轨道表示式(电子排布图)为
(2)高温下CuO能转化为
 的原因是
的原因是(3)
 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是(4)
 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是(5)
 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为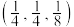 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为 晶体的密度为
晶体的密度为 (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次



