名校
1 . 如下图所示,A是酒的主要成分,D为具有果香的无色油状液体。由A到D的转化如图,请回答下列问题:___________ ,该反应类型为___________ 反应。
(2)请写出由A生成B的化学反应方程式___________ ,B中所含官能团的名称是___________ 该反应类型为___________ 反应。
(3)C的结构简式为___________ ,C与 互为
互为___________ 。
(4)写出A与C反应生成D的化学反应方程式___________ 。
(5)油脂和物质D具有相同官能团,下列物质中不属于油脂的是___________ 。

(2)请写出由A生成B的化学反应方程式
(3)C的结构简式为
 互为
互为(4)写出A与C反应生成D的化学反应方程式
(5)油脂和物质D具有相同官能团,下列物质中不属于油脂的是
| A.花生油 | B.石蜡油 | C.棉籽油 | D.牛油 |
您最近一年使用:0次
名校
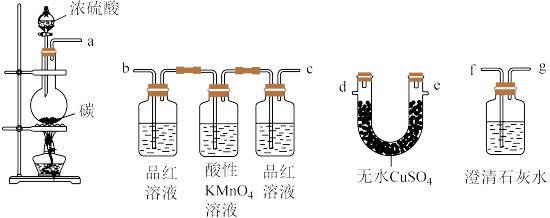
2 . 某化学兴趣小组为检验木炭和浓硫酸反应生成的产物,设计如图装置,请回答:___________ ;盛装碳粉的仪器的名称是___________ 。
(2)上述装置接口的连接顺序为a→___________ 。
(3)写出木炭和浓硫酸发生反应的化学方程式___________ 。
(4)U形管中现象是___________ ,证明产物中有___________ (填化学式)。
(5)酸性KMnO4溶液的作用是___________ 。
(6)澄清石灰水的作用是___________ 。
(7)写出SO2与酸性KMnO4反应的离子方程式___________ 。
(2)上述装置接口的连接顺序为a→
(3)写出木炭和浓硫酸发生反应的化学方程式
(4)U形管中现象是
(5)酸性KMnO4溶液的作用是
(6)澄清石灰水的作用是
(7)写出SO2与酸性KMnO4反应的离子方程式
您最近一年使用:0次
3 . 下列所述变化为吸热反应的是
A.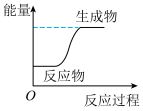 | B. | C. | D. |
您最近一年使用:0次
2024-06-18更新
|
36次组卷
|
2卷引用:宁夏回族自治区石嘴山市平罗县平罗中学2023-2024学年高一下学期5月期中化学试题
名校
解题方法
4 . 用下列装置不能达到相关实验目的的是
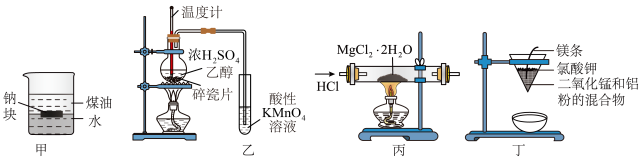
| A.用装置甲证明:ρ(煤油)<ρ(钠)<ρ(水) |
| B.利用图乙装置检验乙醇与浓硫酸共热生成了乙烯 |
| C.用装置丙制取无水MgCl2 |
| D.用装置丁制取金属锰 |
您最近一年使用:0次
名校
解题方法
5 . 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。
Ⅰ.甲醇-水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓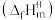 数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
则

_______  ,该反应在
,该反应在_______ (填“高温”“低温”或“任意温度”)下能自发进行。
Ⅱ.乙醇-水催化重整亦可获得,主要反应如下:
反应①: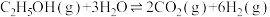
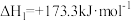
反应②:
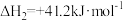
(2)向恒容密闭容器中充入1mol 和3mol
和3mol  发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时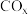 的分布分数
的分布分数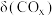 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。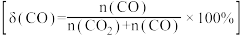
_______ (写出2条)。
②200℃以后,解释曲线a随温度变化趋势的原因:_______ 。
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内
___  ,该温度下,反应②的
,该温度下,反应②的
_______ (保留小数点后两位)。
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:_______ ,当转移1.2mol电子时,正极消耗的氧气的体积为_______ L(标准状况下)。
Ⅰ.甲醇-水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓
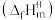 数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。| 物质 |  |  |  |  |
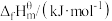 | 0 | -393.5 | -241.8 | -200.7 |


 ,该反应在
,该反应在Ⅱ.乙醇-水催化重整亦可获得,主要反应如下:
反应①:
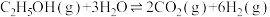
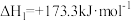
反应②:

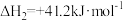
(2)向恒容密闭容器中充入1mol
 和3mol
和3mol  发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时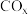 的分布分数
的分布分数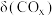 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。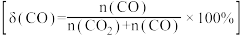

②200℃以后,解释曲线a随温度变化趋势的原因:
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内

 ,该温度下,反应②的
,该温度下,反应②的
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:

您最近一年使用:0次
2024-06-08更新
|
151次组卷
|
3卷引用:2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学
名校
解题方法
6 . Si、S、Se在自然界中形成多种多样的物质结构。回答下列问题:
(1)Se与O同族,电负性较大的是______ ;基态Se原子的价电子运动状态有____ 种。
(2)已知液态的二氧化硫可以发生类似水的自电离: 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为_______ , 的空间结构为
的空间结构为_______ 。
(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为________ ,二者中更易与 形成配位键的是
形成配位键的是________ 。 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是______ 。
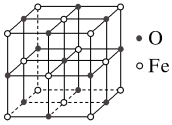
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρ g·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与O2-紧邻且等距离的Fe2+数目为______ ,Fe2+与O2-最短核间距为_____ pm。
(1)Se与O同族,电负性较大的是
(2)已知液态的二氧化硫可以发生类似水的自电离:
 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为 的空间结构为
的空间结构为(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物
 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为 形成配位键的是
形成配位键的是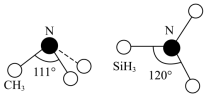
 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρ g·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与O2-紧邻且等距离的Fe2+数目为
您最近一年使用:0次
名校
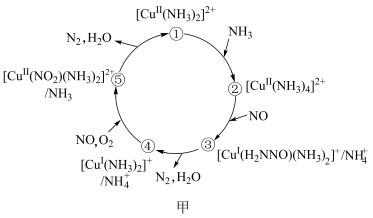
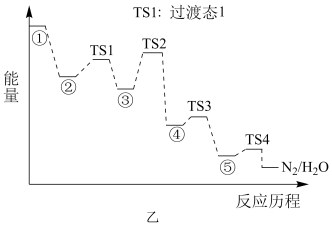
7 . 某种二价铜微粒[CuⅡ(NH3)2]2+的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
| A.升高温度,脱硝反应的正反应速率的增大程度小于逆反应速率的增大程度 |
B.该催化过程的总反应方程式为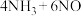  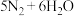 |
| C.[CuⅡ(NH3)2]2+可加快脱硝速率,提高脱硝的平衡转化率 |
| D.微粒[CuⅡ(NH3)2]2+中的NH3的键角小于氨气中NH3分子的键角 |
您最近一年使用:0次
名校
解题方法
8 . 中成药连花清瘟胶囊可用于流感的防治,其成分之一绿原酸的结构简式如下:
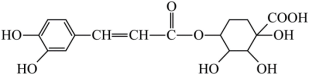
| A.苯环上的一氯代物有三种 | B.1 mol该物质最多可与4 mol氢气发生加成反应 |
| C.分子中所有碳原子可能共平面 | D.该分子含有手性碳原子 |
您最近一年使用:0次
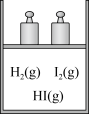
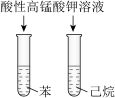
9 . 下列装置或操作能达到实验目的的是
| 选项 | A | B |
| 装置或操作 |
|
|
| 目的 | 证明氢氧化铝是两性氢氧化物 | 验证碳酸的酸性比苯酚的强 |
| 选项 | C | D |
| 装置或操作 |
|
|
| 目的 | 验证改变压强能破坏化学平衡状态 | 鉴别苯和己烷 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 水合肼(N2H4·H2O)作为一种重要的精细化工原料,主要用于合成AC、D1PA,TSH等发泡剂。工业上常用尿素[CO(NH2)2]、NaOH、NaClO溶液反应制备水合肼。
已知:①Cl2与NaOH反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3。
②N2H4·H2O沸点为118℃,具有强还原性。
回答下列问题:
Ⅰ.制备NaClO溶液(实验装置如图所示):_______ 。
(2)装置C中发生反应的离子方程式为_______ ,用冰水浴控制温度在25℃以下,其主要目的是_______ 。
Ⅱ.制备水合肼:
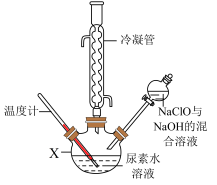
将制得的NaClO与NaOH的混合溶液滴入尿素水溶液中,在一定温度下加热,装置如图所示(夹持及控温装置已略),充分反应后,仪器X中的溶液经蒸馏获得水合肼粗品,剩余溶液再进一步处理还可获得副产品NaCl和Na2CO3·10H2O。_______ ,X中发生反应的化学方程式是_______ 。
(4)若滴加NaClO溶液的速度较快时,水合肼的产率会下降,原因是_______ 。
(5)水合肼是二元弱碱,在溶液中可发生类似NH3·H2O的电离。写出水合肼和HCl控物质的量之比为1∶1反应的离子方程式:_____ 。
(6)实验室可用碘测定水合肼的浓度,称取5.0g水合肼样品,加入适量水、稀硫酸、碳酸氢钠,配成500mL溶液,从中取出20.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.200mol·L-1I2标准溶液进行滴定,滴定终点的现象是_______ ,测得消耗标准溶液的体积为24.00mL,则样品中水合肼(N2H4·H2O)的质量分数为______ (已知:N2H4·H2O+2I2+H2SO4+6NaHCO3=N2↑+4NaI+6CO2↑+Na2SO4+7H2O)。
已知:①Cl2与NaOH反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3。
②N2H4·H2O沸点为118℃,具有强还原性。
回答下列问题:
Ⅰ.制备NaClO溶液(实验装置如图所示):
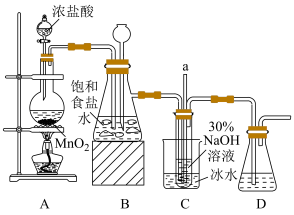
(2)装置C中发生反应的离子方程式为
Ⅱ.制备水合肼:
将制得的NaClO与NaOH的混合溶液滴入尿素水溶液中,在一定温度下加热,装置如图所示(夹持及控温装置已略),充分反应后,仪器X中的溶液经蒸馏获得水合肼粗品,剩余溶液再进一步处理还可获得副产品NaCl和Na2CO3·10H2O。
(4)若滴加NaClO溶液的速度较快时,水合肼的产率会下降,原因是
(5)水合肼是二元弱碱,在溶液中可发生类似NH3·H2O的电离。写出水合肼和HCl控物质的量之比为1∶1反应的离子方程式:
(6)实验室可用碘测定水合肼的浓度,称取5.0g水合肼样品,加入适量水、稀硫酸、碳酸氢钠,配成500mL溶液,从中取出20.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.200mol·L-1I2标准溶液进行滴定,滴定终点的现象是
您最近一年使用:0次
2024-06-02更新
|
116次组卷
|
2卷引用:2024届宁夏回族自治区石嘴山市平罗县平罗中学高三下学期模拟预测理综试题-高中化学