名校
解题方法
1 . “类推”是一种重要的学习方法,但有时会产生错误,下列类推得到的结论正确的是
| A.第二周期元素简单氢化物的稳定性顺序是HF>H2O>NH3;则第三周期元素简单氢化物的稳定性顺序也是HCl>H2S>PH3 |
| B.CO2是分子晶体;则SiO2也是分子晶体 |
| C.根据对角线规则,元素Li和Mg的某些性质相似,则元素C和P的某些性质也相似 |
D. 和P4都为正四面体形结构, 和P4都为正四面体形结构, 中键角为109°28′,P4中键角也为109°28′ 中键角为109°28′,P4中键角也为109°28′ |
您最近一年使用:0次
名校
2 . 氯气是现代工业和生活中常用的杀菌消毒剂。回答下列问题:
(1)实验室常用 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为___________ 。实验室还可用 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的___________ (选填“A”或“B”)作为发生装置,反应的离子方程式为___________ 。
(说明:试管中溶液均为 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)
①实验I中反应方程式为___________ ,由此推断氧化性:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
②实验Ⅱ中溶液变红是由于溶液中含有___________ (填微粒符号,下同);使溶液褪色的微粒是___________ 。
(1)实验室常用
 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的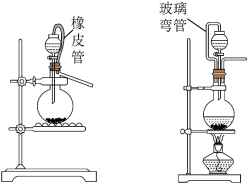
| 实验Ⅰ | 实验Ⅱ | |
| 实验操作 |
|
|
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 |
 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)①实验I中反应方程式为

 (填“
(填“ ”或“
”或“ ”)。
”)。②实验Ⅱ中溶液变红是由于溶液中含有
您最近一年使用:0次
名校
3 . 下列情景下的化学反应式书写正确的是
| A.醋酸中滴加石蕊溶液变浅红色:CH3COOH=CH3COO-+H+ |
| B.将稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| C.NaHCO3和NaOH溶液反应的离子反应方程式:H++OH-=H2O |
| D.湿法冶铜的离子反应方程式为:Fe+Cu2+=Fe2++Cu |
您最近一年使用:0次
名校
4 . 化学贯穿古今,下列对古诗词所涉及化学知识的解读不正确的是
| A.“错把陈醋当成墨,写尽半生纸上酸”,陈醋是混合物 |
| B.“熬胆矾铁斧,久之亦化为铜”,其中铜能导电,所以铜是电解质 |
| C.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”能产生丁达尔效应 |
| D.“松叶堪为酒,春来酿几多”,清香的美酒在酿制过程中发生的变化涉及电子转移 |
您最近一年使用:0次
5 . 下列说法正确的是
| A.乙醇能被CuO氧化生成乙醛,乙醛又能将新制的Cu(OH)2还原成Cu |
| B.用饱和Na2CO3溶液能鉴别乙酸乙酯、乙醇、乙酸 |
| C.可用酸性高锰酸钾溶液除去甲烷中的乙烯杂质 |
| D.油脂属于高分子化合物,是混合物,可用蒸馏的方法分离 |
您最近一年使用:0次
名校
解题方法
6 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究乙醇消去反应的产物 | 取4mL乙醇,加入12mL浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入2mL溴水中 | 若溴水褪色,则乙醇消去反应的产物为乙烯 |
| B | 探究KI与FeCl3反应的限度 | 取5mL0.1mol·L-1KI溶液于试管中,加入1mL0.1mol·L-1FeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与FeCl3的反应有一定限度 |
| C | 判断某卤代烃中的卤素 | 取2mL卤代烃样品于试管中,加入5mL20%KOH水溶液混合后加热,再滴加AgNO3溶液 | 若产生的沉淀为白色,则该卤代烃中含有氯元素 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠 | 若产生无色气体,则乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 设 表示阿伏伽德罗常数数值,下列说法错误的是
表示阿伏伽德罗常数数值,下列说法错误的是
 表示阿伏伽德罗常数数值,下列说法错误的是
表示阿伏伽德罗常数数值,下列说法错误的是A.常温下,14gC2H4和C4H8混合气体中含有极性键数目为2 |
B.1mol氨基(-NH2)中含有电子的数目为9 |
C.常温常压下,124gP4中所含P-P键数目6 |
D.标准状况下,11.2L苯中含有C-H键的数目3 |
您最近一年使用:0次
名校
8 . 下围是以氮气和氢气为原料合成氨,并以氨为原料生产硝酸的工艺流程(其中空气等基础原料已略去).________________ .
(2)若条件控制不当,氨氧化装置中可能发生副反应, 与
与 生成
生成 ,该副反应中氧化剂与还原剂的物质的量之比为
,该副反应中氧化剂与还原剂的物质的量之比为________ .
(3)下列离子能在溶液中共存,但加入适量 溶液后无法大量共存的是________.
溶液后无法大量共存的是________.
(4)将25.6g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生 和NO混合气体的体积为8.96L(标准状况,不考虑
和NO混合气体的体积为8.96L(标准状况,不考虑 二聚).待产生的气体全部释放后,向溶液加入100mL
二聚).待产生的气体全部释放后,向溶液加入100mL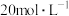 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为________  .
.
(5)可以用 还原
还原 生成BaO,该过程分两步进行.下图表示该过程相关物质浓度随时间的变化关系,第一步反应中消耗的
生成BaO,该过程分两步进行.下图表示该过程相关物质浓度随时间的变化关系,第一步反应中消耗的 与
与 的物质的量之比是
的物质的量之比是________ .

(2)若条件控制不当,氨氧化装置中可能发生副反应,
 与
与 生成
生成 ,该副反应中氧化剂与还原剂的物质的量之比为
,该副反应中氧化剂与还原剂的物质的量之比为(3)下列离子能在溶液中共存,但加入适量
 溶液后无法大量共存的是________.
溶液后无法大量共存的是________.A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
(4)将25.6g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生
 和NO混合气体的体积为8.96L(标准状况,不考虑
和NO混合气体的体积为8.96L(标准状况,不考虑 二聚).待产生的气体全部释放后,向溶液加入100mL
二聚).待产生的气体全部释放后,向溶液加入100mL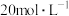 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 .
.(5)可以用
 还原
还原 生成BaO,该过程分两步进行.下图表示该过程相关物质浓度随时间的变化关系,第一步反应中消耗的
生成BaO,该过程分两步进行.下图表示该过程相关物质浓度随时间的变化关系,第一步反应中消耗的 与
与 的物质的量之比是
的物质的量之比是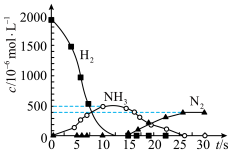
您最近一年使用:0次
解题方法
9 . 下列说法错误的是
| A.福尔马林可用于食品保鲜 | B.臭氧可用于自来水消毒 |
| C.明矾可用于净水 | D.高纯硅可用于制芯片 |
您最近一年使用:0次
解题方法
10 . 性质决定用途,用途反映性质。结合下表已知信息,下列相关叙述正确的是
| 物质及其编号 | 分子式 | 沸点/℃ | 水溶性 | |
| ① | 甘油 |  | 290 | |
| ② | 1,2-丙二醇 | 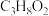 | 188 | |
| ③ | 乙醇 |  | 78 | 与水以任意比混溶 |
| ④ | 丙烷 |  | -42.1 | 难溶于水 |
| A.①②③属于饱和一元醇 |
| B.可推测出乙二醇的沸点应低于乙醇的沸点 |
| C.常温下,②在水中的溶解度较小 |
| D.醇分子之间、醇分子与水分子之间均能形成氢键 |
您最近一年使用:0次