名校
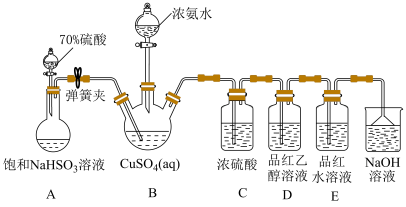
1 . NH4CuSO3(亚硫酸亚铜铵)是一种白色难溶于水、难溶于酒精的化工产品。某小组设计如下实验装置制备NH4CuSO3并探究SO2的漂白性。
ⅱ.然后向三颈烧瓶中通入SO2直至不再产生白色沉淀;
ⅲ.反应完毕后,将装置B中混合物过滤、酒精洗涤、干燥,即得成品。
已知:实验中还观察到装置D中溶液无明显现象,装置E中溶液红色褪去。
请回答下列问题:
(1)检查装置A气密性的操作方法为_____ 。
(2)装置C的目的是_____ 。
(3)实验步骤ⅱ中生成白色沉淀的离子方程式为_____ 。
(4)实验步骤ⅲ中用酒精替代水洗涤的优点是_____ 。
(5)为探究装置D、E中实验现象,化学兴趣小组对装置E中品红褪色的原因猜想如下:
猜想ⅰ:甲同学认为使品红褪色的微粒主要是 ;
;
猜想ⅱ:乙同学认为使品红褪色的微粒主要是 ;。
;。
为了验证猜想ⅰ和ⅱ,进行以下实验:
将10mL品红水溶液分成两份,在两份溶液中分别加入0.1mol·L-1的_____ 溶液(填化学式,下同)和0.1mol·L-1_____ 溶液,发现前者褪色快,后者褪色慢,说明上述猜想i比ⅱ合理。
(6)测定产品中 的含量:称取0.4200g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00mL0.1000mol·L-1H2SO4溶液全部吸收,用0.0900mol·L-1标准NaOH溶液滴定过量的H2SO4,消耗NaOH溶液22.00mL,则样品中NH4CuSO3的质量分数是
的含量:称取0.4200g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00mL0.1000mol·L-1H2SO4溶液全部吸收,用0.0900mol·L-1标准NaOH溶液滴定过量的H2SO4,消耗NaOH溶液22.00mL,则样品中NH4CuSO3的质量分数是_____ %(结果保留三位有效数字)。下列操作使测得的NH4CuSO3质量分数偏大的为_____ (填字母)。
a.滴定前仰视滴定管读数,滴定后读数正确
b.NaOH标准溶液使用前敞口放置于空气中一段时间
c.滴定结束读数时,发现滴定管尖嘴处还悬有一滴标准氢氧化钠溶液
d.用H2SO4溶液吸收NH3操作缓慢,导致部分NH3外逸到空气中
ⅱ.然后向三颈烧瓶中通入SO2直至不再产生白色沉淀;
ⅲ.反应完毕后,将装置B中混合物过滤、酒精洗涤、干燥,即得成品。
已知:实验中还观察到装置D中溶液无明显现象,装置E中溶液红色褪去。
请回答下列问题:
(1)检查装置A气密性的操作方法为
(2)装置C的目的是
(3)实验步骤ⅱ中生成白色沉淀的离子方程式为
(4)实验步骤ⅲ中用酒精替代水洗涤的优点是
(5)为探究装置D、E中实验现象,化学兴趣小组对装置E中品红褪色的原因猜想如下:
猜想ⅰ:甲同学认为使品红褪色的微粒主要是
 ;
;猜想ⅱ:乙同学认为使品红褪色的微粒主要是
 ;。
;。为了验证猜想ⅰ和ⅱ,进行以下实验:
将10mL品红水溶液分成两份,在两份溶液中分别加入0.1mol·L-1的
(6)测定产品中
 的含量:称取0.4200g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00mL0.1000mol·L-1H2SO4溶液全部吸收,用0.0900mol·L-1标准NaOH溶液滴定过量的H2SO4,消耗NaOH溶液22.00mL,则样品中NH4CuSO3的质量分数是
的含量:称取0.4200g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00mL0.1000mol·L-1H2SO4溶液全部吸收,用0.0900mol·L-1标准NaOH溶液滴定过量的H2SO4,消耗NaOH溶液22.00mL,则样品中NH4CuSO3的质量分数是a.滴定前仰视滴定管读数,滴定后读数正确
b.NaOH标准溶液使用前敞口放置于空气中一段时间
c.滴定结束读数时,发现滴定管尖嘴处还悬有一滴标准氢氧化钠溶液
d.用H2SO4溶液吸收NH3操作缓慢,导致部分NH3外逸到空气中
您最近一年使用:0次
名校
解题方法
2 . 选择性催化还原法(SCR法)去除 是脱硝问题研究的热点,催化剂的选取是技术的核心。
是脱硝问题研究的热点,催化剂的选取是技术的核心。
(1)以 为催化剂的催化原理:
为催化剂的催化原理: 与
与 形成能提供氢离子的酸性位(如图所示),
形成能提供氢离子的酸性位(如图所示), 吸附在酸性位上生成中间体继续与NO反应。
吸附在酸性位上生成中间体继续与NO反应。 )形式存在,请写出该离子的结构式
)形式存在,请写出该离子的结构式___________ ;
②其他条件相同, 、NO以一定速率,通过一定量
、NO以一定速率,通过一定量 催化剂催化脱硝,当NO含量一定,
催化剂催化脱硝,当NO含量一定,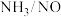 比值大于1.0后NO脱除率变化不大,其原因可能是
比值大于1.0后NO脱除率变化不大,其原因可能是___________ 。
(2)以 为催化剂的反应机理如图1所示:
为催化剂的反应机理如图1所示:___________ 。
②NO脱除率随温度变化如图2所示,温度高于1000℃时NO脱除率明显下降,可能原因是:___________ 。
(3)以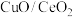 为催化剂
为催化剂
①理想 晶胞如图3所示,实际晶体中会含有部分氧空位。部分
晶胞如图3所示,实际晶体中会含有部分氧空位。部分 填充在由
填充在由 构成的
构成的___________ (填“四面体”或“八面体”)空隙中。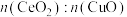 情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在
情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在 或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于
或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于___________ 上(填“ ”或“CuO”);
”或“CuO”);
③测定某催化剂中 质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用
质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用 硫酸亚铁铵[
硫酸亚铁铵[ ]溶液滴定,已知滴定时发生反应为
]溶液滴定,已知滴定时发生反应为 ,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为
,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为___________ (写出计算过程 ,计算结果保留4位有效数字)
 是脱硝问题研究的热点,催化剂的选取是技术的核心。
是脱硝问题研究的热点,催化剂的选取是技术的核心。(1)以
 为催化剂的催化原理:
为催化剂的催化原理: 与
与 形成能提供氢离子的酸性位(如图所示),
形成能提供氢离子的酸性位(如图所示), 吸附在酸性位上生成中间体继续与NO反应。
吸附在酸性位上生成中间体继续与NO反应。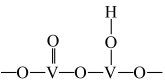
 )形式存在,请写出该离子的结构式
)形式存在,请写出该离子的结构式②其他条件相同,
 、NO以一定速率,通过一定量
、NO以一定速率,通过一定量 催化剂催化脱硝,当NO含量一定,
催化剂催化脱硝,当NO含量一定,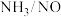 比值大于1.0后NO脱除率变化不大,其原因可能是
比值大于1.0后NO脱除率变化不大,其原因可能是(2)以
 为催化剂的反应机理如图1所示:
为催化剂的反应机理如图1所示:
②NO脱除率随温度变化如图2所示,温度高于1000℃时NO脱除率明显下降,可能原因是:
(3)以
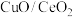 为催化剂
为催化剂①理想
 晶胞如图3所示,实际晶体中会含有部分氧空位。部分
晶胞如图3所示,实际晶体中会含有部分氧空位。部分 填充在由
填充在由 构成的
构成的
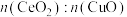 情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在
情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在 或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于
或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于 ”或“CuO”);
”或“CuO”);③测定某催化剂中
 质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用
质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用 硫酸亚铁铵[
硫酸亚铁铵[ ]溶液滴定,已知滴定时发生反应为
]溶液滴定,已知滴定时发生反应为 ,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为
,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为
您最近一年使用:0次
2024-01-21更新
|
397次组卷
|
2卷引用:江苏省海安高级中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
3 . 智能手机因其集成的高清摄像头和智能传感器而常被应用于化学实验。某实验小组利用实验室中的废铁屑(久置但未生锈)制备硝酸铁,并利用配制的硝酸铁标准溶液对“硫酸亚铁补铁剂”中铁元素的含量进行测定。
已知: 溶液有强氧化性,浓度越大,氧化性越强。
溶液有强氧化性,浓度越大,氧化性越强。
实验过程如下:
实验I: 的制备
的制备
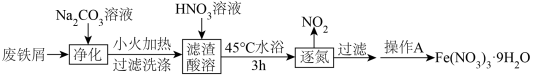
(1)实验室中保存 溶液时,往往加入少许
溶液时,往往加入少许_______ ,目的是_______ 。请简述验证 溶液被部分氧化的实验过程和现象
溶液被部分氧化的实验过程和现象_______ 。
(2)经推测,逐氮过程中的 气体,是
气体,是 发生了分解,写出该反应的化学方程式:
发生了分解,写出该反应的化学方程式:_______ 。
(3)操作A包含的实验步骤有:_______ 、_______ 、过滤、洗涤、干燥。
实验Ⅱ:标准硝酸铁溶液的配制
准确称取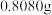 的
的 按如图步骤配成
按如图步骤配成 溶液。
溶液。
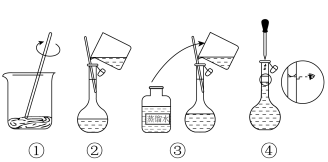
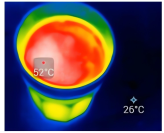
(4)智能手机连接热成像配件FLIROnePro可即时测定过程①中溶液温度。若将如图溶解所得溶液立即转移至容量瓶中并进行定容,则上述操作会导致配得溶液浓度_______ (填“偏高”、“偏低”或“无影响”)。
实验Ⅲ:绘制标准 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线
①分别向7个 容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0
容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0 实验Ⅱ中标定的浓度为
实验Ⅱ中标定的浓度为 的
的 标准溶液,然后分别加入
标准溶液,然后分别加入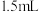 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
②将配好的溶液加入到 比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:

(5)上述实验中,根据合理数据处理得
_______ (保留1位有效数字)。
实验V:“硫酸亚铁补铁剂中铁元素含量的测定
①取补铁剂样品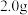 ,加入
,加入 蒸馏水完全溶解,再加入足量
蒸馏水完全溶解,再加入足量 溶液,充分反应后配成
溶液,充分反应后配成 溶液。
溶液。
②取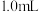 ①中所配溶液于
①中所配溶液于 容量瓶中,加入
容量瓶中,加入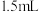 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
将最终配好的溶液加入到 比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
(6)“硫酸亚铁补铁剂”中铁元素的质量分数为_______  (保留2位有效数字)。
(保留2位有效数字)。
(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂中的铁元素含量的有_______。
已知:
 溶液有强氧化性,浓度越大,氧化性越强。
溶液有强氧化性,浓度越大,氧化性越强。实验过程如下:
实验I:
 的制备
的制备
(1)实验室中保存
 溶液时,往往加入少许
溶液时,往往加入少许 溶液被部分氧化的实验过程和现象
溶液被部分氧化的实验过程和现象(2)经推测,逐氮过程中的
 气体,是
气体,是 发生了分解,写出该反应的化学方程式:
发生了分解,写出该反应的化学方程式:(3)操作A包含的实验步骤有:
实验Ⅱ:标准硝酸铁溶液的配制
准确称取
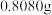 的
的 按如图步骤配成
按如图步骤配成 溶液。
溶液。
(4)智能手机连接热成像配件FLIROnePro可即时测定过程①中溶液温度。若将如图溶解所得溶液立即转移至容量瓶中并进行定容,则上述操作会导致配得溶液浓度

实验Ⅲ:绘制标准
 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线①分别向7个
 容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0
容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0 实验Ⅱ中标定的浓度为
实验Ⅱ中标定的浓度为 的
的 标准溶液,然后分别加入
标准溶液,然后分别加入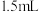 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。②将配好的溶液加入到
 比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:| 比色管编号 | S0 | S1 | S2 | S3 | S4 | S5 | S6 |
 溶液( 溶液( ) ) | 0 | 0.5 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
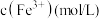 | 0 | 0.0001 | 0.0002 | 0.0004 | 0.0006 | 0.0008 | 0.001 |
| 灰度值 | 127.3 | 119.4 | 107.1 | 87.3 | 65.3 | 47.2 | 29.2 |

(5)上述实验中,根据合理数据处理得

实验V:“硫酸亚铁补铁剂中铁元素含量的测定
①取补铁剂样品
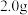 ,加入
,加入 蒸馏水完全溶解,再加入足量
蒸馏水完全溶解,再加入足量 溶液,充分反应后配成
溶液,充分反应后配成 溶液。
溶液。②取
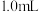 ①中所配溶液于
①中所配溶液于 容量瓶中,加入
容量瓶中,加入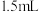 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。将最终配好的溶液加入到
 比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。(6)“硫酸亚铁补铁剂”中铁元素的质量分数为
 (保留2位有效数字)。
(保留2位有效数字)。(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂中的铁元素含量的有_______。
A.提前除去实验I溶解铁屑所用硝酸中的 杂质 杂质 |
B.用浓硝酸溶液代替实验Ⅳ中所用的 溶液 溶液 |
C.整个实验中所用的 溶液均采用相同浓度的溶液 溶液均采用相同浓度的溶液 |
| D.将配制的样品溶液和7个标准溶液放在一起在相同条件下同时拍照,再统一进行数据处理 |
您最近一年使用:0次
名校
4 . 一定条件下,乙酸酐[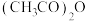 ]醇解反应可
]醇解反应可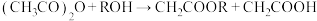 进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入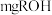 样品充分反应后,加适量水使剩余乙酸酐完全水解:
样品充分反应后,加适量水使剩余乙酸酐完全水解: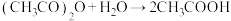 。
。
③加指示剂并用 -甲醇标准溶液滴定至终点消耗标准溶液
-甲醇标准溶液滴定至终点消耗标准溶液 。
。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液
甲醇标准溶液滴定至终点,消耗标准溶液 。
。
对于上述实验,下列做法正确的是
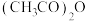 ]醇解反应可
]醇解反应可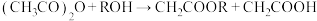 进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:①配制一定浓度的乙酸酐-苯溶液
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入
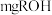 样品充分反应后,加适量水使剩余乙酸酐完全水解:
样品充分反应后,加适量水使剩余乙酸酐完全水解: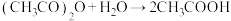 。
。③加指示剂并用
 -甲醇标准溶液滴定至终点消耗标准溶液
-甲醇标准溶液滴定至终点消耗标准溶液 。
。④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
 甲醇标准溶液滴定至终点,消耗标准溶液
甲醇标准溶液滴定至终点,消耗标准溶液 。
。对于上述实验,下列做法正确的是
| A.滴定读数时,应双手一上一下持滴定管 |
| B.滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点 |
C.样品中羟基含量(质量分数)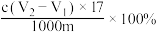 |
| D.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小 |
您最近一年使用:0次
名校
解题方法
5 . 三草酸合铁(Ⅲ)酸钾晶体 为翠绿色晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体的实验步骤如下:
为翠绿色晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体的实验步骤如下:
Ⅰ.制备
ⅰ.称取9.80g摩尔盐[ ,
,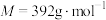 ]加入250mL水中,再加入10mL30%
]加入250mL水中,再加入10mL30% 溶液,搅拌,微热。
溶液,搅拌,微热。
ⅱ.继续加入 氨水至过量,加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得
氨水至过量,加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得 沉淀。
沉淀。
Ⅱ.制备
ⅲ.称取13.00gKOH和10.00g 加入盛有100mL水的烧杯中,加热使其完全溶解后,搅拌,将步骤ii制取的
加入盛有100mL水的烧杯中,加热使其完全溶解后,搅拌,将步骤ii制取的 加入此溶液中。加热,使
加入此溶液中。加热,使 溶解,溶液呈翠绿色。
溶解,溶液呈翠绿色。
ⅳ.过滤,将滤液浓缩。浓缩液转移至50mL烧杯中,后进行冷却结晶,过滤,用少量水和95%乙醇洗涤晶体,干燥,称量晶体质量为9.80g。
已知:二价铁在碱性介质中比酸性介质中更易氧化。请回答下列问题:
(1)步骤ⅰ中微热时,若温度过高,产生的影响是_____ 。
(2)摩尔盐相比硫酸亚铁不易变质,其原因是_____ 。
(3)步骤ⅱ中使用的抽滤装置如图所示,仪器a的作用是_____ 。
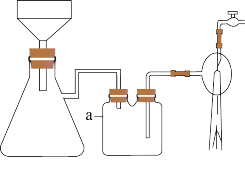
(4)步骤ⅲ中,反应的化学方程式为_____ 。
(5)测定产品中铁的含量。
①称量 样品于锥形瓶中,溶解后用稀
样品于锥形瓶中,溶解后用稀 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。滴定终点的现象是
。滴定终点的现象是_____ 。
②向上述溶液中加入过量锌粉,振荡至反应完全,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。则产品中铁的质量分数的表达式为
。则产品中铁的质量分数的表达式为_____ 。
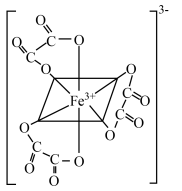
(6)经测定,配离子 具有如图所示的八面体结构,推测其中心原子
具有如图所示的八面体结构,推测其中心原子 的杂化方式为_____(填标号)。
的杂化方式为_____(填标号)。
 为翠绿色晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体的实验步骤如下:
为翠绿色晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体的实验步骤如下:Ⅰ.制备

ⅰ.称取9.80g摩尔盐[
 ,
,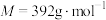 ]加入250mL水中,再加入10mL30%
]加入250mL水中,再加入10mL30% 溶液,搅拌,微热。
溶液,搅拌,微热。ⅱ.继续加入
 氨水至过量,加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得
氨水至过量,加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得 沉淀。
沉淀。Ⅱ.制备

ⅲ.称取13.00gKOH和10.00g
 加入盛有100mL水的烧杯中,加热使其完全溶解后,搅拌,将步骤ii制取的
加入盛有100mL水的烧杯中,加热使其完全溶解后,搅拌,将步骤ii制取的 加入此溶液中。加热,使
加入此溶液中。加热,使 溶解,溶液呈翠绿色。
溶解,溶液呈翠绿色。ⅳ.过滤,将滤液浓缩。浓缩液转移至50mL烧杯中,后进行冷却结晶,过滤,用少量水和95%乙醇洗涤晶体,干燥,称量晶体质量为9.80g。
已知:二价铁在碱性介质中比酸性介质中更易氧化。请回答下列问题:
(1)步骤ⅰ中微热时,若温度过高,产生的影响是
(2)摩尔盐相比硫酸亚铁不易变质,其原因是
(3)步骤ⅱ中使用的抽滤装置如图所示,仪器a的作用是

(4)步骤ⅲ中,反应的化学方程式为
(5)测定产品中铁的含量。
①称量
 样品于锥形瓶中,溶解后用稀
样品于锥形瓶中,溶解后用稀 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。滴定终点的现象是
。滴定终点的现象是②向上述溶液中加入过量锌粉,振荡至反应完全,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀
 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。则产品中铁的质量分数的表达式为
。则产品中铁的质量分数的表达式为(6)经测定,配离子
 具有如图所示的八面体结构,推测其中心原子
具有如图所示的八面体结构,推测其中心原子 的杂化方式为_____(填标号)。
的杂化方式为_____(填标号)。
A. | B. | C. | D. |
您最近一年使用:0次
2024-04-09更新
|
130次组卷
|
3卷引用:河北省沧州市泊头市八县联考2023-2024学年高三下学期3月月考化学试题
6 . 我国科学家用粗氢氧化高钴 制备硫酸钴晶体(
制备硫酸钴晶体(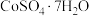 ),其工艺流程如下:
),其工艺流程如下:

已知:ⅰ.还原浸出液中的阳离子有: 、
、 、
、 和
和 等
等
ⅱ.部分物质的溶度积常数(25℃)
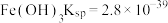
ⅲ.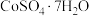 溶解度随温度升高而明显增大
溶解度随温度升高而明显增大
(1)Co元素位于元素周期表的_______ 区,基态Co原子的核外电子排布式为_______ 。
(2)浸出 时,理论上还原性离子和氧化性离子物质的量比为
时,理论上还原性离子和氧化性离子物质的量比为_______ 。
(3)写出“氧化沉铁”的离子方程式_______ ,25℃时,浊液中铁离子浓度为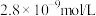 ,此时溶液
,此时溶液
_______ 。
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因_______ 。
(5)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氯化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为: 。
。
已知:铁氰化钾标准液浓度为 ,Co(Ⅱ)标准液质量浓度为
,Co(Ⅱ)标准液质量浓度为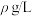 。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗
。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗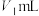 铁氰化钾标准液、
铁氰化钾标准液、 Co(Ⅱ)标准液。
Co(Ⅱ)标准液。
计算样品中钴含量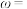
_______ (以钴的质量分数 计)。
计)。
(6)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为_______ 。已知:晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,则该晶胞的高
,则该晶胞的高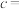
_______  (列出计算式)。
(列出计算式)。

 制备硫酸钴晶体(
制备硫酸钴晶体(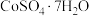 ),其工艺流程如下:
),其工艺流程如下:
已知:ⅰ.还原浸出液中的阳离子有:
 、
、 、
、 和
和 等
等ⅱ.部分物质的溶度积常数(25℃)

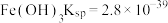
ⅲ.
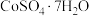 溶解度随温度升高而明显增大
溶解度随温度升高而明显增大(1)Co元素位于元素周期表的
(2)浸出
 时,理论上还原性离子和氧化性离子物质的量比为
时,理论上还原性离子和氧化性离子物质的量比为(3)写出“氧化沉铁”的离子方程式
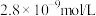 ,此时溶液
,此时溶液
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因
(5)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氯化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为:
 。
。已知:铁氰化钾标准液浓度为
 ,Co(Ⅱ)标准液质量浓度为
,Co(Ⅱ)标准液质量浓度为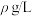 。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗
。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗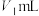 铁氰化钾标准液、
铁氰化钾标准液、 Co(Ⅱ)标准液。
Co(Ⅱ)标准液。计算样品中钴含量
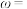
 计)。
计)。(6)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,则该晶胞的高
,则该晶胞的高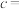
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
7 . 回答下列问题
Ⅰ.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献,下图为联合制碱法的主要过程(部分物质已略去)。

(1)沉淀池中总反应的化学方程式为___________ 。
(2)产品碳酸钠中可能含有氯化钠,验证方法为___________ 。
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
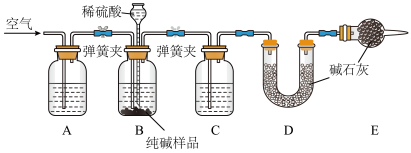
(3)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若___________ ,说明装置不漏气。
(4)装置A中的试剂为___________ (填名称),装置C中的试剂为___________ (填名称)。
(5)实验结束后通入空气的目的:___________ 。
(6)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为___________ (保留小数点后一位);若缺少E装置,会使测定结果___________ (填“偏高”或“偏低”)。
Ⅰ.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献,下图为联合制碱法的主要过程(部分物质已略去)。

(1)沉淀池中总反应的化学方程式为
(2)产品碳酸钠中可能含有氯化钠,验证方法为
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。

(3)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若
(4)装置A中的试剂为
(5)实验结束后通入空气的目的:
(6)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为
您最近一年使用:0次
2023-11-04更新
|
431次组卷
|
2卷引用:江西省赣州市信丰中学2023-2024学年高一上学期11月月考化学试题
8 . 亚硝酸钙是白色粉末,易潮解,易溶于水,微溶于乙醇、乙醚。实验室用NO和CaO2 (淡黄色固体)制备无水亚硝酸钙的装置(夹持装置略)如图所示。
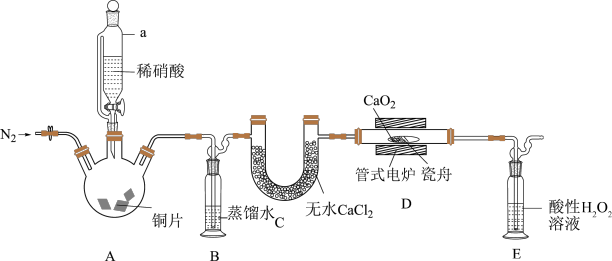
回答下列问题:
(1)实验开始先通N2,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a与普通分液漏斗相比,其优点是___________ 。
(2)装置E中,酸性H2O2溶液可将剩余的NO氧化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(3)CaO2完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②打开止水夹,向装置中通入一段时间N2;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……。则操作②的目的是___________ 。
(4)上述装置存在一处缺陷,会导致亚硝酸钙产率降低,改进的方法是___________ 。
(5)测定所得亚硝酸钙中硝酸钙的含量。
实验原理: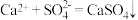 ;
;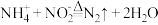
实验步骤: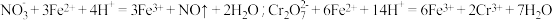
I.准确称取ag所得亚硝酸钙,置于150mL烧杯中,加入100mL蒸馏水和bg足量的硫酸钠,搅拌均匀,将溶液与沉淀全部移入250mL容量瓶,加蒸馏水稀释至刻度,摇匀,过滤;(忽略固体对溶液体积的影响)
Ⅱ.取25.00mL滤液于500mL锥形瓶中,加入足量NH4Cl饱和溶液,煮沸5min;
Ⅲ.冷却后用少量蒸馏水洗涤锥形瓶内壁,再加入25.00mLc₁mol·L-1硫酸亚铁铵[(NH4)2SO4·FeSO4]溶液、在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1:1);
Ⅳ.加4滴指示剂,迅速用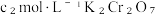 标准液滴定至终点,消耗K2Cr2O7标准液VmL。
标准液滴定至终点,消耗K2Cr2O7标准液VmL。
则所得亚硝酸钙中硝酸钙的质量分数为___________ ;已知在酸性条件下, 可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是
可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是___________ (填标号)。
a.步骤l中,称量时样品发生了潮解
b.步骤Ⅱ中,煮沸时间过短
c.步骤Ⅲ中量取的硫酸亚铁铵溶液的实际体积小于25.00mL
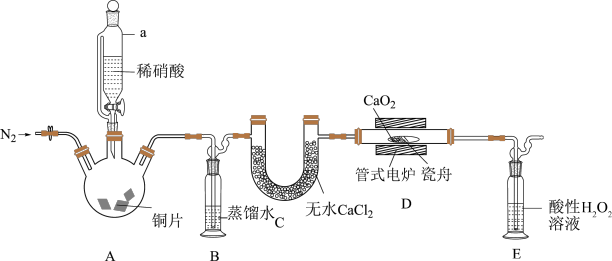
回答下列问题:
(1)实验开始先通N2,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a与普通分液漏斗相比,其优点是
(2)装置E中,酸性H2O2溶液可将剩余的NO氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为(3)CaO2完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②打开止水夹,向装置中通入一段时间N2;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……。则操作②的目的是
(4)上述装置存在一处缺陷,会导致亚硝酸钙产率降低,改进的方法是
(5)测定所得亚硝酸钙中硝酸钙的含量。
实验原理:
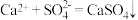 ;
;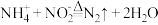
实验步骤:
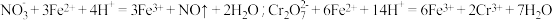
I.准确称取ag所得亚硝酸钙,置于150mL烧杯中,加入100mL蒸馏水和bg足量的硫酸钠,搅拌均匀,将溶液与沉淀全部移入250mL容量瓶,加蒸馏水稀释至刻度,摇匀,过滤;(忽略固体对溶液体积的影响)
Ⅱ.取25.00mL滤液于500mL锥形瓶中,加入足量NH4Cl饱和溶液,煮沸5min;
Ⅲ.冷却后用少量蒸馏水洗涤锥形瓶内壁,再加入25.00mLc₁mol·L-1硫酸亚铁铵[(NH4)2SO4·FeSO4]溶液、在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1:1);
Ⅳ.加4滴指示剂,迅速用
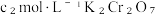 标准液滴定至终点,消耗K2Cr2O7标准液VmL。
标准液滴定至终点,消耗K2Cr2O7标准液VmL。则所得亚硝酸钙中硝酸钙的质量分数为
 可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是
可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是a.步骤l中,称量时样品发生了潮解
b.步骤Ⅱ中,煮沸时间过短
c.步骤Ⅲ中量取的硫酸亚铁铵溶液的实际体积小于25.00mL
您最近一年使用:0次
名校
解题方法
9 . 连二亚硫酸钠(Na2S2O4)是无机精细化学品,在造纸、印染等行业应用广泛。某科研小组通过以下方案制备Na2S2O4并测定其纯度。
已知:①Na2S2O4在空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定。
②低于52℃时Na2S2O4在水溶液中以Na2S2O4·2H2O形态结晶,高于52℃时Na2S2O4·2H2O在碱性溶液中脱水成无水盐。
请回答下列问题:
I.Na2S2O4的制备
其制备过程如下:
步骤1:安装好整套装置(夹持装置省略),并检查装置的气密性;
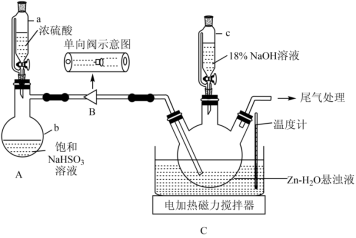
步骤2:在三颈烧瓶中依次加入Zn粉和水,电磁搅拌形成悬浊液;
步骤3:打开仪器a的活塞,向装置C中先通入一段时间SO2;
步骤4:打开仪器c的活塞滴加稍过量NaOH溶液使装置C中溶液的pH在8.2~10.5之间;
步骤5:过滤,将滤液经“一系列操作”可获得Na2S2O4。
(1)仪器a的名称是___________ 。
(2)写出装置A中发生反应的化学方程式:_______ 。
(3)装置B(单向阀)的作用是防倒吸,下列装置能代替它的是_____ (填字母)。
a.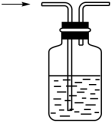 b.
b.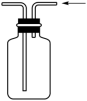
c.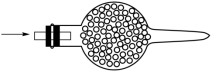 d.
d.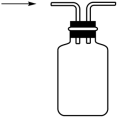
(4)步骤3中生成物为ZnS2O4,该反应需控制温度在35~45℃进行,其原因为___________ 。
(5)步骤4中,需控制溶液的pH在8.2~10.5之间,其原因为:
①pH太大Zn(OH)2会溶解;
②pH太小Zn2+沉淀不完全;
③___________ 。
(6)“一系列操作”包括:
a.搅拌下用水蒸气加热至60℃左右;
b.分批逐步加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液;
c.趁热过滤;
d.用乙醇洗涤。
上述操作的合理顺序为___________ →干燥(填字母)。
Ⅱ.Na2S2O4含量的测定
实验装置:
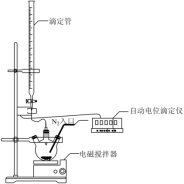
实验原理:[Fe(CN)6]3-+S2O +OH-——SO
+OH-——SO +[Fe(CN)6]4-+H2O(未配平)。
+[Fe(CN)6]4-+H2O(未配平)。
实验过程:称取0.25g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.10mol·L-1,K3[Fe(CN)6]标准溶液,达到滴定终点时消耗24.00mL标准溶液。
(7)样品中Na2S2O4的质量分数为______ %(假设杂质不参与反应);若实验过程中忘记通入N2,对测定Na2S2O4含量的影响是_______ (填“偏低”“偏高”或“无影响”)。
已知:①Na2S2O4在空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定。
②低于52℃时Na2S2O4在水溶液中以Na2S2O4·2H2O形态结晶,高于52℃时Na2S2O4·2H2O在碱性溶液中脱水成无水盐。
请回答下列问题:
I.Na2S2O4的制备
其制备过程如下:
步骤1:安装好整套装置(夹持装置省略),并检查装置的气密性;

步骤2:在三颈烧瓶中依次加入Zn粉和水,电磁搅拌形成悬浊液;
步骤3:打开仪器a的活塞,向装置C中先通入一段时间SO2;
步骤4:打开仪器c的活塞滴加稍过量NaOH溶液使装置C中溶液的pH在8.2~10.5之间;
步骤5:过滤,将滤液经“一系列操作”可获得Na2S2O4。
(1)仪器a的名称是
(2)写出装置A中发生反应的化学方程式:
(3)装置B(单向阀)的作用是防倒吸,下列装置能代替它的是
a.
 b.
b.
c.
 d.
d.
(4)步骤3中生成物为ZnS2O4,该反应需控制温度在35~45℃进行,其原因为
(5)步骤4中,需控制溶液的pH在8.2~10.5之间,其原因为:
①pH太大Zn(OH)2会溶解;
②pH太小Zn2+沉淀不完全;
③
(6)“一系列操作”包括:
a.搅拌下用水蒸气加热至60℃左右;
b.分批逐步加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液;
c.趁热过滤;
d.用乙醇洗涤。
上述操作的合理顺序为
Ⅱ.Na2S2O4含量的测定
实验装置:

实验原理:[Fe(CN)6]3-+S2O
 +OH-——SO
+OH-——SO +[Fe(CN)6]4-+H2O(未配平)。
+[Fe(CN)6]4-+H2O(未配平)。实验过程:称取0.25g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.10mol·L-1,K3[Fe(CN)6]标准溶液,达到滴定终点时消耗24.00mL标准溶液。
(7)样品中Na2S2O4的质量分数为
您最近一年使用:0次
名校
10 . 废旧锌锰电池中的黑锰粉含有MnO2、MnO(OH)、NH4Cl和少量ZnCl2、Fe2O3及炭黑等,为了保护环境、充分利用锰资源,通过如下流程制备MnSO4。
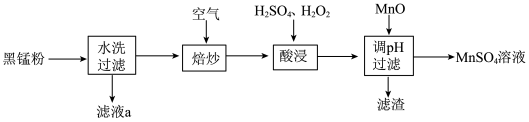
(1)Mn2+的价电子排布式为_______ 。
(2)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为_______ 。
(3)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡:再加入稀H2SO4,固体未明显溶解。
实验Ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是_______ ,实验Ⅱ中发生反应的离子方程式为_______ 。
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是_______ 。
(4)最近科学家研制出超薄铁磁β-MnSe半导体,β-MnSe的晶胞结构如图所示。β-MnSe中Mn的配位数为_______ 。

(5)MnSO4可通过反应制得Mn3O4,在加热烘干Mn3O4过程中常常混有Mn2O3杂质,现对样品中Mn3O4的含量进行测定。取Mn3O4样品22.19g加入足量浓盐酸并加热,得到标准状况下2.24L氯气。(Mn3O4和Mn2O3在加热时均能和浓盐酸反应生成MnCl2)计算样品中Mn2O3的质量分数为_______ 。(写出计算过程)

(1)Mn2+的价电子排布式为
(2)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为
(3)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡:再加入稀H2SO4,固体未明显溶解。
实验Ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是
(4)最近科学家研制出超薄铁磁β-MnSe半导体,β-MnSe的晶胞结构如图所示。β-MnSe中Mn的配位数为

(5)MnSO4可通过反应制得Mn3O4,在加热烘干Mn3O4过程中常常混有Mn2O3杂质,现对样品中Mn3O4的含量进行测定。取Mn3O4样品22.19g加入足量浓盐酸并加热,得到标准状况下2.24L氯气。(Mn3O4和Mn2O3在加热时均能和浓盐酸反应生成MnCl2)计算样品中Mn2O3的质量分数为
您最近一年使用:0次



